¶ MANUAL DE MÉTODOS OFICIAIS PARA DIAGNÓSTICO LABORATORIAL DE DOENÇAS DOS ANIMAIS - Volume VII - PARTE D - MULTIESPÉCIES
¶ Folha de rosto
© 2025 Ministério da Agricultura e Pecuária. Todos os direitos reservados. É permitida a reprodução parcial ou total desta obra, desde que citada a fonte e que não seja para venda ou qualquer fim comercial. A responsabilidade pelos direitos autorais de textos e imagens desta obra é do autor.
Ano 2025
Elaboração, distribuição, informações:
Ministério da Agricultura e Pecuária
Secretaria de Defesa Agropecuária - SDA
Departamento de Serviços Técnicos - DTEC
Esplanada dos Ministérios, Bloco D, Anexo, Ala B, 4º andar, sala 433
CEP: 70043-900, Brasília - DF
www.agricultura.gov.br
e- mail: cgal@agro.gov.br
Central de Relacionamento: 0800 704 1995
Equipe Técnica:
Ana Cristina Gonçalves Pinto da Rocha
Ana Carolina de Oliveira Nascimento
Anapolino Macedo de Oliveira
Aerlem Cynara Silva
Ana Karina Cunha Callado
Andrea Padilha de Alencar
Anselmo Vasconcelos Rivetti Júnior
Antônio Augusto Fonseca Júnior
Cid Aristóteles de Siqueira Alencar
Dilmara Reischak
Fernanda Gomes Cardoso
Isabela Ciarlini de Azevedo
João Marcos Nacif da Costa
Juliana Nabuco Pereira Otaka
Luanda Bispo Santos do Nascimento Maués
Luciana Amaral Pinto
Luciana Rabello Ferreira
Luciana Taborda Corrêa
Marcelo Fernandes Camargos
Marco Antônio de Carvalho Marques Serqueira
Paulo Martins Soares Filho
Patrícia Gomes de Souza
Rene Ribeiro da Silva
Sheila de Matos Xavier
Silvio Orlan de Castro Chaves
Soraya Cecilia Albieri Camillo
CGAL
¶ Folha resumo
|
Macroprocesso: Laboratórios |
Objetivo: Realizar a padronização, harmonização, atualização e a unificação dos procedimentos para execução de ensaios laboratoriais da área de Diagnóstico Animal, , destinadas aos laboratórios oficiais e credenciados da Rede Nacional de Laboratórios Agropecuários |
|||
|
Processo: Análises Laboratoriais |
||||
|
Entrega: Segurança e saúde dos rebanhos animais |
Público alvo e demais interessados: Laboratórios oficiais e credenciados do Ministério da Agricultura e Pecuária (Mapa) |
Versão do documento: 2 |
||
|
Setor responsável e responsabilidades A Coordenação Geral de Laboratórios Agropecuários do Departamento de Serviços Técnicos é responsável pela elaboração, atualização e envio para aprovação deste manual, tendo responsabilidade quanto aos procedimentos descritos no documento. |
||||
¶ 1. Definições e conceitos
¶ 1.1 Definições
Não aplicável.
¶ 1.2 Conceitos
Não aplicável.
¶ 2. Responsabilidades
O presente manual possui vigência e prazo indeterminados e será revisado sempre que necessário, pela Coordenação Geral de Laboratórios Agropecuáriosdo Departamento de Serviços Técnicos (CGAL/DTEC).
A gestão desse manual está sob a responsabilidade da CGAL/DTEC que prestará auxílio ao público alvo leitor dúvidas e/ou sugestões quanto à aplicação deste manual devem ser submetidas ao Departamento responsável.
A publicação e atualização das versões na plataforma oficial da SDA para acesso pelo público alvo será de responsabilidade da Secretaria representada pelo DTEC.
¶ 3. Objetivo
O objetivo do Manual é reunir os métodos analíticos a serem empregados na execução de ensaios laboratoriais da área de Diagnóstico Animal da Rede Nacional de Laboratórios Agropecuários (Rede LFDA e Laboratórios credenciados junto ao Ministério da Agricultura e Pecuária).
¶ 4. Procedimentos
¶ 4.1. Tuberculose
¶ 4.1.1. Amostras
São consideradas amostras para o diagnóstico da Tuberculose, amostras de tecidos ou órgãos de animais infectados com o microrganismo, com ou sem lesões sugestivas de tuberculose:
I - Isolamento
a) linfonodos.
b) Fígado.
c) Pulmão.
d) Lesões sugestivas.
II - PCR (Biologia molecular)
a) Linfonodos.
b) Fígado.
c) Pulmão.
d) Cultura bacteriana.
e) Lesões sugestivas.
¶ 4.1.2. Recebimento das Amostras
I – A manipulação das amostras para isolamento e para biologia molecular para a detecção de Mycobacterium deverá ser realizada em nível de biossegurança 3.
II – Para a PCR, todos os procedimentos após o tratamento das amostras serão realizados no laboratório com nível 1 de biossegurança.
III – Todas as amostras recebidas para diagnóstico de Tuberculose deverão ser registradas em formulário próprio. Neste mesmo formulário, deverão ser preenchidos, no momento do processamento da amostra, os campos Lesão (sim ou não) e Início da análise.
IV – No caso das amostras que forem submetidas a diagnóstico por isolamento, deve-se registrar os dados do diagnóstico em formulário próprio.
V – Quando for necessário o estoque das culturas de campo isoladas, registrar o estoque em formulário próprio.
VI – Para atendimento aos Programas e Controles Oficiais do MAPA os laboratórios credenciados somente receberão as amostras previstas na legislação em vigor para as finalidades e ensaios previstos no seu escopo de credenciamento.
VII – Deverão ser obedecidos os critérios de verificação de conformidade das amostras estabelecidos no Volume I - REGRAS GERAIS.
VIII – As amostras deverão ser encaminhadas congeladas ao laboratório, individualmente e obedecendo a critérios de biossegurança.
¶ 4.1.3. Diagnóstico Molecular
I – O desempenho dos métodos de ensaio deverá ser verificado conforme definições estabelecidas pelo Manual da CGAL para validação de métodos moleculares.
II – Todos os insumos utilizados na análise devem ser controlados e previamente testados e aprovados.
III – O laboratório deverá realizar os ensaios obedecendo às temperaturas preconizadas pelo fabricante dos insumos.
Nota 1: Com relação às temperaturas preconizadas pelo fabricante dos insumos:
I – Quando esta informação não constar na bula o laboratório deverá consultar o fabricante, mesmo que a indicação seja de realização a temperatura ambiente.
II – Quando não informado pelo fabricante, serão considerados como temperatura ambiente, valores de temperatura entre 18 e 25ºC.
IV – Antes da utilização dos insumos, realizar a avaliação de todos os parâmetros referentes aos lotes e valores de ponto de corte dos critérios interpretação dos resultados.
V – O laboratório deve estabelecer um meio de avaliação apropriado para todos os insumos utilizados nos ensaios.
VI – Devem ser retidos os registros dos controles dos ensaios realizados, devendo ser registrada data e responsável de todas as etapas realizadas para cada amostra analisada.
VII – Os resultados encontrados para cada amostra e controles, dados dos insumos utilizados e outras informações pertinentes devem ser registrados em formulários próprios e/ou sistema informatizado do próprio laboratório.
Nota 2: A utilização de sistemas informatizados para registros apenas é permitida quando:
I – A inclusão dos dados for realizada durante a execução e leitura do ensaio, sem anotação prévia em formulários de papel. Dados transcritos não são considerados dados brutos.
II – As alterações de informações estejam prontamente disponíveis e rastreáveis, sem a necessidade de intervenção de especialistas em informática ou geração de logs ou equivalentes.
III – O dado anterior, o responsável pela alteração e a data da realização da alteração estiver prontamente disponível.
VIII – O diagnóstico direto (isolamento e biologia molecular) refere-se à identificação do agente causador da brucelose.
IX – A amplificação de fragmentos do genoma de M. bovis ou de micobactérias do complexo M. tuberculosis, através da utilização de iniciadores específicos, pela técnica de PCR permite inferir a presença destes microrganismos na amostra clínica.
X – O diagnóstico molecular de tuberculose é dado a partir de duas reações de qPCR. A reação denominada IS1081 é realizada primeiro, e tem como alvo o elemento de inserção IS1081 presente em bactérias do complexo M. tuberculosis. Já a reação denominada RD4.88 tem como iniciadores, regiões que flanqueiam uma deleção específica no genoma de M. bovis, conhecida como região de diferença 4 (RD4). Isso garante que os produtos de PCR formados na reação sejam apenas do genoma do M. bovis, visto que, em genomas de outros organismos do complexo M. tuberculosis, o tamanho da região entre os iniciadores é grande o suficiente para inviabilizar a qPCR. Em caso de resultado negativo na IS1081, a mesma amostra de DNA é submetida à RD4.88.
XI – Quando pertinente, o diagnóstico pode ser completado a critério do analista e responsável, pela confirmação através do sequenciamento genético. Neste caso, a amostra de DNA pode ser submetida a três reações de PCR convencional, denominadas Mtub-gyrB, TB11/TB12 (ambas tendo o genoma de bactérias do complexo M. tuberculosis como alvo) e Mb400 (específica para M. bovis).
XII – A PCR em tempo real desenvolvida para avaliar a qualidade da extração de DNA das amostras de tecido é denominada β-actina58 e tem por alvo o genoma de bovinos, ovinos e suínos. Ela não detecta genoma de equinos e outros animais que não sejam bi-ungulados.
¶ Técnicas de diagnóstico de tuberculose animal
¶ A - Isolamento
¶ Materiais
- Areia lavada estéril.
- Conjuntos de gral / pistilo, tamanho médio, com aproximadamente 12 cm de diâmetro.
- Dosador de 3 a 5g.
- Pratos de alumínio ou placas de Petri de vidro de aproximadamente 14,5 cm de diâmetro.
- Pinças dente de rato.
- Papel alumínio.
- Fitas de pH 6-10, intervalo de 0,3 a 0,5.
- Fitas de pH 1-11, intervalo de 1.
- Sacos plásticos autoclaváveis para descarte de material contaminado.
- Sacos plásticos para armazenar amostra (500 mL), resistentes à perfuração e com fechamento a prova de vazamento.
- Cabos de Bisturi (nº 4).
- Lâminas de bisturi (nº 21).
- Tesouras.
- Pipetas de vidro graduadas de 1 mL ou 2 mL, estéreis.
- Tubos de centrífuga de 50 mL, estéreis.
- Suportes para inclinar tubos de ensaio na horizontal.
- Estantes para suporte dos tubos de centrífuga de 50 mL.
- Estantes para suporte dos tubos Eppendorf ou criotubos de 2 mL.
- Balão de fundo chato ou Erlenmeyer estéril de 2000 mL (para recolher o resíduo).
- Lâminas para microscopia com extremidade fosca.
- Eppendorf ou criotubos de 2 mL.
- Bastões de metal estéreis.
- Papel para proteção de bancada ou equivalente.
- Gaze.
- Caneta de retroprojetor.
- Alça bacteriológica 10 µL, descartável, estéril.
- Descarte de alças bacteriológicas contaminadas.
- Caixa para armazenar criotubos de 2 mL.
- Etiquetas autocolantes.
- Cubas para descarte de pipetas.
- Cubas ou bandejas para degelo de amostras.
- Tubos de ensaio 16 x 150 mm com tampa de rosca.
¶ Equipamentos e instrumentos
- Cabine de Segurança Biológica (CSB) Classe II tipo A.
- Estufa bacteriológica a 36 ºC ± 1 ºC.
- Centrífuga refrigerada com capacidade para tubos de 50mL e 3000 x g.
- Autoclave de fronteira.
- Refrigerador.
- Congelador.
- Timer digital.
- Microscópio ótico.
- Pipetadores.
- Banho maria.
- Registrador de Temperatura.
¶ Insumos - Meios de cultura
- Meio Lowenstein-Jensen (LJ) - opcional.
- Meio Stonebrink (SB).
- Meio Middebrook 7H9 20% glicerol - opcional.
- Meio Middlebrook 7H11 com aditivos.
¶ Soluções
- Solução de ácido sulfúrico 6 %.
- Solução tampão de fosfato de sódio bibásico ou solução salina 0,48% fosfatada tamponada (PBS) pH 7,2 - 7,4.
- Água destilada estéril.
- Solução de Virkon 3,0% - opcional.
- Solução de hipoclorito 10 -12 % ( solução estoque para preparo de solução de hipoclorito 1 %).
- Solução de hipoclorito 1 %.
- Solução de ácido peracético 15 % (solução estoque para preparo de solução de ácido peracético 0,35 %).
- Solução de ácido peracético 0,35%.
- Solução para estoque de micobactéria com soro equino.
- Solução de tampão TE 1x.
- Solução de SDS a 10%.
- Solução de proteinase K 10 mg/Ml.
- Álcool 70%.
¶ Realização do ensaio
¶ Preparação do tecido
a) Descongelar as amostras colocando-as em recipientes apropriados sob refrigeração “Over night” ou à temperatura ambiente por algumas horas até que descongele.
b) Dentro da Cabine de Segurança Biológica (CSB), abrir o frasco da amostra e, com a ajuda de uma pinça, colocar o tecido em um prato de alumínio/placa de Petri e avaliá-lo macroscopicamente para verificar a presença e as características das lesões (figuras 1, 2 ,3 e 4). Em seguida, com auxílio de pinça e bisturi, deve-se seccionar o tecido em pequenos fragmentos.
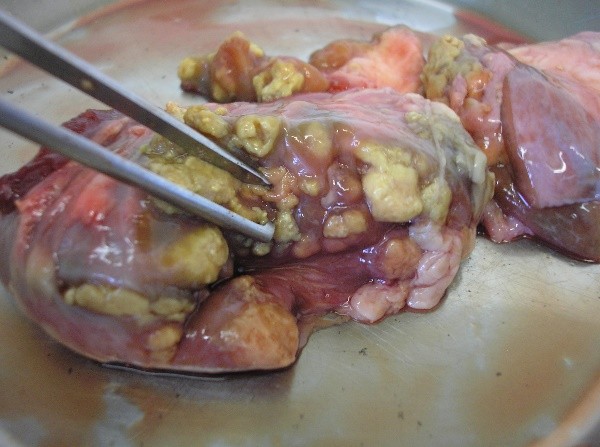
|
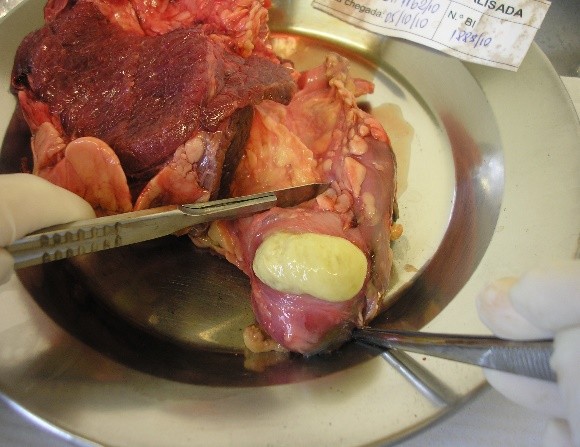
|
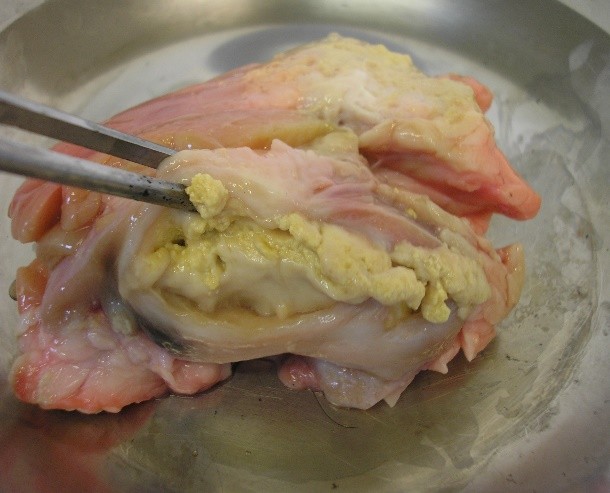
|
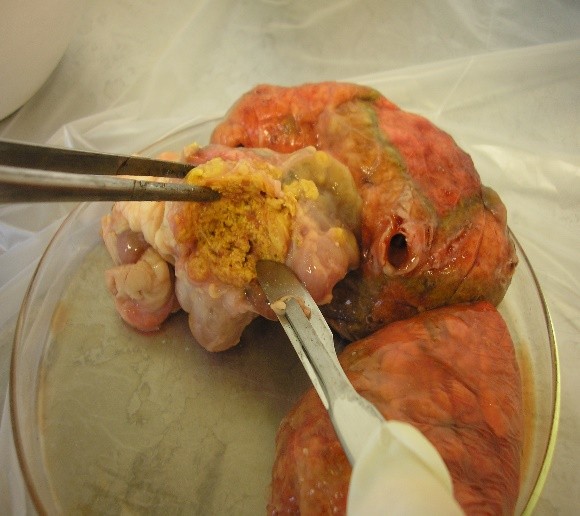
|
¶ Trituração da amostra
- Caso a amostra seja destinada a realização de isolamento, deve-se selecionar partes do tecido que contenham lesão e interface com tecido sadio e picotar em fragmentos pequenos. Após transferir uma porção aproximada de 3 g a 5 g da amostra fragmentada para o gral, salpicar a areia sobre o material e com o auxílio de um pistilo, triturar até obter um macerado homogêneo.
- Caso a amostra de tecido não apresente lesão típica, picotar uma quantidade suficiente da amostra. Transferir uma porção aproximada de 3 g a 5 g do material fracionado para um gral identificado com o número da amostra. Caso haja sobra adequada de tecido, separar de 3 g a 5 g do material picotado em sacos plásticos de tamanho adequado para armazenagem das mesmas (aproximadamente 50 mL), resistentes à perfuração e com fechamento à prova de vazamento, identificando-o com o número da amostra e congelando-o em seguida. Essa porção poderá ser utilizada em caso de necessidade de reprocessamento.
¶ Descontaminação com ácido sulfúrico 6 %
- Adicionar à amostra já triturada, aproximadamente 40 mL de ácido sulfúrico 6%, cobrindo todo o material. Homogeneizar levemente. Controlar o tempo de contato do ácido com a amostra. Registrar em formulário a hora em que o ácido foi adicionado à amostra.
- Centrifugar até se obter líquido transparente e material sedimentado no fundo do tubo. Sugere-se centrifugar por quinze minutos a 3000 x g sob refrigeração.
- Após centrifugação, descartar cuidadosamente o sobrenadante em balão ou erlenmeyer de volume apropriado, e neutralizar a acidez do material sedimentado no fundo do tubo com aproximadamente 40mL de tampão fosfato de sódio bibásico.
- O tempo total de contato do material com o descontaminante não deve exceder trinta minutos, incluindo os quinze minutos da centrifugação.
¶ Neutralização
- Com o auxílio de um bastão de metal, ressuspender o sedimento do fundo do tubo com aproximadamente 40 mL de solução tampão de fosfato de sódio bibásico. Registrar em formulário a hora em que o tampão foi adicionado ao sedimento (fim do contato do ácido com o material em análise). Pingar uma gota do sobrenadante no papel indicador e conferir o pH.
- Se o pH estiver em torno da neutralidade (6.0 - 7.0), aguardar 10 minutos aproximadamente, aspirar 1 mL da parte turva logo acima da massa de tecido sedimentada com pipeta graduada de 2 mL ou 1 mL e inocular em meios de cultura.
- Se o pH ainda estiver ácido, centrifugar novamente até se obter líquido transparente e material sedimentado ao fundo do tubo. Descartar o sobrenadante, ressuspender o material com aproximadamente 40 mL de solução salina 0,48% fosfatada tamponada (PBS) pH 7,2 - 7,4 ou tampão fosfato de sódio bibásico e conferir o pH do sobrenadante novamente.
¶ Inoculação nos meios de cultura
- Para cada amostra, semear dois tubos de meio Middlebrook 7H11 com aditivos e dois tubos de meio Stonebrink com aproximadamente 0,2 mL de inóculo em cada um. Os tubos devem ser identificados com o número da amostra correspondente, a data da análise e com a sequência numérica do tubo.
- Movimentar os tubos de forma que o inóculo entre em contato com toda a superfície do meio.
- Incubar os tubos semeados na posição horizontal, em suportes próprios, em estufa a 36 ºC ± 1 ºC, com a tampa afrouxada (aproximadamente 1/3 de volta), até a secagem do inóculo (aproximadamente uma semana).
- Após este tempo, colocar os tubos na vertical com as tampas apertadas, e continuar com a incubação em estufa a 36 ºC ± 1 ºC, por até dez semanas.
- Quando a intenção for tentar isolar outro tipo de micobactéria que não seja M. Bovis pode-se utilizar também o meio Meio Lowenstein-Jensen (LJ).
- Para cada amostra, semear dois tubos de meio Middlebrook 7H11 com aditivos e dois tubos de meio Stonebrink com aproximadamente 0,2 mL de inóculo em cada um. Os tubos devem ser identificados com o número da amostra correspondente, a data da análise e com a sequência numérica do tubo.
- Movimentar os tubos de forma que o inóculo entre em contato com toda a superfície do meio.
- Incubar os tubos semeados na posição horizontal, em suportes próprios, em estufa a 36 ºC ± 1 ºC, com a tampa afrouxada (aproximadamente 1/3 de volta), até a secagem do inóculo (aproximadamente uma semana).
- Após este tempo, colocar os tubos na vertical com as tampas apertadas, e continuar com a incubação em estufa a 36 ºC ± 1 ºC, por até dez semanas.
¶ Acompanhamento semanal
Verificar, semanalmente, se houve crescimento de UFC típica em algum tubo de meio incubado e registrar o resultado observado. As características das UFCs de M. bovis em meio de cultura Middlebrook 7H11 são: aspecto rugoso, bordas irregulares e cor acastanhada, aparecem aproximadamente a partir da segunda semana, sendo mais visíveis a partir da terceira semana (Figura 5). Em meio de cultura Stonebrink (SB) as características das colônias são: arredondadas com bordos regulares ou não, às vezes em forma de ovo frito, cor creme e brilhante, aparecem aproximadamente a partir da terceira semana, sendo mais visíveis a partir da quinta semana (Figura 6).

|

|
¶ Resultado do isolamento
Ao final de no máximo dez semanas de incubação dos tubos de meio de cultura, o resultado do isolamento será um dos seguintes:
- UFC típica de M. bovis: isolamento de ao menos uma UFC típica visível em qualquer um dos tubos.
- Ausência de crescimento: nenhuma UFC típica observada.
- Contaminação dos tubos: quando todos os tubos de meios de cultura sofrerem contaminação. Se restar ao menos um tubo de meio de cultura sem contaminação (e sem crescimento de UFC típica), o resultado do isolamento será ausência de crescimento.
Registrar estes resultados.
¶ Testes de identificação
- Em caso de isolamento de UFC típica, uma suspensão do isolado deverá ser encaminhada para biologia molecular para a realização de testes de identificação.
- Para enviar UFCs isoladas biologia molecular, transferir, com o uso de alça bacteriológica, uma quantidade de crescimento para um Eppendorf/criotubo contendo aproximadamente 1,5 mL de tampão TE 1X, suficiente para turvar o tampão (Sugerem-se duas alças cheias de crescimento). Previamente ao envio, o criotubo/Eppendorf deverá ser identificado. Em caso, de estoque desta suspensão, a mesma deve ser mantida congelada a -20ºC. Antes do envio para biologia molecular, a amostra deverá ser inativada em banho-maria por temperatura de 87 ºC + 5 ºC por 1 hora.
- Caso o envio não seja realizado logo após a inativação, guardar o Eppendorf/criotubo em caixa própria para armazenar criotubos de 2 mL. Etiquetar a caixa externamente identificando as culturas como inativadas e incubar em freezer até o envio.
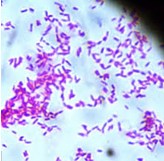
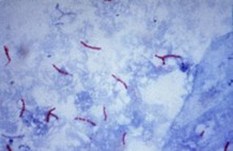
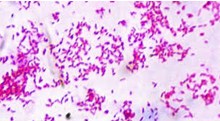
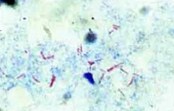
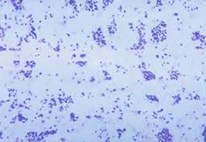
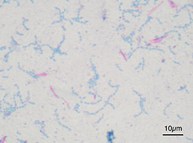
- Caso haja dúvida de se tratar de uma UFC típica, a critério do analista e/ou do responsável pelo setor, poderá ser confeccionada uma lâmina com o esfregaço da colônia e realizada a coloração pelo método de Ziehl-Neelsen, visando à verificação da presença de BAAR (Bacilo Álcool-Ácido Resistente), antes de encaminhá-la para testes de identificação:
- BAAR: bastonetes delgados, ligeiramente curvos, isolados, aos pares ou em grupos corados em vermelho com o fundo azul.
- Outros microrganismos: corados em azul.
|
|
|
|
|
|
Alternativamente, a identificação das culturas bacterianas obtidas no isolamento poderá ser realizada por meio de provas bioquímicas.
Existindo necessidade de estocagem de amostras de culturas isoladas de Mycobacterium spp., deve-se proceder tal procedimentos em criotubos/Eppendorf contendo Soro Equino ou Meio Middebrook 7H9 20% glicerol.
¶ Reprocessamento da amostra
O reprocessamento deverá ocorrer quando se tratar de uma amostra que apresente lesões típicas e cujo resultado do isolamento após incubação tenha sido um dos seguintes:
- Ausência de crescimento.
- Contaminação dos tubos.
- Outras situações, de acordo com avaliação técnica realizada por pessoal qualificado (analistas e/ou responsável pelo setor)
O reprocessamento só poderá ocorrer se, durante a etapa de preparação da amostra, tiver sido possível a separação de uma porção adequada de tecido para reprocessamento.
¶ Emissão dos resultados
I – Os resultados deverão ser emitidos em documento denominado “Relatório de Ensaio”.
¶ Descarte de Amostras e Resíduos
I – Anteriormente ao descarte de amostras e produtos de ensaio, deve ser realizado registro de descarte em formulário próprio e conferência.
II – Os materiais descartados devem ser separados adequadamente entre resíduos químicos e biológicos.
III – O laboratório deve assegurar a biossegurança dos resíduos gerados, e seguir as legislações ambientais vigentes durante todo o processo do descarte.
IV – O resíduo obtido da descontaminação e neutralização da amostra tecidual, antes da autoclavação, deverá ser tratado adequadamente.
V – As superfícies de trabalho devem ser desinfetadas antes e ao final dos trabalhos ou imediatamente após qualquer derramamento de material infeccioso, com solução de Virkon 3,0%, solução de hipoclorito 1% (em caso de pouca ou nenhuma matéria orgânica) ou solução de ácido peracético 0,35 %, por no mínimo 10 minutos.
¶ Retenção de itens de ensaio
I – As amostras de espécimes clínicos poderão ser descartadas 60 dias após a emissão do relatório de ensaio.
II – As colônias de Mycobacterium spp. isoladas poderão ser recolhidas em veículos de liofilização e congeladas a -70ºC para posterior envio ao LFDA-MG.
¶ B - PCR em Tempo Real - qPCR
¶ Materiais
- Microplacas ou microtubos para leitura óptica de qPCR.
- Selante para microplacas para leitura óptica de qPCR.
- Microtubos de 0,5mL e 1,5mL (para preparo do mix de reação).
- Caneta de retroprojetor permanente.
- Descartador.
- Luvas descartáveis para procedimento.
- Ponteiras com filtro.
- Estantes para microtubos.
¶ Equipamentos e instrumentos
- Micropipetas cujos volumes sejam adequados ao protocolo de extração utilizado, e à quantidade total de mix de qPCR a ser preparado.
- Equipamento de extração específico de acordo com a metodologia adotada.
- Termociclador para PCR em Tempo Real.
- Cabine de segurança biológica com filtro HEPA classe II (requisito mínimo) ou estação de trabalho para PCR (Workstation PCR) com luz UV germicida;
- Agitador de tubos.
- Centrífuga para microtubos e microplacas.
¶ Insumos
- Água livre de nucleases.
- Tampão TE pH 8,0.
- MgCl2 25mM.
- oligonucleotídeos descritos no Quadro 1.
- Master mix para qPCR.
- Kit de extração de DNA.
Quadro 1: Oligonucleotídeos utilizados para qPCR
| Oligonucleotídeo | Tipo de PCR | Sequência | Referência |
|
Mbo.IS1081.124.F Mbo.IS1081.124.R Mbo.IS1081.124.S |
qPCR |
5´-AGGAACGCCTCAACCGAGAG-3’ 5´-CCTTCGATCCATTCGTCGTG3-’ 5´FAM-CGACGCCGAACCGACGTCGTC-BHQ13’ |
Sales et al., 2014a Soares Filho et al., 2019 |
|
Mbo.RD4.88.F Mbo.RD4.88.R Mbo.RD4.88.S |
qPCR |
5’-CGCCTTCCTAACCAGAATTG-3’ 5’-GGAGAGCGCCGTTGTAGG3-’ 5´FAM-AGCCGTAGTCGTGCAGAAGCGCA-BHQ1-3’ |
Moura et al., 2016 |
|
β-actina.58.F β-actina.58.R β-actina.58.S |
qPCR |
5’-TGCCGGAGCCGTTGT-3’ 5’-AACCAGTTCGCCATGGAT-3’ 5’FAM-TGATATTGC-ZEN-TGCGCTCGTGGTC-ABKFQ-3’
|
Bielanski et. al., 2009 |
Nota: Para análise do gene constitutivo aplicada a amostras de mamíferos e outros vertebrados que não sejam bi-ungulados, sugere-se o uso do conjunto de oligonucleotídeos para 18S conforme Quadro 1.
¶ Padrões (controles positivos)
O padrão positivo (IS1081 e RD4.88) deve ser o DNA extraído das amostras de referência M. bovis AN5 ou M. bovis BCG ou equivalentes disponíveis no laboratório.
O padrão positivo para β-actina deve corresponder ao DNA extraído de uma amostra de campo.
O padrão positivo deve ser diluído de forma a se obter um Ct (Cycle Threshold) entre 20 e 35.
Nota: A cada análise, sugere-se que seja preenchida uma carta controle. Quando for detectado desvio em relação ao limite superior da carta controle, ainda que o mesmo esteja abaixo de 35, convém investigar e de acordo com critério do analista, a reação deverá ser repetida com o uso de nova diluição da solução estoque do padrão positivo.
¶ Soluções
- Solução de Álcool 70%.
- Solução descontaminante de moléculas residuais de RNAs / DNAs / amplicons /resíduos de proteínas de superfícies, entre as quais DNAses/RNAses.
¶ Realização do ensaio
¶ Processamento de amostras destinadas a PCR direto de tecido animal
Caso a amostra seja destinada a realização de PCR direto a partir de amostra de tecido animal deve-se separar um fragmento de tecido, de aproximadamente 0,5 a 1,0 gramas, preferencialmente com lesão sugestiva de tuberculose, e acondicionar em criotubo contendo 500 microlitros de solução constituída por 450 µl de TE 1X e 50 µl de SDS a 10%.
A inativação e a extração da amostra serão realizadas simultaneamente através da adição de 50 µl de proteinase K e subsequente incubação em banho Maria a 56,5 ºC + 3,5 ºC (são aceitáveis valores entre 20 ºC e 60 ºC, conforme orientação dos manuais dos fabricantes da enzima) por processo overnight.
Em caso de estoque das amostras de tecido para PCR, realizar o procedimento até a etapa de acréscimo da solução de TE 1X/SDS 10% e congelá-las a uma temperatura menor que -20 °C.
¶ Extração do DNA
A extração de DNA poderá ser realizada através de método automatizado, como por exemplo extração automatizada por beads magnéticas, ou por processo manual como por exemplo extração por colunas de sílica. Os métodos manuais utilizando kits de colunas de sílica são alternativas para o processamento de poucas amostras ou em caso de impossibilidade do uso dos equipamentos automáticos. Os procedimentos analíticos de extração de DNA deverão ser registrados em planilha específica.
Nota: Extrair juntamente com as amostras, um Controle de Extração (CE), correspondendo apenas aos reagentes empregados na metodologia. Este controle é dispensável nos métodos automatizados, como por exemplo, extração por beads magnéticas, cuja manipulação da amostra e processos manuais são mínimos. Já para extração de DNA por coluna, cujo método implica em diversas etapas de transferência da amostra, o Controle de Extração é obrigatório.
¶ Diluição dos oligonucleotídeos
- Ressuspender os oligonucleotídeos (iniciadores e sondas liofilizados) em tampão TE pH=8, de modo que a solução estoque seja de 500pmol/µL. É recomendável utilizar vórtex de tubos para dar um spin no tubo liofilizado antes de abri-lo.
- Para a detecção de M. bovis (primer Mbo.RD4.88) recomenda-se as seguintes concentrações das soluções de trabalho: sonda a 40pmol/µL e iniciadores a 60pmol/µL. Usar como diluente água livre de nucleases.
- Para a detecção de bactérias do complexo M. tuberculosis (primer IS1081.124) recomenda-se as seguintes concentrações das soluções de trabalho: sonda a 25pmol/µL e iniciadores a 30pmol/µL. Usar como diluente água livre de nucleases.
- Para a detecção do gene constitutivo do hospedeiro β-actina recomenda- se soluções de trabalho de todos os oligonucleotídeos a 10pmol/µL. Usar como diluente água livre de nucleases.
Nota: Outras diluições podem ser calculadas de acordo com os volumes necessários para o teste, desde que atendam a concentração final prescrita para o protocolo.
¶ Preparo do Mix de Reação
- Os procedimentos de registro do preparo do mix deverão ser registrados em planilha específica
- Descongelar e homogeneizar todos os reagentes.
- Identificar os tubos ou placas.
- Na sala limpa para preparo de mix, preparar o volume necessário a todas as reações em um único microtubo para posteriormente dividir os volumes por reações individualmente. Seguir as instruções descritas nas Quadros 2, 3 ou 4 contendo as informações de cada reação.
- Na sala específica para aplicação de DNA, aplicar a amostra ao mix de PCR conforme Quadro 2, 3 ou 4 e registrar os reagentes e equipamentos utilizados em planilha especifica.
- Adicionar a solução de ácidos nucleicos extraídos conforme volume indicado nas Quadros 2, 3 ou 4 na sala de aplicação de DNA.
- Selar as placas ou fechar os tubos. É recomendável realizar um spin no caso de uso de placas de qPCR.
- Dispor os tubos/placa no termociclador e programá-lo conforme dados da Quadro 5.
- Verificar a integridade e eficiência da extração do material genético, bem como a presença de inibidores por meio de PCR em tempo real para β-actina 58 ou outro gene constitutivo que o analista julgar pertinente.
Nota: Considerar o volume para pelo menos uma reação de branco de reação, em que conste apenas os reagentes do mix de PCR e água livre de nucleases como template da reação.
Quadro 2: Insumos e volumes utilizados na qPCR para diagnóstico de M. tuberculosis (IS1081)*
| Reagente | Concentração | Volume | Concentração Final |
| Água livre de nucleases | - | 4 | - |
| PCR MasterMix | 2x | 12,5 | 1x |
| Mbo.IS1081.124.F | 30 µM | 0,5 | 600 nM |
| Mbo.IS1081.124.R | 30 µM | 0,5 | 600 nM |
| Mbo.IS1081.124.S | 25 µM | 0,5 | 500 nM |
| MgCl2 | 25 mM | 4 | 4 mM |
| VOLUME DE MIXPOR TUBO (µL) | 22 | ||
| VOLUME DE DNA (µL) | 3 | ||
| VOLUME TOTAL(µL) | 25 |
*As condições da reação podem ser modificadas de acordo com o kit utilizado.
Quadro 3: Insumos e volumes utilizados na qPCR para diagnóstico de M. bovis (RD4)*
| Reagente | Concentração | Volume | Concentração Final |
| Água livre de nucleases | - | - | - |
| PCR MasterMix | 2x | 12,5 | 1x |
| Mbo.RD4.88.F | 60 µM | 0,25 | 600 nM |
| Mbo.RD4.88.R | 60 µM | 0,25 | 600 nM |
| Mbo.RD4.88.S | 40 µM | 0,25 | 400 nM |
| MgCl2 | 25 mM | 9 | 9 mM |
| VOLUME DE MIXPOR TUBO (µL) | 22 | ||
| VOLUME DE DNA (µL) | 3 | ||
| VOLUME TOTAL(µL) | 25 |
*As condições da reação podem ser modificadas de acordo com o kit utilizado.
Quadro 4: Insumos e volumes utilizados na qPCR para β-actina 58*
| Reagente | Concentração | Volume | Concentração Final |
| Água livre de nucleases | - | 1,8 | - |
| PCR Master Mix | 2x | 5 | 1x |
| Β-actina.58-F | 10 µM | 0,375 | 375 nM |
| Β-actina.58-R | 10 µM | 0,375 | 375 nM |
| Β-actina.58-S | 10 µM | 0,25 | 250 nM |
| MgCl2 | 25 mM | 1,2 | 3 mM |
| VOLUME DE MIXPOR TUBO (µL) | 9 | ||
| VOLUME DE DNA (µL) | 1 | ||
| VOLUME TOTAL(µL) | 10 |
*As condições da reação podem ser modificadas de acordo com o kit utilizado.
Quadro 5: Programa de ciclagem para detecção do M. bovis, M. tuberculosis e β-actina 58
| Temperatura (ºC) | Tempo | Fluorescência | N° de ciclos |
| * | * | Off | 1 |
| * | Off | ||
| 95 | 15´´ | Off |
50
|
| 60 | 60´´ | On |
*Parâmetros definidos conformeo protocolo do kit de qPCR.
O relatório da corrida deveráser gravado como arquivo eletrônico para fins de rastreabilidade.
Critérios de aceitação do Ensaio
- As amostras com valor de Cycle Threshold (Ct) menor ou igual a 40 para a reação IS1081 serão consideradas positivas, não sendo necessária a realização dos testes para o gene RD4 e para o gene constitutivo β-actina. O laudo analítico corresponderá à detecção ou ausência de detecção do genoma.
- As amostras com Ct acima de 40 ou ausência de amplificação para o gene IS1081 deverão ser submetidas aos testes para o gene RD4 e para o gene constitutivo β-actina.
- As amostras que não apresentarem amplificação para o gene constitutivo β-actina, deverão ser submetidas a nova extração e posterior repetição das qPCRs.
- O ponto de corte para considerar uma amostra positiva para M. bovis ou para micobactérias do complexo M. tuberculosis é igual a Ct 40,0. Amostras que amplificarem acima deste Ct serão consideradas negativas.
- Os resultados da reação só serão considerados válidos se houver amplificação com Ct menor ou igual a 35 na cepa de referência positiva, e não houver amplificação no branco de reagentes e no controle de extração (caso houver). Além disso, a curva de amplificação deve ter formato sigmoide característico para a técnica.
¶ C - PCR convencional - PCR
¶ Materiais
- Microtubos em tiras (strips) ou unitários 0,2 mL ou microplacas de PCR (para amplificação em termociclador).
- Microtubos de 0,5mL e 1,5mL (para preparo do mix de reação).
- Selante adesivo para placas.
- Caneta de marcador permanente.
- Descartador.
- Luvas descartáveis para procedimento.
- Ponteiras com filtro.
- Estantes para microtubos.
¶ Equipamentos e instrumentos
- Micropipetas cujos volumes sejam adequados ao protocolo de extração utilizado, e à quantidade total de mix de PCR a ser preparado.
- Equipamento de extração específico de acordo com a metodologia adotada.
- Termociclador para PCR convencional.
- Cabine de segurança biológica com filtro HEPA classe II (requisito mínimo) ou estação de trabalho para PCR (Workstation PCR) com luz UV germicida.
- Cuba e fonte para eletroforese em gel de agarose.
- Transiluminador.
- Agitador de tubos.
- Centrífuga para microtubos e microplacas.
Nota: Alternativamente à eletroforese em gel de agarose, pode-se utilizar equipamento de eletroforese capilar e seus respectivos kits de análise.
¶ Insumos
- Água livre de nucleases;
- Tampão TE pH 8,0;
- Master Mix 5x;
- MgCl2 25mM;
- Enzima Taq DNA polimerase
- Kit de extração de DNA;
- Agarose em pó;
- Oligonucleotídeos (Quadro 1).
Quadro 1: Oligonucleotídeos utilizados para PCRs
| Oligonucleotídeo | Tipo de PCR | Sequência | Referência |
|
TB11 TB12 |
PCR |
ACCAACGATGGTGTGTCCAT CTTGTCGAACCGCATACCCT |
Sales et al., 2014b |
|
Mb400F Mb400R |
PCR |
AACGCGACGACCTCATATTC AAGGCGAACAGATTCAGCAT |
Sales et al., 2014b |
|
Mtub-gyrB.F Mtub-gyrB.R |
PCR |
TCGGACGCGTATGCGATATC ACATACAGTTCGGACTTGCG |
Kasai et al., 2000 |
¶ Padrões (controles positivos)
- Padrões para as PCRs Mb400 e TB11/TB12: o padrão positivo deve corresponder ao DNA extraído das amostras de referência M. bovis AN5, e M. bovis BCG ou equivalentes disponíveis no laboratório.
- O padrão para PCR Mtub-gyrB deve corresponder ao DNA extraído de uma amostra de campo ou o controle sintético específico.
¶ Soluções
- Solução de Álcool 70%.
- Solução descontaminante de moléculas residuais de RNAs / DNAs / amplicons /resíduos de proteínas de superfícies, entre as quais DNAses/RNAses.
¶ Realização do ensaio
¶ Processamento de amostras destinadas a PCR direto de tecido animal
Caso a amostra seja destinada a realização de PCR direto a partir de amostra de tecido animal deve-se separar um fragmento de tecido, de aproximadamente 0,5 a 1,0 gramas, preferencialmente com lesão sugestiva de tuberculose, e acondicionar em criotubo contendo 500 microlitros de solução constituída por 450 µl de TE 1X e 50 µl de SDS a 10%.
A inativação e a extração da amostra serão realizadas simultaneamente através da adição de 50 µl de proteinase K e subsequente incubação em banho Maria a 56,5 ºC + 3,5 ºC (são aceitáveis valores entre 20 ºC e 60 ºC, conforme orientação dos manuais dos fabricantes da enzima) por processo overnight.
Em caso de estoque das amostras de tecido para PCR no DDB, realizar o procedimento até a etapa de acréscimo da solução de TE 1X/SDS 10% e congelá-las a uma temperatura menor que -20 °C.
¶ Extração do DNA
A extração de DNA poderá ser realizada através de método automatizado, como por exemplo extração automatizada por beads magnéticas, ou por processo manual como por exemplo extração por colunas de sílica. Os métodos manuais utilizando kits de colunas de sílica são alternativas para o processamento de poucas amostras ou em caso de impossibilidade do uso dos equipamentos automáticos. Os procedimentos analíticos de extração de DNA deverão ser registrados em planilha específica.
Nota: Extrair juntamente com as amostras, um Controle de Extração (CE), correspondendo apenas aos reagentes empregados na metodologia. Este controle é dispensável nos métodos automatizados, como por exemplo, extração por beads magnéticas, cuja manipulação da amostra e processos manuais são mínimos. Já para extração de DNA por coluna, cujo método implica em diversas etapas de transferência da amostra, o Controle de Extração é obrigatório.
¶ Diluição dos primers
- Ressuspender os oligonucleotídeos (iniciadores e sondas liofilizados) em tampão TE pH=8, de modo que a solução estoque seja de 500pmol/µL. É recomendável utilizar centrífuga de tubos para dar um spin no tubo liofilizado antes de abri-lo.
- Recomenda-se que as soluções de trabalho para os iniciadores tenham concentração de 10 pmol/µL.
Nota: Outras diluições podem ser calculadas de acordo com os volumes necessários para o teste, desde que atendam a concentração final prescrita para o protocolo.
¶ Preparo do Mix de Reação
- Os procedimentos de registro do preparo do mix deverão ser registrados em planilha específica.
- Descongelar e homogeneizar todos os reagentes.
- Identificar os tubos ou placas.
- Preparar o volume necessário para todas as reações em um único tubo para posteriormente dividir os volumes por reação individualmente. Seguir as instruções descritas nas Quadros 2, 3 e 4 e registrar todos os reagentes
- Adicionar a solução de ácidos nucleicos extraídos conforme volume indicado na Quadro 5, 6 e 7 em local determinado no laboratório diferente daquele em que o mix de PCR foi preparado (Sala de aplicação de DNA).
- Selar as placas ou fechar os tubos. É recomendável realizar um spin no caso de uso de placas de PCR.
- Programar o termociclador conforme dados da Quadro 5, 6 e 7.
Nota: Considerar o volume para pelo menos uma reação de branco de reação, em que conste apenas os reagentes do mix de PCR e água livre de nucleases como template da reação.
Quadro 2: Concentrações dos reagentes para a PCR TB11/TB12
| Reagente | Concentração | Volume | Concentração Final |
| Água livre de nucleases | _ | 8,1 | - |
| Master Mix 5x | 5 x | 4 | 1x |
| dNTP | 10 mM | 0,4 | 200 µM |
| MgCl2 | 25 mM | 1,2 | 1,5 mM |
| TB11 | 10 µM | 2 | 0,4 µM |
| TB12 | 10 µM | 2 | 0,4 µM |
| Enzima Taq DNA polimerase | 5 U/µL | 0,3 | 1x |
| VOLUME DE MIX POR TUBO (µL) | 18 | 1x | |
| VOLUME DE DNA (µL) | 2 | ||
| VOLUME TOTAL (µL) | 20 |
*As condições da reação podem ser modificadas conforme o kit de PCR utilizado.
Quadro 3: Concentrações dos reagentes para a PCR Mb400
| Reagente | Concentração | Volume | Concentração Final |
| Água livre de nucleases | _ | 8,1 | - |
| Master Mix 5x | 5 x | 4 | 1x |
| dNTP | 10 mM | 0,4 | 200 µM |
| MgCl2 | 25 mM | 1,2 | 1,5 mM |
| Mb400F | 10 µM | 2 | 0,4 µM |
| Mb400R | 10 µM | 2 | 0,4 µM |
| Enzima Taq DNA polimerase | 5 U/µL | 0,3 | 1x |
| VOLUME DE MIX POR TUBO (µL) | 18 | 1x | |
| VOLUME DE DNA (µL) | 2 | ||
| VOLUME TOTAL (µL) | 20 |
*As condições da reação podem ser modificadas conforme o kit de PCR utilizado.
Quadro 4: Concentrações dos reagentes para a PCR Mtub-gyrB
| Reagente | Concentração | Volume | Concentração Final |
| Água livre de nucleases | _ | 8,1 | - |
| Master Mix 5x | 5 x | 4 | 1x |
| dNTP | 10 mM | 0,6 | 200 µM |
| MgCl2 | 25 mM | 2 | 1,5 mM |
| Mb400F | 10 µM | 1,5 | 0,4 µM |
| Mb400R | 10 µM | 1,5 | 0,4 µM |
| Enzima Taq DNA polimerase | 5 U/µL | 0,3 | 1x |
| VOLUME DE MIX POR TUBO (µL) | 18 | 1x | |
| VOLUME DE DNA (µL) | 2 | ||
| VOLUME TOTAL (µL) | 20 |
*As condições da reação podem ser modificadas conforme o kit de PCR utilizado.
Quadro 5: Programação para a PCR TB11/TB12
| Fase | Temperatura | Tempo | N° de Ciclos |
| Pré-incubação | * | 1 | |
| Ativação | ** | ** | 1 |
| Amplificação | 94 ºC | 45” | 35 |
| 56 ºC | 45” | ||
| 72 ºC | 45” | ||
| Extensão | 72 ºC | 10' | 1 |
* Verificar se o kit possui fase de pré-amplificação.
** Cabe ao analista verificar o tempo de ativação da enzima conforme a bula do kit.
Quadro 6: Programação para a PCR Mb400
| Fase | Temperatura | Tempo | N° de Ciclos |
| Pré-incubação | * | 1 | |
| Ativação | ** | ** | 1 |
| Amplificação | 94 ºC | 30” | 35 |
| 56 ºC | 30” | ||
| 72 ºC | 30” | ||
| Extensão | 72 ºC | 10' | 1 |
* Verificar se o kit possui fase de pré-amplificação.
** Cabe ao analista verificar o tempo de ativação da enzima conforme a bula do kit.
Quadro 11: Programação para a PCR Mtub-gyrB
| Fase | Temperatura | Tempo | N° de Ciclos |
| Pré-incubação | * | 1 | |
| Ativação | ** | ** | 1 |
| Amplificação | 94 ºC | 1’ | 45 |
| 55 ºC | 1’ | ||
| 72 ºC | 1’20” | ||
| Extensão | 72 ºC | 10' | 1 |
* Verificarse o kit possui fase de pré-amplificação.
** Cabe ao analistaverificar o tempo de ativaçãoda enzima conformea bula do kit.
O resultado do ciclo de amplificação poderá ser avaliado através de eletroforese em gel de agarose ou de equipamento de eletroforese capilar.
¶ Critérios de aceitação do Ensaio
- Os controles positivos devem apresentar bandas amplificadas de acordo com o padrão esperado, sendo o tamanho em pares de base girando em torno de 139 pb para a reação TB11/TB12, 400 pb para a reação Mb400; 1020 pb para a reação Mtub-gyrB.
- Os controles negativos não devem apresentar bandas em padrão semelhante ao dos controles positivos.
- Amostras com padrão de eletroforese semelhantes ao do controle positivo serão consideradas positivas, podendo ser submetidas a sequenciamento genético para confirmação a critério do analista.
¶ Interpretação dos resultados
- Os controles positivos devem apresentar bandas amplificadas de acordo com o padrão esperado, sendo o tamanho em pares de base girando em torno de: 400pb para a reação Mb400; 439 pb para a reação TB11/TB12; 1020 pb para a reação Mtub-gyrB.
- Os controles negativos não devem apresentar bandas em padrão semelhante ao dos controles positivos.
- Amostras com padrão de eletroforese semelhantes ao do controle positivo serão consideradas positivas, podendo ser submetidas ao sequenciamento para confirmação de acordo com critério do analista.
¶ Emissão dos resultados
I – Os resultados deverão ser emitidos em documento denominado “Relatório de Ensaio”.
¶ Descarte de amostras e resíduos
I –Anteriormente ao descarte de amostras e produtos de ensaio, deverão ser observados os prazos mínimos de retenção de itens de ensaio.
II – Anteriormente ao descarte de amostras e produtos de ensaio, deve ser realizado registro de descarte em formulário próprio e conferência.
III – Os materiais descartados devem ser separados adequadamente entre resíduos químicos e biológicos;
IV –O laboratório deve assegurar a biossegurança dos resíduos gerados, e seguir as legislações ambientais vigentes durante todo o processo do descarte.
¶ Retenção de itens de ensaio
I – Os isolados para análise de PCR devem ser armazenados por período mínimo de 12 meses a partir da realização das análises, em freezer a -20 ºC.
II – As amostras negativas devem ser armazenadas por período mínimo de 90 dias a partir da realização das análises, em freezer a -20 ºC.
¶ 5. Base Legal e Documentos de Referência
BRASIL. Ministério da Agricultura e Pecuária. Portaria SDA/MAPA nº 1110, de 13 de maio de 2024. Institui diretrizes para publicação e manutenção de manuais técnicos no âmbito da SDA.
BRASIL. Ministério da Saúde. Centro de Referência Professor Hélio Fraga. Manual de Bacteriologia da Tuberculose. 3 ed. Rio de Janeiro: Fundação Nacional de Saúde, 2005. 239p.
Bielanski A, AlgireJ, Lalonde A, Nadin-Davis S. Transmission of bovine viraldiarrhea vírus (BVDV) via in vitro-fertilized embryos to recipientes, but not to their offspring. Theriogenology. 2009 Feb; 71(3):499-508.
C.J.C. Philips et al. The transmission of Mycobacterim bovis infection to cattle. Research in Veterinary Science 74 (2003) 1-15.
GRANGE, J.M.; YATES, M. D. KANTOR, I. N. Guidelines for speciation within the Mycobacterium tuberculosis complex. 2 ed. WHO/EMC/ZOO 96.4. 1996.
H. Kasai, T. Ezaki, S. Harayama. Differentiation of Phylogenetically Related Slowly Growing Mycobacteria by Their gyrB Sequences. Journal of Clinical Microbiology, Jan. 2000, p. 301–308.
HOLTON, J.; SHETTY, N.; V.MC DONALD. Efficacy of ‘Nu-Cidex’ (0,35% acid peracetic) against mycobacteria and cryptosporidia. Journal of Hospital Infection, 31, p. 235-244, 1995. ISSA, M.A. et al. Comparative Study of Mycobacterium bovis primary isolation methods. Brazilian Journal of Microbiology, v. 48, n.1, p. 139-144, 2017.
KENT, P.T.; KUBICA, G.P. Public Health Mycobacteriology: a guide for the level III laboratory. Atlanta: Centers for Disease Control. 1985. 207p.
Manual of Standards for Diagnostic Tests and Vaccines. Paris: Office International des Epizooties/World Organization for Animal Health. França. 2009, Cap.: 2.4.7: Bovine Tuberculosis, p. 1-16. http://www.oie.int/eng/normes/mmanual/2008/pdf/2.04.07_BOVINE_TB.pdf Acesso em 01/04/2010.
M.L. Sales (a), A.A. Fonseca Jr.1, L. Orzil1 Validation of two real-time PCRs targeting the PE-PGRS 20 gene and the region of difference 4 for the characterization of Mycobacterium bovis isolates. Genetics and Molecular Research 13 (2): 4607-4616 (2014).
M.L. Sales (b), A.A. Fonseca Jr., E.B. Sales, A.C.P. Cottorello, et al. Evaluation of molecular markers for the diagnosis of Mycobacterium bovis. Folia Microbiol 59 (3): May, 2014.
MOTA, P.M.P.C. Estudo da Esofagostomose como Fator Predisponente de Reações Alérgicas Inespecíficas da Tuberculose Bovina. Tese de Mestrado. Escola de Medicina Veterinária,.UFMG, Belo Horizonte, 1985.
Moura, A., Hodon M.A., Soares Filho, P.M., Comparison of nine DNA extraction methods for the diagnosis of bovine tuberculosis by real time PCR. Ciência Rural, Santa Maria, v.46, n.7, p.1223- 1228, jul, 2016.
Public Health Agency of Canada. Mycobacterium tuberculosis, Mycobacterium bovis – Material Safety Data Sheets (MSDS). Infectious Substances. Section I. Infectious Agent. http://www.phac-aspc.gc.ca/msds-ftss/msds103e-eng.php Acesso em 11/01/2011.
Soares Filho PM, Ramalho AK, de Moura Silva, Hodon MA, de Azevedo Issa M, Fonseca Júnior AA, Mota PMPC, Silva CHO, dos Reis JKP, Leite RC. Evaluation of post-mortem diagnostic tests sensitivity and specificity for bovine tuberculosis using Bayesian latent class analysis. Res Vet Sci. 2019 Aug;125: 14-23.
¶ 6. Disposições Gerais
As sugestões para aprimoramento ou possíveis correções deste documento devem ser direcionadas ao Departamento responsável, para alinhamento das melhores práticas de mercado, legislação vigente e/ou regulamentações, que não tenham sido contempladas na versão vigente.
¶ 7. Histórico de revisões
| Versão | Conteúdo alterado | Data | Motivo |
|---|---|---|---|
| 1 | - | Elaboração do documento | |
| 2 | Itens A, B | 31.03.2026 | Formatação, inclusão de item C para separação dos métodos - PCR em tempo real (B) e PCR convencional (C) |