¶ Folha de rosto
© 2022 Ministério da Agricultura, Pecuária e Abastecimento. Todos os direitos reservados. É permitida a reprodução parcial ou total desta obra, desde que citada a fonte e que não seja para venda ou qualquer fim comercial. A responsabilidade pelos direitos autorais de textos e imagens desta obra é do autor.
Elaboração, distribuição, informações:
Ministério da Agricultura, Pecuária e Abastecimento
Secretaria de Defesa Agropecuária - SDA
Departamento de Saúde Animal – DSA
Coordenação de Animais Terrestres - CAT
Esplanada dos Ministérios, Bloco D, Anexo A, 4º andar, sala 318
CEP: 70043-900, Brasília - DF
Tel: (61) 3218-2855
https://www.gov.br/agricultura/pt-br
E-mail: dsa.gab@agro.gov.br
Central de Relacionamento: 0800 704 1995
Equipe Técnica: Luciana Guirelli Ábrego, Heber Luiz Pereira, Aroni Sattler, Vagner de Alencar Arnaut de Toledo, Décio Luiz Gazzoni, Pedro da Rosa Santos, Rejane Stubs Parpinelli e Annelisede Souza Rosa Fontana.
Colaborador: Roberto Carvalho.
¶ Folha resumo
|
Macroprocesso: 22 - Prevenção, controle e erradicação de doenças e pragas |
Objetivo: O Manual de Doenças das Abelhas foi elaborado por meio do Projeto de Cooperação Técnica Internacional para o Fortalecimento do Sistema Brasileiro de Defesa Agropecuária – PCT/BRA/IICA 13/004 com o objetivo de reunir informações relevantes para o Serviço Veterinário Oficial brasileiro. Trazendo um apanhado de informações sobre a cadeia produtiva, biologia, fisiologia, organização social das abelhas, materiais e equipamentos, são tratados ainda temas ligados diretamente à saúde das abelhas, como boas práticas visando o controle de doenças, intoxicações, principais doenças que acometem a cadeia produtiva e seu diagnóstico diferencial. |
|||
|
Processo: 22.04 - Regulamentar as ações de saúde animal e sanidade vegetal |
||||
|
Entrega: Sanidade dos animais e das plantas |
Público alvo e demais interessados:
|
Versão do documento: 1.0 |
||
|
Setor responsável e responsabilidades A gestão desse manual está sob a responsabilidade do Departamento de Saúde Animal (DSA) que prestará auxílio ao público alvo leitor dúvidas e/ou sugestões quanto à aplicação deste manual devem ser submetidas ao Departamento responsável. |
||||
¶ Definições e conceitos
- Cibário: Relativo ou pertencente às partes bucais de um inseto.
- Colmeia: Estrutura onde se alojam abelhas, podem ser rústicas ou racionais, construídas para o manejo de colônias.
- Colônia: Unidade animal quando se trata de abelhas, composta por abelhas adultas, crias e alimento em estruturas próprias.
- Elipsoides: Próprio de ou que tem a forma de elipse; elipsoide.
- Enxame: Conjunto de abelhas adultas, rainha e operárias, casualmente zangões/machos.
- Gáleas: Nos insetos, lobo externo das maxilas limitado pelos estipes.
- Glossa: Nos insetos, projeção em forma de língua na porção mediana dos lábios.
- Heterotálico: Diz-se dos fungos em que as estruturas sexuais masculinas e femininas não estão no mesmo indivíduo, são autoestéreis.
- Lacínias: Uma das peças, achatada, que compõem as maxilas dos insetos.
- Micélio: Talo de fungos, composto de filamentos (hifas) que constituem sua parte vegetativa e são destituídos de clorofila.
- Opercular: De opérculo, estrutura que serve de tampa ou cobertura a uma cavidade ou orifício.
- Óstio: Abertura que dá acesso a órgão tubular, ou que se encontra entre duas cavidades corporais distintas; ostium.
- Palpos labiais: Apêndice segmentado das maxilas ou do lábio dos insetos.
- Paraglossa: Nos insetos, cada um dos dois lobos no ápice dos lábios, lateralmente às glossas.
- Protrátil: Que se pode alongar para a frente; protráctil, protraível.
- Provisões: Conjunto de artigos de consumo e reserva de alimentos; provimento, víveres.
- Região Pantropical: Que ocorre em qualquer região dos trópicos (diz-se de organismo).
- Sanidade: Conjunto de condições que conduzem ao bem-estar e à saúde.
- Saúde: Estado de equilíbrio dinâmico entre o organismo e seu ambiente, o qual mantém as características estruturais e funcionais do organismo dentro dos limites normais para sua forma de vida e para a sua fase do ciclo vital.
- Tergitos: Cada um dos escleritos do tergo no corpo dos artrópodes.
- Voltinismo: Mesmo que voltismo, termo usado nas ciências biológicas para indicar a frequência das reproduções anuais de um organismo.
¶ Responsabilidades
O presente manual possui vigência e prazo indeterminado e será revisado sempre que necessário pela Coordenação de Animais Terrestres (CAT) do Departamento de Saúde Animal (DSA) e aprovada pela Secretaria de Defesa Agropecuária (SDA).
A gestão desse manual está sob a responsabilidade do Departamento de Saúde Animal (DSA) que prestará auxílio ao público alvo leitor dúvidas e/ou sugestões quanto à aplicação deste manual devem ser submetidas ao Departamento responsável.
A publicação e atualização das versões na plataforma oficial da SDA para acesso pelo público alvo será de responsabilidade da Secretaria representada pelo Departamento de Saúde Animal (DSA).
¶ Objetivo
O Manual de Doenças das Abelhas foi elaborado por meio do Projeto de Cooperação Técnica Internacional para o Fortalecimento do Sistema Brasileiro de Defesa Agropecuária – PCT/BRA/IICA 13/004 com o objetivo de reunir informações relevantes para o Serviço Veterinário Oficial brasileiro. Trazendo um apanhado de informações sobre a cadeia produtiva, biologia, fisiologia, organização social das abelhas, materiais e equipamentos, são tratados ainda temas ligados diretamente à saúde das abelhas, como boas práticas visando o controle de doenças, intoxicações, principais doenças que acometem a cadeia produtiva e seu diagnóstico diferencial.
¶ Procedimentos
¶ 1. INTRODUÇÃO
O valor das abelhas e demais polinizadores para a manutenção da biodiversidade é imensurável. As abelhas são consideradas responsáveis, de forma direta ou indireta pela polinização de aproximadamente 70% das espécies cultivadas para produção de alimentos no mundo. O serviço ecossistêmico de polinização realizado pelas abelhas gera recursos e promove o aumento na produção e na qualidade de diversos produtos agrícolas (FAO, 2016; USDA, 2017, CGEE, 2017).
As culturas agrícolas podem ser totalmente dependentes, depender em certo grau e outras podem se beneficiar do serviço de polinização realizado pelas abelhas. Embora algumas espécies vegetais não necessitem de agentes polinizadores para produzir frutos e sementes, a presença de apiários e meliponários no entorno da plantação contribui no processo de polinização das culturas que dela se beneficiam, resultando em aumento de produtividade agrícola.
Com a crescente demanda por alimentos no mundo, e sendo o Brasil um dos protagonistas desse cenário, torna-se prioridade a busca por maior produção, especialmente aumentando a produtividade por área. A presença de abelhas no cenário agrícola está associada a uma produção mais responsável e seu valor na agricultura foi estimado por pesquisadores em cerca de R$ 43 bilhões, considerando apenas as culturas que se tem informações de área plantada e grau de dependência por polinização conhecido (WOLOWSKI et al., 2019). O incremento de produtividade associado às abelhas é de extrema relevância para o desenvolvimento do a gronegócio nacional, que tem previsão de crescimento significativo nos próximos 10 anos (USDA, 2020).
Considerando o exposto, a saúde das abelhas é fundamental tanto para a produção de mel e demais produtos das abelhas como para a segurança alimentar. A compreensão, supervisão e difusão do conhecimento sobre o manejo adequado das colônias de modo a evitar pragas, doenças e contaminantes, deve fazer parte das políticas públicas para desenvolvimento do setor agropecuário.
Apesar de não estarem sob o escopo do Programa Nacional de Saúde das Abelhas – PNSAb, as crescentes ocorrências de mortalidade de abelhas por suspeita de intoxicação vêm causando preocupação. As intoxicações de abelhas são agravos não infecciosos e por esse motivo não fazem parte da vigilância sanitária animal preconizada para as doenças de abelhas de interesse do programa sanitário. Os sintomas mais comuns das intoxicações observados a campo serão evidenciados por esse manual, para que o Serviço Veterinário Oficial possa considerá-los em suas ações sanitárias para a elaboração de diagnóstico diferencial, quando couber.
Ressaltamos que os Órgãos Executores de Sanidade Agropecuária - OESAs possuem a autonomia necessária para realizar investigações de casos de mortalidade de abelhas onde a única suspeita clínica seja a intoxicação. Em alguns Estados, esse trabalho tem sido realizado em parcerias com órgãos como o Ministério Público, Universidades, entre outros. Maiores informações sobre forma de registrar essas investigações a campo, estão disponíveis no manual do e-SISBRAVET, disponível no sítio eletrônico do Ministério da Agricultura, Pecuária e Abastecimento – MAPA.
Em 2008, foi criado pelo Ministério da Agricultura, Pecuária e Abastecimento o Programa Nacional de Sanidade Apícola (PNSAp). Diante do crescimento exponencial que a meliponicultura vem apresentando no território nacional, o programa sanitário foi revisado e passou a ser denominado Programa Nacional de Saúde das Abelhas - PNSAb, expandindo assim suas ações estratégicas também para as abelhas nativas sem ferrão. O objetivo do programa consiste em fortalecer a cadeia produtiva das abelhas, através de ações de vigilância e defesa sanitária animal, de modo a prevenir, controlar ou erradicar doenças que acometem as abelhas, fomentando a importância da saúde para garantir o sucesso da cadeia produtiva da Apicultura e da Meliponicultura no Brasil (MAPA, 2008).

Figura 1.1. Abelha A. mellifera em polinização dirigida na cultura do melão no estado da Bahia (acima à esquerda); abelha mandaçaia (Melipona quadrifasciata) em planta ornamental (acima à direita); Operária coletando pólen em inflorescência de gramínea, pesquisadores da África encontraram maior rendimento reprodutivo de Braquiária com a presença de abelhas (abaixo à esquerda – Adamou e Tchuenguem Fohouo (2014)); Operária de abelha nativa em polinização dirigida na cultura do morango em Minas Gerais (abaixo à direita). (Fotos: Heber Luiz Pereira).
¶ 1.1 Meliponicultura
As abelhas (Anthophila) compõem um grande grupo, com mais de 20.000 espécies descritas no mundo e ocupam diversos ecossistemas (ITIS, 2018). O Brasil se destaca com pouco mais de 1.900 espécies já catalogadas até 2020 (DISCOVERY LIFE, 2020).
As abelhas nativas sem ferrão são sociais e representam aproximadamente 600 espécies, sendo 330 espécies conhecidas no Brasil, catalogadas em 33 gêneros (CORTOPASSI-LAURINO e NOGUEIRA NETO, 2016; CAMARGO e PEDRO, 2013). Apresentam variações como a entrada de seus ninhos, número de indivíduos no ninho, bem como o hábito de nidificação, com formas e cores diferenciadas, sendo que algumas espécies se adaptam facilmente ao manejo. Com a grande diversidade presente no país, os nomes populares das abelhas nativas sem ferrão muitas vezes se confundem nas diferentes regiões do Brasil, sendo necessário utilizar nomes científicos para identificá-las de maneira correta (NOGUEIRA-NETO, 1997; SANTOS, 2010).
Diferentemente das abelhas de hábitos solitários, as abelhas sociais apresentam diferentes níveis de organização. Vivem em colônias populosas, com centenas a milhares de abelhas fêmeas operárias e, geralmente, apenas uma rainha, e os indivíduos machos, os zangões, podem ou não estar presentes nas colônias (VIT, PEDRO e ROUBIK, 2013).
A criação de abelhas nativas sem ferrão é uma atividade desenvolvida há séculos, com relatos desde os primórdios das antigas civilizações do Egito Antigo. Ao decorrer da história da evolução da humanidade, em todo o continente americano antes da introdução da abelha europeia (Apis mellifera), o mel se destacou como produto de uso medicinal na cultura indígena, se tornando o produto mais valorizado das abelhas indígenas (ou nativas), sendo uma das primeiras fontes de açúcar para o ser humano, e hoje vem ganhando destaque na produção em várias regiões do país (BALLIVIÁN, 2008; SILVA e PAZ, 2012).
As abelhas que existiam no Brasil até o ano de 1839 eram chamadas abelhas nativas, abelhas indígenas, ou meliponíneos, o motivo pelo qual muitas das denominações científicas desse grupo de abelhas sejam denominadas de origem linguística indígena tupi, e a diversidade dessas espécies de abelhas é consideravelmente elevada. Inicialmente desenvolvida pelos índios, a criação de abelhas sem ferrão estendeu-se aos pequenos produtores e de uma maneira rústica e tradicional, sendo considerada uma atividade de renda econômica complementar (NOGUEIRA-NETO,1997; COLETTO-SILVA, 2005; SILVA e PAZ, 2012). A criação racional de abelhas sem ferrão é definida como meliponicultura, termo utilizado pela primeira vez por Nogueira-Neto em 1953, e é praticada há séculos por populações tradicionais e vem ganhando adeptos nos últimos anos (NOGUEIRA-NETO, 1953; BARBIÉRI e FRANCOY, 2020).
Os meliponíneos se encontram em toda região pantropical do planeta e, ocupam também algumas regiões de clima temperado subtropical. Assim, essas abelhas são encontradas na maior parte da América Neotropical, não ocorrendo em regiões de clima temperado (NOGUEIRA- NETO, 1997; PEREIRA et al., 2011; VILLAS-BÔAS, 2012; CAMARGO, 2013).
.jpg)
Nos últimos 10 anos a meliponicultura teve uma grande expansão, devido aos novos modelos de colmeias, popularização do uso de iscas e facilidade de comercialização via redes sociais, mesmo que irregular e com possíveis riscos sanitários (OLIVEIRA et al., 2012). No entanto, existem entraves como a falta de conhecimento por parte dos meliponicultores e pelos responsáveis pelo cadastramento (OESAs e Órgão ambiental) que dificultam a legalização dos meliponários. Mesmo com essa problemática é observado uma crescente utilização destas abelhas em cultivos, voltada para a polinização dirigida.

Figura 1.3. Diversidade entre diferentes espécies de abelhas nativas sem ferrão: 1- Abelhas jataí (Tetragonisca angustula); 2 - Abelhas uruçu boca-de-renda (Melipona seminigra); 3 - Abelhas iraí (Nannotrigona testaceicornis); 4 - Abelhas lambe-olhos (Leurotrigona muelleri); 5 - Abelha uruçu amarela (Melipona flavolineata). (Fotos: Cristiano Menezes)
¶ 1.2 Apicultura no Brasil
Com o processo da expansão territorial europeia e a colonização das novas terras, as abelhas que antigamente ocupavam apenas o Velho Mundo (o mundo conhecido pelos europeus até o século XV) foram introduzidas em locais onde não se tinham registros de sua existência. As primeiras colônias de Apis mellifera encontradas nas Américas datam do século XVII, no ano de 1621 (CRANE, 1990).
No período imperial de 1839, por meio de autorização do rei Dom Pedro II foram introduzidas no Brasil as primeiras abelhas europeias da subespécie Apis mellifera mellifera proveniente da cidade do Porto em Portugal, dando início à produção de mel no Brasil (NOGUEIRA-NETO, 1997; WIESE, 2005; PEREIRA et al., 2014). Antes desse processo de introdução das abelhas europeias, no Brasil se conheciam apenas as abelhas nativas sem ferrão, ou também conhecidas como abelhas indígenas, a exemplo: mandaçaia (Melipona quadrisfasciata Lepeletier), tiúba (Melipona compressipes), jataí (Tetragonisca angustula L.), uruçu (Melipona scutellaris L.), dentre outras (NOGUEIRA-NETO, 1997; KERR, 1980; WOLFF, 2008).
No ano de 1845, imigrantes alemães trouxeram consigo algumas raças de A. mellifera mellifera provenientes da Alemanha, introduzindo-as no sul do Brasil (Rio Grande do Sul, Santa Catarina e Paraná), dando início à apicultura racional brasileira. Entre os anos de 1870 e 1880, Hannemann e Schenck, Hanewn e Brunnet trouxeram da Alemanha as primeiras A. mellifera ligustica para o Sul do Brasil, também conhecidas como abelhas amarelas italianas (Figuras 1.4 e 1.5). Estas abelhas foram introduzidas no Brasil, para ser utilizada a cera branca na confecção de velas para fins religiosos, visto que a cera produzida pelas abelhas nativas sem ferrão, era de pequena quantidade e possui cor marrom, por ser uma mistura de cera e resina entre outros produtos, não sendo interessante sua utilização para aquela finalidade (NOGUEIRA-NETO, 1997; GONÇALVES, 2001; FRANCOY, 2007).
Com a chegada de mais imigrantes ao Brasil durante os anos seguintes, outras subespécies também foram trazidas pelos europeus, sendo introduzidas no Brasil a A. mellifera carnica e a A. mellifera caucasica, disseminando as abelhas por todo território brasileiro (GONÇALVES, 1994; WIESE, 2005). Sendo assim, destacam-se as quatro principais subespécies de abelhas europeias introduzidas em terras brasileiras no século XIX: a alemã Apis mellifera mellifera, a italiana Apis mellifera ligustica, a austríaca Apis mellifera carnica e a russa Apis mellifera caucasica (GONÇALVES, 1994; OLIVEIRA e CUNHA, 2005).
¶ 1.3 Processo de africanização apicultura brasileira


Até o ano de 1956, somente as subespécies europeias haviam sido introduzidas no Brasil pelos colonizadores na época do Brasil colonial. Em meados da década de 1950, a produção de mel sofreu uma queda devido ao surgimento de doenças e pragas que atacavam as colônias. A baixa produtividade das abelhas europeias no Brasil, com valores de 4 a 6 mil toneladas/ano no país, não era condizente com o tamanho e com as características tropicais propícias à exploração da apicultura (KERR, 1992; GONÇALVES, 2006; PEREIRA, 2011).
Preocupados com a baixa produção do mel brasileiro, o governo brasileiro tomou algumas medidas para reverter tal quadro. Oficialmente convidado pelo governo, o engenheiro agrônomo e geneticista especialista em abelhas, Prof. Dr. Warwick Estevam Kerr, professor da Escola Superior de Agricultura Luiz de Queiroz – ESALQ, de Piracicaba – SP, foi o escolhido para estudar o problema e apresentar ao governo brasileiro uma proposta que permitisse elevar a produtividade das colônias de abelhas (GONÇALVES, 2006; REIS e PINHEIRO, 2011).
O Dr. Warwick Estevam Kerr realizou um minucioso estudo na literatura apícola mundial da época, constatando que, no continente africano, havia uma abelha melífera muito mais produtiva que as europeias existentes aqui do Brasil, denominada A. mellifera scutellata. Em 1956, o próprio Prof. Kerr realizou uma viagem ao continente africano com o intuito de aprofundar o estudo das abelhas africanas, durante a qual entusiasmou-se com a capacidade produtiva das espécies de Apis locais (KERR, 1967). Kerr importou da África rainhas da subespécie Apis mellifera scutellata (anteriormente conhecidas como Apis mellifera adansoni, nome científico usado até meados do ano de 1975) para realizar estudos no Brasil (KERR, 1967; RUTTNER et al., 1978; GONÇALVES, 2006).
9
Devido a um erro de manejo e de forma acidental, a tela excluidora que estava na entrada das colmeias que continham rainhas importadas foi retirada, o que permitiu que as rainhas africanas puras enxameassem antes de ser realizado o programa de melhoramento genético planejado pelo Prof. Kerr nas proximidades da cidade de Rio Claro-SP (KERR, 1967; RINDERER et al., 1993).
Sendo assim, as rainhas novas puras africanas (A. m. scutellata) foram fecundadas por zangões de diversas subespécies europeias da região, iniciando uma rápida expansão por todo o Brasil, dando início ao chamado período de africanização. Esse consiste no processo de hibridização originando um descendente polihíbrido, posteriormente denominado de abelha africanizada. Desde o início, esses novos descendentes mantiveram sempre as características comportamentais e morfológicas das abelhas puras africanas e de maneira rápida e gradual ocorreu o processo de enxameação e africanização das abelhas A. mellifera. Este período foi considerado como um marco inicial de um novo momento na história da apicultura brasileira (KERR, 1967; DE JONG, 1996; GONÇALVES, 2006; PEREIRA, 2011; SOARES, 2012).
No Brasil, a abelha africanizada apresentou desempenho superior às abelhas europeias presentes no continente. As abelhas africanizadas se destacam por apresentarem elevada capacidade de defesa e adaptação a novos ambientes, capacidade reprodutiva muito mais eficiente com facilidade de enxamearem, rusticidade, maior tolerância a doenças, apresentando características únicas e próprias (DE JONG, 1996; GONÇALVES, 2006).
Por causa destas novas formas de adaptação e expansão, a abelha africanizada rapidamente se espalhou pelas Américas, colonizando inicialmente o Brasil, expandindo por quase toda a América do Sul, exceto as regiões abaixo do paralelo 33° na Argentina, em que o limite foi provavelmente imposto pelas baixas temperaturas de inverno encontradas nesta região (KERR, 1982; SHEPPARD et al., 1999; GONÇALVES, 2006).
10
Ao Oeste, a expansão foi limitada devido a presença da Cordilheira dos Andes, que impediu a passagem dos enxames em razão das baixas temperaturas. O Chile é o único país da América do Sul que não apresenta abelhas africanizadas em seu território até os dias de hoje (DEL LAMA et al., 2004, FRANCOY, 2007). A América Central foi ligeiramente colonizada, mesmo com tentativas frustradas de se criar barreiras que impedissem o avanço dos enxames na região do Panamá (BOREHAM e ROUBIK, 1987). Atualmente, ocupam grande parte ou totalidade dos Estados da Califórnia, Texas, Arizona, Novo México e Nevada, no Sul dos Estados Unidos (ALICE PINTO et al., 2007).
Durante muitos anos foram destacadas as características negativas destas abelhas, provocando o abandono ou redução drástica da atividade pelos apicultores, que não estavam preparados. A principal razão foi o elevado grau de defensividade das abelhas africanizadas, porém ressalte-se que muito pouco ou quase nada se sabia sobre seu comportamento, resultando na falta de técnicas de manejo adequados. Aliado a isto, foi criado um movimento negativista trazido pelos meios de comunicação em relação às conhecidas e apelidadas “abelhas assassinas”, que também contribuíram ainda mais para a decadência da apicultura no Brasil nesse período (SOARES, 2004; RANGEL, 2013).
Esta visão negativa diminuiu conforme se comprovou a produtividade dessas abelhas. O surgimento das abelhas africanizadas no Brasil e as suas consequências na vida dos apicultores, comerciantes, pesquisadores e na produção, causaram uma ampla modificação no cenário apícola brasileiro. Após essas mudanças a apicultura está em ampla expansão, tendo destaque como a atividade do agronegócio de maior desenvolvimento, permitindo que o Brasil seja conhecido como produtor e exportador dos produtos apícolas, sendo que algumas décadas depois o país passou a produzir em torno de 40 mil toneladas/ano (GONÇALVES et al., 2010; IBGE, 2018).
As abelhas africanizadas apresentam maior tolerância a pragas e doenças em relação às abelhas de origem europeias, não necessitando da utilização de produtos químicos para o controle sanitário (DELAPLANE e MAYER, 2005). A africanização contribuiu para a resistência a patógenos e maior eficiência no comportamento de remoção de ninhadas infestadas pelo ácaro Varroa destructor (GUERRA-JÚNIOR et al., 2000). A defensividade tem sido uma das características mais marcantes da abelha africanizada em relação a europeia (DE SOUZA et al., 2012).
11
¶ 1.4 Cadeia produtiva de apicultura e meliponicultura
Tanto a cadeia produtiva da apicultura quanto a da meliponicultura devem ser vistas como serviço ecossistêmico de polinização, pois o Brasil tem excelente potencial apícola (flora e clima), sendo considerada uma importante atividade que contribui para o desenvolvimento social e econômico (ASSAD et al., 2018). A cadeia produtiva da apicultura na atualidade, principalmente no que se refere a exploração do seu produto principal, o mel, assume crescente importância econômica e social em todo o país, contribuindo efetivamente com ocupação de mão de obra e geração de renda. A cadeia produtiva apícola no Brasil vem produzindo anualmente mais de 40 mil toneladas de mel, obtidas a partir de mais de 2 milhões de colônias espalhadas por todo o território nacional (IBGE, 2017; IBGE, 2018).
A cadeia é uma importante atividade econômica que gera emprego e renda, sendo o mercado do mel estimado em 500 milhões de reais e o valor agregado em polinização de culturas agrícolas superior a 65 bilhões de reais ao ano (ASSAD et al., 2018; GIANNINI et al., 2015). Ela engloba desde os suprimentos como equipamentos de campo e as colmeias; o setor produtivo com o apicultor e a casa do mel, o processamento, que é o entreposto, o setor comercial que engloba o distribuidor e a indústria, os mercados informal e de varejo, findando a cadeia produtiva com o consumidor final, gerando renda a todos os elos da cadeia e contribuindo para o desenvolvimento social e econômico, fornecendo um alimento de qualidade biológica, alto valor nutricional e que contribui para a segurança alimentar (LENGLER e RATHMANN, 2006; FERNANDES JÚNIOR e ARAÚJO SILVA, 2016; ASSAD et al., 2018).
Em ordem crescente, destacam-se como maiores produtores de mel do mundo em 2017, a China (551.476 ton/ano), Turquia (114.471 ton/ano) e Argentina (76.379 ton/ano). O Brasil encontra-se em 11° lugar (41.594 ton/ano) (FAO, 2019). O mercado apícola vem apresentando ótimas expectativas de expansão, considerando o aumento da procura no mercado nacional e as oportunidades de exportação, aliando-se a esses aspectos as parcerias que têm sido estabelecidas pelos apicultores (ASSAD et al., 2018).
Em relação aos produtos da meliponicultura, não existe legislação nacional que regulamente a produção, e sua comercialização é dificultada por não haver parâmetros de qualidade específicos a esta categoria (BARBIÉRI e FRANCOY, 2020). Atualmente não existe no país um mercado bem estabelecido de produtos, apenas iniciativas pontuais. As diversas técnicas utilizadas nessa criação resultam de iniciativas informais de pequenos meliponicultores e que difere nas mais diversas regiões do país (VILAS BOAS, 2012; KOSER et al., 2020).
Um dos maiores problemas na produção de mel de abelhas nativas é a falta do manejo e das boas práticas de manipulação durante o processo de beneficiamento do mel, representando um impacto negativo (COSTA et al., 2017). A capacitação técnica nas etapas desde o manejo das colônias até a comercialização do produto é de extrema importância de modo a garantir uma cadeia produtiva de qualidade. Contudo, o “Selo Arte” criado com a Lei 13.680 (BRASIL, 2018) trouxe avanços em relação à comercialização dos méis de abelhas sem ferrão, uma vez que os produtos artesanais de origem animal, que passaram por fiscalizações regionais (municipal ou estadual), e podem ter a sua comercialização permitida em todo o território nacional. Para tanto, devem estar devidamente registrados e apresentarem características e processo de manipulação artesanal (BARBIÉRI e FRANCOY, 2020).
A maior parte dos meliponicultores não possui registro e não emite notas de compra e venda, logo não há estimativas reais da movimentação econômica da meliponicultura no Brasil. Devido a essa amplitude das características peculiares dessas abelhas nativas do país, não se tem uma instrução normativa única para os produtos da meliponicultura, como ocorre com os produtos da apicultura. O fato decorre dos enormes desafios para que a produção e a comercialização de mel e outros produtos de abelhas nativas sem ferrão sejam regulamentadas em todo território nacional (VILAS BOAS, 2012; KOSER et al., 2020).
Alguns estados brasileiros, de forma independente e no âmbito de sua autonomia, elaboraram leis estaduais específicas para a regulamentação do mel de abelhas nativas da sua região, que dispõem sobre a criação, o manejo, o comércio e o transporte de abelhas sociais nativas (meliponíneos) de cada estado (PARANÁ, 2017). Um exemplo é a Lei 19.152 de 2017 para o estado Paraná, que estabelece, além de regras de conformidade, a criação de um selo de certificação ambiental, que autoriza o produtor a vender e comercializar espécies nativas (PARANÁ, 2017). Essas iniciativas contribuem para o comércio local do mel e de colônias de abelhas sem ferrão, mas não permite a comercialização interestadual (ADAB, 2014, ADAPAR, 2017) e de colônias fora de seu bioma (CONAMA, 2020).
13
¶ 1.5 Importância econômica da sanidade e perdas de acesso a mercados
A ocorrência de doenças nas colônias pode acarretar prejuízos diretos na cadeia produtiva apícola e meliponícola devido a diminuição da produtividade e perdas de enxames em casos graves, e indiretos com perda de mercado interno e externo. No Brasil, os produtos apícolas têm se expandido, conquistado o mercado interno e mundial, gerando crescimento no setor com oportunidades para produtores e empresas do segmento (MARTINEZ e SOARES, 2012; BALBINO et al., 2015). As abelhas africanizadas apresentam maior resistência e, somado as condições climáticas do Brasil, a ocorrência e os danos provocados por doenças e pragas são menores, quando comparados às abelhas europeias (CAMARGO et al., 2002).
Em virtude do risco potencial que a presença de patógenos pode causar, os apicultores e meliponicultores devem estar sempre atentos à situação sanitária das abelhas, conferindo a saúde de suas colônias. Para isso, devem estar capacitados ao reconhecimento visual das anormalidades que possam indicar a presença de possíveis doenças, o que auxiliará a evitar a disseminação e o impacto de novas doenças no Brasil. A capacitação e introdução de novas técnicas se tornam práticas indispensáveis para auxiliar na redução dos efeitos e prejuízos que as pragas e doenças podem acarretar para o mercado da apicultura e meliponicultura nacionais (TASSINARI et al., 2013, FREITAS et al., 2017).
Sabendo reconhecer os principais sintomas de doenças e pragas, o apicultor poderá tomar medidas imediatas e necessárias, como o isolamento das colônias atacadas, e comunicação imediata ao serviço de defesa animal do estado. Esta comunicação possibilitará a realização de procedimentos de atendimento à notificação de doença, coleta de amostras pelo médico veterinário oficial e seu envio para laboratórios oficiais ou credenciados para análise e diagnóstico precisos. Assim, o produtor colaborará para evitar a contaminação de seus apiários e meliponários, e também apiários e meliponários presentes em sua região e para a saúde apícola do País.
¶ 2. BIOLOGIA DE Apis mellifera E MELIPONINI
A grande diversidade de abelhas no mundo engloba abelhas que possuem desde hábitos solitários até altamente sociais. Por isso, iremos focar nas informações que permitam um reconhecimento fácil e eficiente das principais características das abelhas em campo, sobretudo para fins de manejo, considerando apenas Apis mellifera (criadas na apicultura) e as da tribo Meliponini (criadas na meliponicultura).
¶ 2.1 Considerações gerais sobre a nomenclatura e classificação
Tanto Apis mellifera quanto abelhas sem ferrão fazem parte dos organismos altamente sociais ou eussociais, que serão abordados detalhadamente no capítulo 3. Assim sendo, compartilham muitas características evolutivas, ecológicas e fisiológicas. De acordo com Michener (1969), por definição, para comporem este grupo, é necessário que três requisitos básicos sejam cumpridos: (1) sobreposição de gerações dentro do mesmo ninho, (2) o cuidado com a prole de forma cooperativa, e (3) divisão de tarefas entre os membros.
Outro aspecto importante é em relação à classificação destes grupos. As abelhas africanizadas estão incluídas na tribo Apini e as abelhas sem ferrão em Meliponini, sendo esta última caracterizada pela presença de um ferrão vestigial, ou seja, não funcional (MICHENER, 2013). Em outras palavras, as abelhas da tribo Meliponini não ferroam, daí o seu nome popular “abelhas sem ferrão”.
¶ 2.2 Ciclo de vida das abelhas
As abelhas pertencem à classe Insecta (insetos) e à ordem Hymenoptera. O ciclo de vida dos organismos desta ordem, que abrange também as formigas e as vespas, é dito de desenvolvimento holometabólico, ou desenvolvimento completo. Em outras palavras, os indivíduos passam pelas fases de ovo - larva - pré-pupa - pupa - inseto adulto (Figura 2.1) (WINSTON, 2003; DA CRUZ-LANDIM, 2009).

¶ 2.2.1 Apis mellifera
A fase larval representa a fase de intensa alimentação, que é aquela em que a abelha ganha peso e cresce. Durante este período, as células de cria estão abertas e, após a sua operculação pelas operárias adultas, a larva tece o casulo e passa para a fase de pupa. Nesta fase da metamorfose, na qual a abelha não se alimenta, ocorrem os processos de pigmentação de olhos e corpo e, ao final, atinge a fase adulta (Tabela 2.1). Quando a transformação está completa, o adulto recém-formado rói o opérculo, sai da célula e finaliza o seu desenvolvimento durante os próximos dias (WINSTON, 2003).
| Tabela 2.1. Tempo médio de desenvolvimento em dias de abelhas A. mellifera europeias e africanizadas. | |||||||
|---|---|---|---|---|---|---|---|
| Indivíduo | Ovo | Larva | Pupa | TOTAL | |||
| Europeia | Africanizada | Europeia | Africanizada | Europeia | Africanizada | ||
| Operárias | 3 | 6 | 5 | 12 | 12 | 21 | 20 |
| Zangões | 3 | 7 | 6,5 | 14 | 14,5 | 24 | 24 |
| Rainha | 3 | 6 | 5 | 7 | 7 | 16 | 15 |
¶ 2.2.2 Meliponini
Em abelhas sem ferrão, todos os processos de muda e metamorfose também ocorrem. No entanto, um aspecto importante é que, em seguida à postura dos ovos pela rainha, as células de cria são imediatamente lacradas pelas operárias (SOMMEIJER et al., 1982), uma vez que todo o alimento larval já foi depositado antes da postura.
¶ 2.3 Os tipos de abelhas (ou castas)
Dentro das colônias, de ambos os grupos, existem nas colônias três tipos básicos de indivíduos: as rainhas e as operárias (ambas fêmeas) e os machos (Figura 2.2). No entanto, quando falamos em castas, essa definição consiste na diferenciação comportamental e morfológica na grande maioria das espécies sociais, entre as fêmeas que compõem uma colônia. Para abelhas então, temos duas castas: a reprodutiva composta pelos machos e a rainha, responsável pela postura de ovos, e a casta operária, representada pelas abelhas que exercem diversas tarefas para o crescimento e a manutenção da colônia: construção de células de cria, alimentação da cria, coleta de alimento, defesa do ninho.
_(pdf.io).jpg)
¶ 2.4 A diferenciação de castas e sexo
Em abelhas, rainhas e operárias se desenvolvem a partir de ovos fertilizados, e os machos a partir de ovos não-fertilizados (reprodução por partenogênese) (DA CRUZ-LANDIM, 2009). Para a compreensão dos mecanismos de formação de rainhas em abelhas, é necessário conhecer os sistemas de alimentação larval, os quais são completamente distintos entre A. mellifera e abelhas sem ferrão (DIETZ e HAYDAK, 1971; HARTFELDER et al., 2006). Além disso, existem diferenças até mesmo entre os meliponíneos.
Em A. mellifera, a rainha faz a postura de ovos na célula de cria e, frequentemente as operárias inspecionam as células para a deposição do alimento larval (BROUWERS et al., 1987). A este processo dá-se o nome de alimentação progressiva. Em abelhas sem ferrão, as operárias nutrizes depositam todo o alimento que será consumido ao longo do desenvolvimento logo antes da oviposição (Figura 2.3). Então, a rainha oviposita sobre o alimento larval e, imediatamente a célula de cria é lacrada pelas operárias (HARTFELDER et al., 2006).
¶
2.4.1 Apis mellifera
Em A. mellifera, os fatores que determinam quem irá se tornar operária ou rainha são diretamente relacionados à alimentação que as larvas recebem (DIETZ e HAYDAK, 1971). A rainha recebe geleia real durante todo o seu desenvolvimento. Esse alimento é composto de secreções das glândulas mandibulares e hipofaringeanas, com a presença de açúcares do néctar (HAYDAK, 1970). O alimento difere com relação ao alimento das larvas que se tornarão operárias por conter mais secreções da glândula mandibular e na quantidade que é fornecida à cria (WINSTON, 2003).
Para Winston (2003), além da alimentação, a estrutura na qual os ovos são depositados pode ser um estímulo importante para prover informações acerca da futura casta/sexo. Por exemplo, um ovo posto em uma célula de operária pode ser transferido para uma de rainha (realeira) e transformar-se em princesa, sob condições favoráveis (Figura 2.4). Da mesma forma, um ovo transplantado de uma realeira para uma célula de operária originará um indivíduo desta casta.
.jpg)
¶ 2.4.2 Meliponini
O mecanismo de determinação de rainhas consiste na principal diferença entre os meliponíneos. Em abelhas do gênero Melipona, os fatores que determinam as castas são alimentares e genéticos (HARTFELDER et al., 2006). A quantidade de alimento recebida por operárias e rainhas é o mesmo, impossibilitando a distinção de uma realeira (as células de cria são do mesmo tamanho). Nas demais abelhas sem ferrão, aquelas larvas que irão se tornar rainhas são alimentadas com uma quantidade maior que o dobro de alimento do que aquelas que serão operárias (MENEZES et al., 2013). Assim, as células de cria de rainhas, ditas realeiras, são visivelmente diferenciadas.
¶ 2.5 Recursos alimentares
As abelhas utilizam recursos retirados das plantas para alimentação, crescimento e desenvolvimento das colônias. As operárias forrageiras coletam o pólen como principal fonte de proteína e néctar como fonte de carboidratos (MICHENER, 1974). A água também é um recurso essencial para abelhas. Durante a coleta de pólen em flores, as abelhas forrageiras aglomeram grãos de pólen em suas corbículas usando uma mistura de néctar e saliva, tal processo facilita a adesão do pólen à corbícula (VOLLET-NETO, 2017). Já o néctar, após ser coletado nas flores, é armazenado em uma estrutura conhecida como o papo das abelhas, e conduzido para dentro das colmeias (ROUBIK, 2006). A coleta de água, quando ocorre, também é armazenada dentro do papo (FREITAS et al., 2007).
¶ 2.5.1 Apis mellifera
Essas abelhas depositam pólen, néctar, mel, e mantêm as suas crias nos mesmos tipos de favos (Figura 2.5), diferentemente do que ocorre em abelhas sem ferrão, como será apresentado a seguir. Vásquez e Olofsson (2009) relataram em A. mellifera a existência de bactérias entéricas das abelhas no pólen recém-coletado, bem como no pólen armazenado no ninho, o que sugere que as abelhas operárias podem inocular microrganismos no pólen durante a coleta em flores. A água como recurso possui quatro funções principais em A. mellifera: o consumo próprio, a regulação de umidade no interior do ninho, diluição do mel e resfriamento da temperatura corporal (ABOU-SHAARA, 2012).
.jpg)
¶ 2.5.2 Meliponini
As abelhas sem ferrão armazenam grãos de pólen e néctar trazidos do campo dentro de potes feitos com cerume (cera + resina), sendo estes, estruturas separadas do ninho (onde ficam as crias) (Figura 2.6). O néctar será processado e desidratado, a fim de ser convertido em mel. Os grãos de pólen são inicialmente frescos e, posteriormente, fermentados (VOLLET-NETO et al., 2017).
.jpg)
Figura 2.6. Vista superior de uma colônia de abelhas sem ferrão (Melipona scutellaris). A seta vermelha indica um pote de pólen; a azul indica um pote de mel em construção; a seta verde representa o invólucro que abriga o ninho (onde ficam as crias). (Foto: Annelise de Souza Rosa Fontana)
Para garantir um fornecimento constante de alimentos e, consequentemente, aumentar as chances de sobrevivência da colônia durante os períodos de escassez de recursos, eles são estocados no ninho (ROUBIK, 1982; MAIA-SILVA et al., 2015). Vollet-Neto et al. (2017) verificaram que as abelhas recém-emergidas consomem muito pólen e elas têm uma preferência significativa pelo pólen fermentado ao invés do pólen fresco. Existem três motivos para tal comportamento: (1) as preferências inatas de abelhas jovens pelo pólen fermentado; (2) a presença de níveis mais elevados de substâncias atraentes no pólen fermentado; e (3) pode haver um aprendizado associativo da fase de larva, pois durante o desenvolvimento a exposição ao pólen fermentado no alimento larval é constante.
A água, para abelhas sem ferrão, serve para a diluição do mel e para compor o alimento larval (ROUBIK, 2006). O mel de meliponíneos é visivelmente mais líquido, assim como o alimento larval. Hartfelder e Engels (1989) relataram que o alimento larval regurgitado pelas operárias de abelhas sem ferrão é constituído por mel, pólen e secreções glandulares, sendo composto por 40-60% de água, 5-12% de açúcares, 1,1-19,4% de proteínas, 0,2-1,3% de aminoácidos livres e 15-30% por pólen.
¶ 2.6 Tamanho populacional das colônias
O tamanho populacional das colônias depende da espécie. Normalmente, uma colônia de abelhas A. mellifera possui entre 60.000 e 80.000 operárias, uma rainha e entre zero e 400 zangões. Proporcionalmente, espécies de abelhas sem ferrão possuem um número relativamente reduzido de indivíduos, podendo variar de cerca de 300 (em gêneros como Nanotrigona) até mais de 10.000 (como em Scaptotrigona) por colônia.
¶ 2.7 Material utilizado e local de construção dos ninhos
¶ 2.7.1 Apis mellifera
As colônias de A. mellifera, por serem muito populosas, necessitam de locais de maior volume para nidificar, que são geralmente ocos de árvores. As cavidades do ninho são verticalmente alongadas e cilíndricas. De acordo com Seeley (2006), encontrar um local apropriado para nidificação é apenas a primeira etapa de uma longa trajetória, até a conclusão do ninho. O material básico para a construção é a cera, produzida pelas glândulas da parte inferior do seu abdome. A construção do ninho tem início assim que um enxame entra na cavidade escolhida. Inicialmente, as abelhas roem toda a madeira podre do teto da cavidade, preparando uma superfície sólida para prender os favos novos. Em seguida, elas se agrupam e, a grande maioria, se ocupa em secretar placas minúsculas de cera. A construção do favo se dá quando as abelhas individuais com placas de cera bem desenvolvidas começam a se desvencilhar de suas irmãs, sobem pelo agrupamento de abelhas e depositam sua cera depois de mastigar cada placa, para misturá-la com uma secreção da glândula mandibular, tornando a cera mais plástica.
¶ 2.7.2 Meliponini
Os meliponíneos podem nidificar nos mais diversos e inusitados locais, podendo ser em solo, troncos ocos de árvores, buracos em rochas, paredes, cavidades já existentes e em barrancos. Nogueira-Neto (1997) e Villas-Bôas (2012) observaram que uma colônia de meliponíneos pode ser formada a partir de uma série de materiais encontrados na natureza, sendo eles o barro e resinas e outros que são produzidos ou processados dentro da colônia, a exemplo do cerume, da própolis ou da geoprópolis, e ainda com material secretado pelas próprias abelhas através do seu abdome, a cera.
De acordo com Nogueira-Neto (1997), a estrutura interna das colônias é construída a partir do cerume, que nada mais é que uma mistura de cera produzida por secreção glandular de abelhas jovens, com própolis que é constituída, principalmente, por resinas coletadas das plantas. O barro é muito utilizado por meliponíneos para a construção das entradas dos ninhos e é o principal constituinte da geoprópolis, que é uma mistura do barro com própolis. A geoprópolis tem características de cimento e é utilizada na vedação da colônia e delimitação de espaços. As grandes massas são denominadas de batumes.
Ainda existem outros materiais utilizados para a construção de ninhos em certos tipos de meliponíneos. A espécie Trigona spinipes, conhecida como abelha- cachorro, utiliza na construção de seus ninhos outros tipos de materiais, como sementes e excrementos animais. Registros de excrementos de origem animal também foram verificados na construção de ninhos de Melipona quadrifasciata, M. subnitida e M. scutellaris. Em função dos muitos hábitos de preocupação higiênico-sanitária encontrados em certos meliponíneos, Nogueira-Neto (1997) enfatizou a importância da pasteurização do mel antes do consumo humano.
¶ 2.8 Arquitetura dos ninhos
¶ 2.8.1 Apis mellifera
O ninho de A. mellifera é composto por favos verticais, formados por alvéolos, com formato hexagonal. Esse formato permite a otimização do uso de material, maior aproveitamento do espaço e maior resistência física para suportar o peso do mel armazenado. Os alvéolos possuem dois tamanhos, sendo naqueles maiores realizadas as posturas de ovos de zangão, e nos menores postura de ovos de operárias ou usados para estocagem de alimento. A prole é criada nas partes centrais da colônia, de forma a facilitar o controle de temperatura pelas operárias. Nessas abelhas, os favos são verticais (Figura 2.7), e as crias, o mel e o pólen encontram-se nos mesmos tipos de alvéolos. O pólen depositado nos alvéolos passa a ser chamado de pão da abelha.
.jpg)
¶ 2.8.2 Meliponini
Uma colônia de meliponíneos é formada por duas estruturas principais: o ninho e os potes de alimento, além de estruturas auxiliares que não ocorrem necessariamente em todas as espécies, como o invólucro, o batume, o túnel de entrada, lixeira e depósito de resina ou própolis (VILLAS-BÔAS, 2012). Os potes de alimento são, em sua maioria, elipsoides, construídos de cerume, e podem apresentar diferentes tamanhos dependendo da espécie. Pólen e mel são armazenados de forma separada em potes distintos, especificamente para cada recurso.
A estrutura do ninho de meliponíneos é formada por cerume, possuindo características distintas de acordo com a espécie. Pode ser formada por células agrupadas, formando discos horizontais (Figura 2.8), verticais (apenas duas espécies), em espiral ou em cachos, quando as células são esparsas e conectadas por pilares de cerume, como por exemplo a espécie Frieseomelitta varia conhecida como marmelada.
.jpg)
¶ 2.9 Comportamento enxameatório
¶ 2.9.1 Apis mellifera
De acordo com Winston (2003), em A. mellifera, são reconhecidos dois tipos de enxames: o natural (reprodutivo) e o de abandono ou migração. Na enxameação natural, a maioria das operárias e a rainha velha (enxame primário), ou uma nova (enxames secundários) saem do ninho para procurar um novo local para nidificar, na maioria das vezes distante da colônia mãe.
A principal característica quando um enxame sai são grandes zumbidos causado por milhares de abelhas que procuram sua rainha e um lugar para se aglomerar. Após deixarem a colônia parental, o enxame voa em massa, a curta distância, e os indivíduos fixam-se num suporte, como, por exemplo, um galho de árvore, formando uma aglomeração tipo “cachos” onde permanecem provisoriamente até o voo para o local de nidificação definitivo. Este tipo de enxameação ocorre geralmente quando as condições ambientais são ótimas, de maneira que o espaço da cavidade do ninho que a população de abelhas ocupa se torne pequeno. Nos momentos que antecedem a enxameação, as operárias promovem o nascimento de uma outra rainha e a rainha velha e suas acompanhantes voam para um outro local. Este tipo de enxame é denominado de enxame primário, no qual sempre há uma rainha fecundada.
O enxame de abandono é caracterizado por abandonar seu local de nidificação deixando crias abertas, crias fechadas e alimento estocado. Para Toledo (1997), existem vários motivos para isto como por exemplo: excesso de fumaça, falta de recursos florais, condições climáticas adversas, estresse devido à predadores e pragas e presença de substâncias químicas tóxicas.
¶ 2.9.2 Meliponini
Por outro lado, a enxameação de abelhas sem ferrão é um processo gradual, com várias etapas, podendo levar várias semanas para o estabelecimento no novo local. Em abelhas sem ferrão, as enxameações ocorrem por conta da superpopulação da colônia, e está associado à abundância de oferta de alimento em campo. O local selecionado não deve ser tão distante da colônia mãe, pois a colônia filha necessita de contato com esta por algumas semanas para obter provisões, até que esteja concluído o estabelecimento no novo local. Brand (2018) reportou que as abelhas menores, a exemplo da jataí, buscam um local para nidificação a poucos metros da colônia mãe, enquanto abelhas maiores, como a mandaçaia, podem ir a maiores distâncias, podendo chegar a 300 metros. Nas primeiras etapas algumas forrageiras saem a campo em busca de um local, podendo encontrar muitos locais distintos e iniciar paralelamente o preparo. Entretanto, para a escolha de apenas um, as abelhas sem ferrão são bastante exigentes e criteriosas, a fim de assegurar o sucesso da nova moradia.
O primeiro ponto a ser considerado é a limpeza, no qual os pedaços de madeira são postos para fora, as frestas são lacradas com geoprópolis e a construção da entrada é iniciada. Procede-se a construção dos potes de mel, tendo como fonte a colônia mãe, que está próxima ao novo ninho. A seguir, se procede a construção dos invólucros do ninho e na parte interna, as células de cria, conferindo o início da formação do disco, tornando o novo lar apto a receber a princesa (rainha virgem). O instante em que se observa uma maior agitação na colônia mãe, é a partida da princesa com muitas operárias e zangões. Esses últimos são aqueles que percorrem grandes distâncias atraídos pelo feromônio da jovem princesa, que pode ou não ser fecundada nesta fase. Mesmo com início da postura da nova rainha, o fluxo de comunicação entre as colônias pelas operárias continua muitas vezes por semanas, a fim de garantir os suprimentos necessários para o novo lar (BRAND, 2018).
¶ 3. ANATOMIA, FISIOLOGIA E ORGANIZAÇÃO SOCIAL
As abelhas são insetos estruturados por uma série de anéis endurecidos conectados entre si por membranas, sendo recoberta por pelos em toda extensão corporal, incluindo os olhos compostos. Esse esqueleto externo (exoesqueleto) serve como proteção contra predadores, desidratação, está envolvido na estruturação muscular e permite movimentos rápidos. O exoesqueleto e as partes internas estão organizados em três partes distintas: cabeça, tórax e abdômen. A estrutura geral de uma abelha é ilustrada na Figura 3.1. Cada parte é chamada de tagma, definida como agrupamentos funcionais do corpo de um inseto. Neste documento serão abordadas as estruturas correspondentes às abelhas Apis mellifera e as sem ferrão, que possuem organização eussocial. A maioria das informações a serem descritas a seguir, referentes à anatomia, baseiam-se nas obras de Snodgrass (1956), Winston (1991), Seeley (1992) e Fransozo (2017).
.jpg)
¶ 3.1 Anatomia externa e interna
¶ 3.1.1 Cabeça
Na cabeça encontram-se, de maneira geral, algumas glândulas, as peças bucais e estruturas sensoriais cefálicas.
¶ 3.1.1.1 Antenas
As antenas possuem os sentidos da audição, do olfato e do tato, fundamentais na escuridão da colmeia. Por meio do olfato elas reconhecem outras operárias do ninho e detectam seus inimigos. No par de antenas estão localizadas as cavidades olfativas, com função de captar odores como o de floradas, ou de rainhas virgens por parte dos zangões. Os zangões contam com cerca de 30 mil cavidades olfativas, as operárias apresentam de 4 a 6 mil e a rainha apresenta cerca de 3 mil cavidades. Cada antena é dividida em três partes: o escapo, ligado à cabeça; o pedicelo (segmento intermediário); e o flagelo, segmento terminal constituído de 10 partes na fêmea e 11 no macho.
¶ 3.1.1.2 Olhos simples e compostos
O complexo sistema visual das abelhas é composto por três olhos simples, situados na parte frontal da cabeça e dois olhos compostos, localizados nas laterais da cabeça, e são capazes de enxergar a longas distâncias. Cada olho composto é formado por milhares de facetas. O número de facetas varia conforme o indivíduo, de 7.000 a 8.600 no zangão, de 4.000 a 6.300 na operária e de 3.000 a 4.000 na rainha. Cada faceta responde individualmente à entrada de ondas luminosas e os agrupamentos de facetas são especializados em diversas funções como perceber planos de polarização da luz, padrões de reconhecimento, as cores e ainda acompanhar os movimentos da cabeça. Os olhos simples, também conhecidos como ocelos, têm a função de detectar a intensidade luminosa e, possivelmente, regulam o padrão das atividades diurnas ou são utilizados para simples orientação quanto à posição do sol.
¶ 3.1.1.3 Aparato bucal
Com relação às peças bucais das abelhas, são do tipo mastigador e sugador. Sugar é um modo de alimentação em que o alimento líquido ou semilíquido é transferido do substrato para a boca, aderindo a um órgão protrátil chamado glossa ou língua. As glossas labiais alongadas e fundidas formam uma língua peluda, que é cercada por gáleas maxilares e palpos labiais para formar uma probóscide tubular que contém o canal alimentar. Na alimentação, a glossa é mergulhada no néctar floral ou no mel, que adere aos pelos, e depois é recolhida de modo que o líquido aderido seja carregado para dentro do espaço entre as gáleas e os palpos labiais. Esse movimento para frente e para trás da glossa ocorre repetidamente. O movimento do líquido para a boca parece resultar da ação da bomba do cibário, facilitado por cada retração da glossa que empurra o líquido para dentro do canal alimentar.
As lacínias e os palpos maxilares são rudimentares e a paraglossa envolve a base da língua, direcionando a saliva do orifício salivar dorsal para dentro de um canal ventral, a partir de onde ela é transportada para o flabelo, um pequeno lóbulo na ponta da glossa; a saliva pode dissolver açúcares sólidos ou semilíquidos. As mandíbulas, esclerotizadas, em forma de colher, ficam na base da probóscide e têm diversas funções, incluindo a manipulação da cera e de resinas vegetais para a construção do ninho, alimentação das larvas e da rainha, limpeza, lutas e retirada de resíduos do ninho, inclusive abelhas mortas.
Ainda na cabeça estão localizadas as glândulas mandibulares, que dissolvem a cera e ajudam a produzir a geleia real juntamente com as glândulas hipofaringeanas, que estão em funcionamento pleno do 5º ao 12º dia de vida da operária e transformam o alimento comum em geleia real. A geleia é fornecida para todas as larvas nos primeiros dias de vida larval e para a rainha durante todo o período larval e vida adulta.
¶ 3.1.1.4 Faringe (anatomia interna)
Associada à parte interna da cabeça encontra-se a faringe. Esta, por sua vez, é a segunda porção do tubo digestivo da abelha, que liga o aparelho bucal ao esôfago.
¶ 3.1.2 Tórax
O tórax é composto de três segmentos: o primeiro ou protórax, o segundo ou mesotórax, e o terceiro ou metatórax. O tagma torácico é aquele que abriga os órgãos referentes à locomoção das abelhas: as pernas e as asas.
¶ 3.1.2.1 Pernas
Cada um dos três pares de pernas possui uma função. O primeiro par de pernas é forrado por pelos microscópicos que servem para limpar as antenas, os olhos, a glossa e as mandíbulas. O segundo par conta com um esporão, com função de limpeza das asas e a retirada do pólen acumulado nas corbículas. Na face externa da tíbia, no terceiro par de pernas localiza-se a corbícula ou sesta do pólen que serve para o transporte do pólen coletado pelas operárias, das flores até os favos do ninho (Figura 3.2). Além das corbículas, existem pentes e espinhos, cuja finalidade serve para retirar as partículas de cera elaboradas pelas glândulas ceríferas, que se localizam nos tergitos abdominais.
Cada perna é formada por seis segmentos: coxa, trocânter, fêmur, tíbia, tarso (constituído de 2 a 5 partes - tarsômeros), pretarso (é o “pé” das abelhas).
.jpg)
¶ 3.1.2.2 Asas
As asas são extensões membranosas do exoesqueleto adaptadas para possibilitar o voo dos dois pares de asas, que se encontram nos segmentos torácicos posteriores. As asas se prendem ao tórax por articulações complexas que permitem uma grande variedade de movimentos. As anteriores são maiores e ligadas ao mesotórax, e as posteriores, menores e ligadas ao metatórax. As asas possuem um complexo sistema de venação (veias) que, além de servir ao fortalecimento das estruturas, são importantes no transporte de hemolinfa e na respiração. A velocidade do voo e a distância dependem dos músculos torácicos que são supridos com a energia derivada do metabolismo do néctar. Para voar, as abelhas juntam a asa anterior com a posterior por meio de pequenos ganchos chamados hámulos, aumentando a superfície de contato com o ar.
¶ 3.1.2.3 Esôfago e espiráculos (anatomia interna)
Associados à parte interna do tórax estão o esôfago e os espiráculos. O esôfago segue-se à faringe e vai em direção a vesícula melífera, e está relacionado ao sistema digestório. Os espiráculos abrem-se nas traqueias torácicas e são associados ao sistema respiratório.
¶ 3.1.3 Abdômen
O abdômen abriga a maioria dos órgãos das abelhas. Nele estão situados a vesícula melífera que serve para transporte de néctar, mel e água, estômago, intestino delgado, glândulas cerígenas e as traqueias e espiráculos. No abdômen dos zangões estão localizados seus órgãos reprodutores, constituídos por um par de testículos, duas glândulas de muco e pênis. Nas fêmeas o sistema reprodutor inclui dois ovários, dois ovidutos laterais, oviduto médio, espermateca (bolsa onde a rainha armazena os espermatozoides dos zangões que a fecundaram) e a glândula acessória (glândula de Dufour). Ainda se localiza os corações que são em números de sete, que comandam o aparelho circulatório, formado pela artéria aorta. Diferentemente dos animais homeotérmicos o sistema circulatório nas abelhas é aberto, ou seja, a hemolinfa é bombeada para o tórax e cabeça, retornando aos corações por ação do diafragma.
Na parte interna das abelhas, tem-se então os seguintes órgãos (Figura 3.3):
- Vesícula melífera: é neste órgão que o néctar colhido das flores inicia sua transformação em mel para depois ser depositado nos alvéolos ou potes de mel, como no caso de abelhas sem ferrão.
- Proventrículo: é constituído por uma válvula localizada na extremidade posterior da vesícula melífera, servindo para controlar a passagem do alimento para o ventrículo.
- Ventrículo: este, por sua vez, é dito o estômago verdadeiro da abelha. Neste local se inicia a digestão do alimento que passa ao intestino delgado.
- Intestino delgado: local em que ocorre a finalização da digestão e assimilação.
- Ampola retal: possui a função de retenção das fezes até a abelha realizar o voo de higiene. Quando isso não acontece a abelha apresenta o abdômen volumoso.
- Tubos de Malpighi: correspondem aos rins, sendo numerosos filamentos excretores. - Traqueias, espiráculos e sacos aéreos: há um par de espiráculos em cada segmento do abdômen que se comunicam com as traqueias e estas, por sua vez, se ligam aos sacos aéreos.
- Ferrão: está localizado no último segmento abdominal das operárias e rainha. O zangão não possui ferrão. Na operária serve de instrumento de defesa e na rainha como guia de postura ou ovipositor. É constituído de três partes: um estilete e duas lancetas. O estilete é a parte que perfura o tecido. As lancetas possuem farpas que prendem o ferrão na superfície ferroada, dificultando sua retirada. O ferrão liga-se à bolsa de veneno e às glândulas ácidas e básicas protegidas por duas bainhas. O ferrão apresenta de sete a nove farpas nas operárias com musculatura fraca, o que facilita a perda do ferrão. Na rainha, o ferrão possui de duas a três farpas com musculatura forte, o que dificulta a sua perda.
As abelhas sem ferrão, na realidade, possuem um ferrão. Porém, ele é atrofiado evolutivamente, não sendo então, funcional.
.jpg)
Figura 3.3. Órgãos de uma abelha, 1- Glossa; 2- Palpo labial; 3- Gálea; 4-Ducto das glândulas salivares; 5- Glândula mandibular; 6- Faringe; 7- glândulas hipofaringeanas; 8- Cérebro; 9- Glândulas salivares da cabeça e tórax; 10- Esôfago; 11- Coração; 12- Papo; 13- Tubos de Malpighi; 14- Ventrículo; 15- Reto; 16- Gânglios torácicos; 17- Corbícula. (Imagem: Cláudio Gomes da Silva Júnior Pedroso)
¶ 3.2 Fisiologia
¶ 3.2.1 Sistema respiratório
O sistema de traqueias está conectado com o exterior através de uma série de orifícios no exoesqueleto, chamados espiráculos. Quando a abelha está sem movimento, a troca de gás ocorre simplesmente por difusão. Entretanto, durante os períodos de grande atividade da abelha, como o voo, o seu abdômen bombeia para aumentar a troca de gás e usa os sacos expandidos na traqueia.
¶ 3.2.2 Sistema circulatório
Tal como em todos os insetos, o sistema circulatório é aberto, consistindo apenas do coração dorsal e da aorta, que auxilia na circulação. A hemolinfa enche a cavidade do corpo da abelha, de maneira que os órgãos flutuem livremente. A hemolinfa entra no coração por uma válvula de retenção chamada óstio, e é bombeada pela aorta. As principais funções do sistema circulatório são: transporte de alimento do ventrículo para células do corpo, remoção de restos de material das células e entrega desse material aos órgãos excretores, lubrificação das articulações do corpo, e defesa contra patógenos.
¶ 3.2.3 Sistema digestório
Localiza-se no abdômen e se conecta com a boca pelo longo esôfago. A extremidade posterior do esôfago se abre na vesícula melífera, bolsa expansível que retém o mel ingerido e é usado como fonte de energia durante o voo, bem como o néctar e a água coletados. A vesícula melífera cheia ocupa a maior parte da cavidade abdominal. O proventrículo impede que o conteúdo da vesícula melífera passe para o ventrículo. Os grãos de pólen da vesícula melífera são, porém, capturados junto com algum líquido e são passados para o ventrículo e, posteriormente, intestino delgado locais em que ocorre a sua digestão e absorção.
Os restos sólidos que consistem principalmente de pólen, glóbulos gordurosos e células mortas são passados do intestino delgado para o reto para serem excretados. O reto se expande consideravelmente para reter as fezes durante o inverno, uma vez que as abelhas normalmente não defecam na colmeia e esperam por um tempo propício na primavera para o voo de higiene a fim de eliminar as fezes acumuladas.
¶ 3.2.4 Sistema nervoso
A estrutura do sistema nervoso consiste em um cérebro e sete gânglios ou células nervosas em várias junções ao longo do corpo. A maior parte do controle nervoso exercido pela abelha não é executada pelo cérebro, mas por esses centros que provém um controle local sobre uma parte da sua musculatura.
¶ 3.2.5 Sistema glandular
As abelhas contam com um sistema glandular complexo e diversificado, constituído por glândulas espalhadas por todo o corpo, as quais serão descritas a seguir.
¶ 3.2.5.1 Glândulas hipofaringeanas
Localizadas na cabeça, possuem a função de transformar o alimento comum (mel e pólen) em geleia real. Apenas as operárias as possuem e desenvolvem-se a partir do 4° ou 5° dias de vida, prolongando-se até o 14° ou 15°. De acordo com Haydak (1970), as larvas que serão rainhas são predominantemente alimentadas com uma secreção branca até o terceiro dia e, a partir do quarto, passam a receber uma alimentação mais clara. O pH das secreções indica que a substância branca provém das glândulas mandibulares, enquanto aquela mais clara se trata de uma mistura de secreção das glândulas hipofaringeanas e mel.
¶ 3.2.5.1 Glândulas salivares
Localizadas na cabeça e no tórax, existem em todas as abelhas (rainhas, operárias e machos). A secreção é um líquido ligeiramente alcalino, utilizado para dissolver e diluir os alimentos açucarados, para lavar as superfícies em que eles estão depositados e, ainda, para umedecer as substâncias mastigadas.
¶ 3.2.5.3 Glândulas mandibulares
Localizadas na cabeça e existem nas duas castas e nos machos, diferindo de tamanho e função. Na rainha, essas glândulas produzem o “feromônio da rainha”, que consegue assim atrair os zangões. Permitem também que as operárias possam reconhecê-la quando suficientemente próximas. Nas operárias jovens, essas glândulas estão envolvidas na produção do alimento larval (componente lipídico). Nas operárias adultas, ocorre a produção de feromônio de alarme.
¶ 3.2.5.4 Glândulas cerígenas
Existem quatro pares de glândulas localizadas do quarto ao sétimo tergitos abdominais. Apresentam o pico de desenvolvimento entre o 9° e o 18° dia. As operárias produzem a cera na forma líquida dissolvida em uma substância volátil que, em contato com o ar, se solidifica formando pequenas escamas.
¶ 3.2.5.5 Glândula de Nasonov ou de orientação
Localizada no 7° segmento dorsal do abdômen das abelhas operárias, possui como função a emissão de um odor que permite o reconhecimento entre as abelhas de uma mesma colônia. Está presente nas operárias e ausente nos zangões.
Em abelhas sem ferrão, o cheiro é utilizado para comunicar a identificação de locais ou recursos florais (por exemplo, entrada, saída), e, portanto, coordenar os movimentos do enxame, atrair abelhas perdidas para a entrada de um ninho e guiar as forrageadoras recrutadas para a fonte de alimento.
¶ 3.2.5.6 Glândulas ácidas e básicas
Localizadas próximo ao ferrão, estão presentes nas operárias e na rainha. Produzem toxinas e participam no estímulo do comportamento defensivo nas operárias.
¶ 3.2.5.7 Glândulas de muco
Localizadas no sistema reprodutor do zangão. Participa do processo de maturação dos espermatozoides. Quando são esvaziadas liberam os espermatozoides junto com um muco de coloração esbranquiçada.
¶ 3.2.5.8 Glândulas espermáticas
Localizadas no sistema reprodutor da rainha, atuam no sistema de armazenamento de espermatozoides.
¶ 3.2.6 Sistema reprodutor
¶ 3.2.6.1 Zangão
O sistema reprodutor nos zangões é composto por um par de testículos, onde são gerados os espermatozoides, e por canais deferentes, que se ligam às vesículas seminais, as quais se unem ao conduto seminal ou ejaculador que desemboca no aparelho copulador ou pênis. Quando em estado de repouso se recolhe no abdômen, porém, no ato do acasalamento (cópula) os órgãos sexuais do macho (genitália) se exteriorizam e, após a cópula, ficam presos na câmara de ferrão da rainha, provocando a morte do zangão. O sêmen com espermatozoides apresenta coloração amarelo marrom, e o muco, produzido pelas glândulas mucosas é de coloração branco leitoso.
¶ 3.2.6.2 Rainha
As rainhas possuem dois ovários, compostos por cerca de 300 a 320 ovaríolos. Os ovaríolos inicialmente são finos e vão se alargando, servem para conduzir os óvulos até os ovidutos. Possuem também dois ovidutos, que são a continuação dos ovários e se unem para formar o oviduto médio que se liga à vagina. A espermateca é constituída por uma bolsa de forma oval onde é armazenado o sêmen após a cópula. Isto indica que a fecundação do ovo ocorre por ocasião da postura da rainha que pode resultar em macho quando não é fecundado e fêmea quando é fecundado. A vagina é contínua ao oviduto mediano, e a espermateca se abre dorsalmente em sua extremidade anterior.
Há ainda a glândula espermática que se liga à espermateca por meio de um tubo e que serve para manter os espermatozoides viáveis durante toda a vida da rainha.
¶ 3.3 Organização social
Para Michener (1969), são reconhecidas as seguintes associações em abelhas: solitárias, subssociais, parassociais e eussociais.
¶ 3.3.1 Solitárias
Cada fêmea constrói e aprovisiona suas próprias células. Após a oviposição, a fêmea lacra o ninho e inicia a construção de outro. Geralmente a fêmea morre antes que a cria amadureça e emerja das células, não havendo contato entre as duas gerações.
¶ 3.3.2 Subssociais
As colônias desta categoria são fundadas por uma única fêmea que constrói, aprovisiona e realiza postura em suas próprias células. Assim como em abelhas solitárias, essas fêmeas também morrem antes do adulto emergir, entretanto, o aprovisionamento dessas células é feito de maneira progressiva, diferentemente do que ocorre nas primeiras.
¶ 3.3.3 Parassociais
Nesta categoria são incluídas as colônias pequenas, constituídas por uma única geração, nas quais há uma maior defesa da colônia. São classificadas ainda em três tipos: comunal, quase-social e semi-social. Nas comunais, grupos de fêmeas pertencentes a uma mesma geração convivem em um mesmo ninho, cada uma construindo, aprovisionando e ovipositando suas próprias células. Nas quase-sociais, ocorre um comportamento de colaboração entre estas fêmeas, a exemplo de quando uma fêmea começa um trabalho de construção ou aprovisionamento de uma célula e outra pode terminar, ou ainda quando algumas fêmeas, de forma cooperativa, constroem e aprovisionam uma célula. Porém, a oviposição é realizada apenas por uma das fêmeas. Nas semi-sociais, há uma ou mais fêmeas fecundadas que põem ovos e outras fêmeas com ovários não desenvolvidos e não fertilizados, porém, sendo de uma mesma geração.
¶ 3.3.4 Eussociais
A eussocialidade é definida por três características:
• Divisão de trabalho, com um sistema de castas envolvendo indivíduos estéreis ou não reprodutivos ajudando aqueles que reproduzem;
• Cooperação entre membros da colônia no cuidado aos jovens; e
• Sobreposição de gerações capazes de contribuir para o funcionamento da colônia.
A eussocialidade é restrita a todas as formigas e cupins, e a algumas abelhas e vespas. As A. mellifera e abelhas sem ferrão representam muito bem o comportamento de eussocialidade. Assim sendo, elas apresentam um sofisticado e complexo sistema de comunicação e orientação.
¶ 3.4 Comunicação e orientação das abelhas
¶ 3.4.1 Transferência de alimento
Nas abelhas A. mellifera, a comunicação pode ser feita por meio de sons, cheiros, danças ou estímulos eletromagnéticos. Porém, a transferência de alimento denominada de trofalaxis é uma das maneiras mais importantes de comunicação, uma vez que durante esse processo ocorrem também trocas de algumas secreções glandulares e propagação de feromônios (Figura 3.4). A trofalaxis funciona como elemento integrador dentro da colônia. O alimento é passado de operária para operária, assim como de operária para rainha, zangões e rainha para operária. Esse processo de troca de alimento pode informar a necessidade de néctar ou água, a qualidade e quantidade de néctar coletado, influenciar a postura, secreção de cera e armazenamento do mel.
O alimento, néctar ou mel regurgitado é transferido de uma abelha para outra pelo fato de uma delas pedir ou oferecer alimento. Rainhas, zangões e operárias pedem alimento, porém, geralmente ele só é oferecido pelas operárias. Existe uma tendência que o alimento seja passado das abelhas mais velhas (coletoras) que coletam esse alimento fora da colônia para as abelhas mais novas (receptoras). Dessa forma, a qualidade e quantidade do alimento coletado influenciam diretamente no processo de postura de ovos, cuidado das crias, do amadurecimento e do armazenamento do mel, da secreção de cera e da construção de favos.
.jpg)
¶ 3.4.2 Comunicação por danças
As operárias podem informar a distância e a localização exata de uma fonte de alimento, ou um novo local para nidificação do enxame. O cientista alemão Karl Von Frisch (1886-1982) descobriu e definiu o sistema de comunicação utilizado para informar sobre a localização da fonte de alimento, observando que as abelhas costumam realizar três tipos de dança: dança em círculo, dança do requebrado ou em forma de oito e dança da foice.
- Dança em círculo: Informa sobre fontes de alimento que estão a menos de cem metros de distância da colônia/enxame;
- Dança do requebrado: Usada para fontes de alimento que estão a mais de cem metros de distância. Nessa dança, a abelha descreve a direção e a distância da fonte;
- Dança da foice: Considerada uma dança de transição entre a dança em círculo e a do requebrado. É utilizada quando o alimento se encontra a cerca de cem metros da colônia/enxame.
As danças podem ser executadas dentro da colmeia, sobre um favo próximo a área de cria, sobre o enxame ou no favo próximo ao alvado. Durante a dança, por exemplo, a forrageira indica a direção da fonte de alimento em relação à posição da colmeia e do sol. A distância da colmeia até a fonte de néctar é informada pelo número de vibrações (requebrados) realizadas e pela intensidade do som emitido durante a dança. Quanto menor a distância entre a fonte e a colmeia, maior o número de vibrações. A forrageira pode interromper sua dança a curtos intervalos e oferecer às operárias que estão observando, o recurso coletado. Assim, ela informa as características do néctar, e as operárias partem em busca desta fonte. O recrutamento aumenta com a intensidade e a duração da dança.
¶ 3.4.3 Comunicação por feromônios
Feromônios são substâncias químicas produzidas por um indivíduo e geram respostas fisiológicas ou comportamentais específicas em outros indivíduos da mesma espécie. São eles o principal meio de comunicação química dentro do ninho. As glândulas exócrinas produtoras de feromônios localizam-se em diferentes partes do corpo, cada uma podendo produzir mais de um tipo de feromônio, cuja ação sobre o comportamento ou fisiologia do indivíduo receptor pode ser tanto individual como em conjunto. As glândulas alteram a quantidade dos componentes de um determinado feromônio em função das atividades desempenhadas na colônia e de acordo com a idade do indivíduo. Em abelhas esses feromônios são transmitidos pelo ar, contato físico ou alimento. Na Tabela 3.1 são apresentados os principais feromônios produzidos pelas abelhas e as reações desencadeadas por eles.
Tabela 3.1. Principais feromônios produzidos pelas abelhas e as reações desencadeadas.
| Feromônios | Função |
| Produzidos por operárias: | |
| Feromônio de trilha em abelhas sem ferrão | Orienta as operárias na localização do ninho e de fontes de alimento |
| Feromônio de alarme | Alerta as operárias para a presença de inimigo próximo à colmeia e repele as operárias de fontes sem disponibilidade de alimento. |
| Feromônio de defesa | Liberado por operárias durante a ferroada, atrai outras operárias para ferroarem o local. |
| Feromônio da glândula de Nasonov | Liberado na entrada da colmeia durante a enxameação, ajuda na orientação e no agrupamento das abelhas. |
| Produzidos por rainhas: | |
| Feromônio da glândula mandibular | Atrai zangões para o acasalamento, mantém a unidade da colônia/enxame, inibe o desenvolvimento dos ovários das operárias e a produção de novas rainhas. |
| Feromônio das glândulas epidermais | Atrai operárias. Age em sinergia com o feromônio da glândula mandibular. |
| Produzidos por zangões: | |
| Feromônio da glândula mandibular do zangão | Atrai rainhas e outros zangões para a área de congregação de zangões. |
| Produzidos por crias: | |
| Feromônio de cria | Estimula a coleta de alimento e inibe o desenvolvimento dos ovários das operárias. Permite que as operárias reconheçam idade, casta e estado de saúde das crias. |
Com base nas evidências pontuadas acima, fica claro que A. mellifera utiliza tanto o cheiro quanto a dança para se comunicar. Em abelhas sem ferrão, a comunicação ocorre, essencialmente, por meio de sinais sonoros e químicos (trilhas de cheiros) (LINDAUER e KERR, 1960; IMPERATRIZ-FONSECA et al., 2004).
¶ 4. MATERIAIS E EQUIPAMENTOS PARA APICULTURA E MELIPONICULTURA
Trabalhar com abelhas A. mellifera africanizadas exige a utilização de equipamentos de segurança para o apicultor ou profissional que irá manejar alguma colônia. Além disso, a utilização de determinados materiais e equipamentos possibilita a produção de diversos produtos apícolas e meliponícolas de forma eficiente e racional.
Para o manejo e inspeção em meliponários é dispensado o uso de fumigador e EPI que serão citados a seguir. Porém, mesmo sem poder ferroar, algumas abelhas se defendem com as mandíbulas e uso de EPI é recomendável. Como exemplos podemos citar as abelhas dos Gêneros Partamona e Scaptotrigona, que são muito defensivas.
¶ 4.1 Fumigador
O fumigador é o equipamento mais importante no manejo de abelhas africanizadas, sendo indispensável para o trabalho de campo. A não utilização do fumigador pode colocar em risco a segurança do apicultor, e de outras pessoas e animais próximos ao apiário.
É formado por um pequeno tambor com fundo, tampa e uma grelha interna que suspende a maravalha ou cepilho a ser queimado. Em um dos lados do fumigador existe um fole, que sopra o ar e na tampa fica localizada a abertura por onde ocorre a saída da fumaça (Figura 4.1).
A fumaça possui a função de desorganizar a estrutura da colônia a ser manejada. Quando a fumaça é direcionada na colmeia, as abelhas a interpretam como um risco iminente à integridade da colônia e, como tentativa de fuga, enchem a vesícula melífera com mel. Dessa forma, possuem maior dificuldade para dobrar o abdômen e ferroar o apicultor durante o manejo.
Durante qualquer manejo a ser realizado na colônia, a fumaça precisa estar fria e com a coloração branca. Sua utilização deve ser conduzida de forma constante e adequada, o que permite o melhor controle possível das abelhas. Características como fumaça quente e em pouca quantidade devem ser evitadas, pois podem gerar maior comportamento defensivo pelas abelhas. O excesso de fumaça pode asfixiar as abelhas ou até gerar o abandono da colmeia. Dependendo da origem do cepilho ou da maravalha, pode ocorrer algum tipo de intoxicação das abelhas ou do apicultor. Desta forma, recomenda-se uso de madeira não tratada.
¶ 4.2 Formão de apicultor
Esta é uma ferramenta de metal que permite a abertura da colmeia (Figura 4.2), e posteriormente, a retirada dos favos para a realização de diversos manejos, como revisão, extração de mel, troca de favos e inspeção dos quadros de cria. Em inspeções sanitárias, o formão deve ser limpo e desinfetado após a utilização em cada colônia.
_(pdf.io).jpg)
¶ 4.3 Equipamento de proteção individual
As vestimentas do apicultor (Figura 4.3) são consideradas equipamentos de proteção individual (EPI). Para qualquer manejo nas colônias de abelhas africanizadas é essencial sua utilização, mesmo se for um manejo rápido e sem abertura das colmeias.
Macacão: Deve ser de cor clara (cores escuras podem desencadear maior defensividade das abelhas). A qualidade do macacão varia de acordo com o material com o qual é confeccionado e, consequentemente, variam os preços de comercialização. Pode ser feito de brim (grosso) ou de materiais sintéticos (náilon, poliéster, albene, space/malha livre, etc.). Pode ser inteiro ou com duas peças (calça e a parte superior), com elásticos nas pernas e braços. A máscara pode fazer parte do macacão ou ser uma peça separada. Os modelos com máscara separada permitem uma melhor higienização por facilitar a lavagem. Alguns modelos de máscara precisam de chapéu, geralmente de palha, outros possuem uma armação que mantém as orelhas e nariz longes da tela. Mesmo utilizando tecidos resistentes, é mais seguro evitar muito contato com a pele, por isso recomenda-se utilizar um macacão com número maior do que normalmente seria utilizado como roupa comum pelo apicultor. Um avanço na apicultura brasileira foi o uso do tecido “space” conhecido como “malha livre” para confecção dos macacões pois a espessura do tecido não permite que o ferrão das abelhas alcance a pele, sendo este composto de camadas de tela em poliamida que permitem excelente ventilação, proporcionando segurança e conforto, sendo considerado 100% antiferroadas.
Luvas: Podem ser feitas de diversos materiais. Couro, napa e borracha, por exemplo, são materiais que garantem a segurança exigida no trabalho com as abelhas. Independente do material, é importante não perder a sensibilidade durante os manejos.
Botas: São recomendadas botas de borracha ou de couro, de cor clara e de cano suficientemente alto, protegendo o apicultor de possíveis ferroadas ou de animais peçonhentos que podem estar nas proximidades do apiário.
_(pdf.io).jpg)
¶ 4.4 Colmeia Langstroth
A colmeia Langstroth (Figura 4.4), padrão adotado pela Confederação Brasileira de Apicultura e Meliponicultura é dividida em tampa, ninho, melgueira, fundo e quadros (caixilhos), com suas especificações técnicas definidas pela ABNT NBR 15.713:2009, sendo o modelo mais adotado pelos apicultores.
_(pdf.io).jpg)
A confecção das colmeias exige que suas medidas sejam respeitadas rigorosamente, para que não ocorram problemas durante os manejos. Assim, não se recomenda que o apicultor produza suas colmeias, a menos que possua habilidade e equipamentos que permitam atender rigorosamente as especificações, especialmente em relação ao “espaço abelha”.
A colmeia Langstroth foi desenvolvida respeitando o chamado “espaço abelha”. Esse espaço físico deve estar presente entre as laterais e os quadros, tampa, fundo e entre os quadros, de forma a permitir a livre movimentação das abelhas. Dessa forma duas abelhas conseguem trabalhar de costas uma para outra, sem que uma comprometa o trânsito ou tarefa da outra. O espaço abelha deve ser de no mínimo 4.5 mm e, no máximo, 9,5 mm. Espaços menores em que as abelhas não conseguem patrulhar são normalmente isolados com própolis, mas se a colônia não for forte fica aberto e se torna refúgio para pragas como formigas, traças ou o pequeno besouro das colmeias.
As colmeias devem ser construídas com madeiras legalizadas (eucalipto, pinus, pau-d’arco, entre outros) e secas, pois, assim, haverá a garantia de caixas resistentes e livres de deformações. O apicultor usará a melgueira acima do ninho. Em algumas regiões com abundância de recursos, pode-se utilizar o sobreninho no lugar da melgueira, porém será mais pesado. Esses materiais são colocados acima do ninho para o armazenamento do mel. Por ser menor que o sobreninho, a melgueira facilita o trabalho durante a coleta do mel. O apicultor poderá acrescentar uma, duas ou mais melgueiras durante o manejo da safra, dependendo do volume de produção (Figura 4.5).
.jpg)
¶ 4.5 Colmeia para meliponíneos
As abelhas nativas sem ferrão são criadas em diferentes modelos de colmeias, a depender da espécie e região do Brasil. O modelo de colmeia que vamos apresentar é o modelo INPA, chamada assim por ter sido desenvolvido no Instituto Nacional de Pesquisas da Amazônia, e é um dos mais difundidos na meliponicultura nacional (Figura 4.6). A construção modular permite uma melhor separação entre a área de crias e os potes com mel, assim como torna o processo de divisão para formação de novas colônias mais rápido e menos destrutivo.
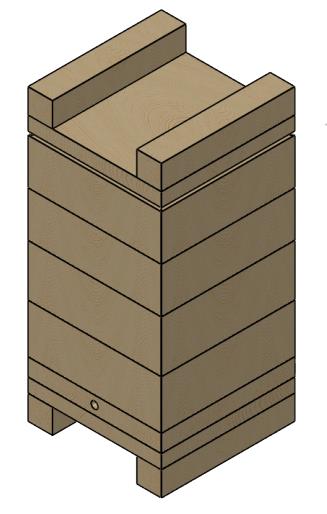
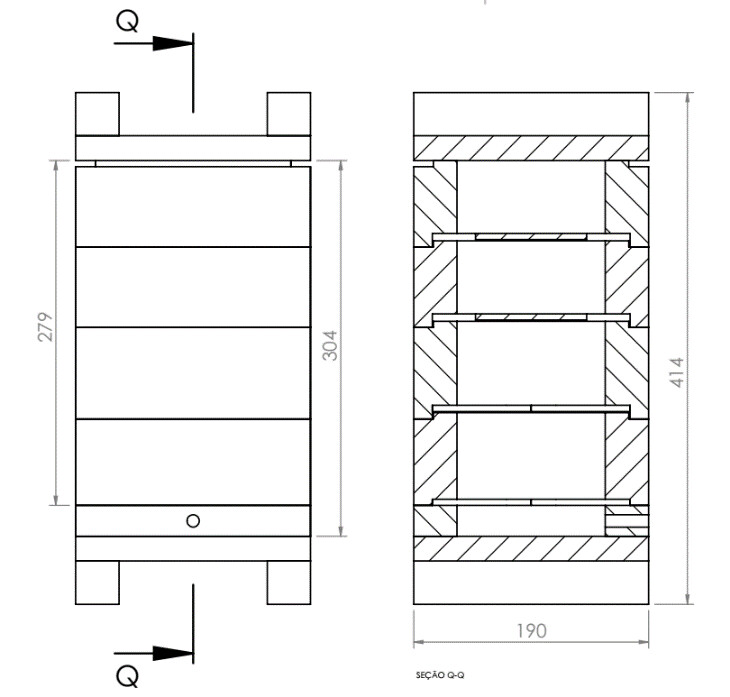
¶ 4.6 Cera alveolada
A cera de abelhas, na sua forma alveolada, com impressão da matriz dos alvéolos (Figura 4.7), serve para facilitar o início da construção dos favos pelas abelhas da colônia. Essa cera em lâminas pode ser comprada ou confeccionada pelo próprio apicultor, caso ele possua os equipamentos apropriados. Em seu manejo, o apicultor pode adotar a mistura de cera de abelhas com parafina ou cera de carnaúba, entretanto no processo de comercialização pode encontrar dificuldade na venda do produto. Caso queira trabalhar com ela pura, o apicultor deve realizar a compra em estabelecimentos idôneos.
A importação de cera de abelha deve seguir todos os requisitos sanitários, buscando mitigar o risco de entrada de pragas e doenças no Brasil. Alguns meliponicultores também utilizam a cera de abelhas A. mellifera para ajudar as abelhas nativas na construção de seus ninhos, devendo ter cuidado com sua origem, pois já foram constatadas em meliponíneos doenças que só eram relatadas em A. mellifera.
_(pdf.io).jpg)
¶ 4.7 Alimentadores
Os alimentadores servem para fornecer suplemento alimentar para as colônias e não são itens obrigatórios, mas apicultores que desejam atingir alta produtividade devem fazer uso desse equipamento nos períodos de baixa disponibilidade de recursos florais. No mercado existem vários modelos disponíveis, tanto para uso individual, como coletivos. Entretanto, não se recomenda os alimentadores coletivos por razões sanitárias. Os mais comuns são os individuais, como o modelo semi-interno Boardman (Figura 4.8), e os internos Doolittle (Figura 4.9), Alexander e de cobertura (Figura 4.10). O modelo utilizado pelos criadores de abelhas varia conforme a quantidade de colônias, custo, e tipo de manejo realizado.
_(pdf.io).jpg)
_(pdf.io).jpg)
_(pdf.io).jpg)
¶ 4.8 Material de limpeza e desinfecção
Para desinfecção dos materiais, é comum utilizar álcool 70%, podendo ser usado o lança-chamas (vassoura de fogo, Figura 4.11) para equipamentos não inflamáveis, como o formão de apicultor e colmeias. É necessário o uso de recipientes que permitam a limpeza e desinfecção dos materiais que serão colocados em contato com as colmeias, se atentando para o fato de que as que apresentarem algum sinal clínico devem ser examinadas por último, visando mitigar o risco de contaminação das colônias saudáveis. O serviço veterinário oficial deverá levar a campo luvas de procedimento (usadas por cima da luva de apicultor) para trocar entre colmeias inspecionadas.
.jpg)
¶ 4.9 Material para uso do Serviço Veterinário Oficial
As enfermidades que atingem as abelhas em vários países no mundo resultam em sérios problemas para a apicultura. Porém, no Brasil, com a presença das abelhas africanizadas, esse problema é minimizado devido a características próprias como a rusticidade dessas abelhas.
Para reconhecer os sintomas das doenças em colônias e coletar material adequado sob suspeita, é importante estar familiarizado com as características das diferentes fases do desenvolvimento das abelhas.
Antes de iniciar a coleta de amostra, deve-se realizar uma observação minuciosa dos favos e ter conhecimento dos materiais necessários para a realização da coleta das amostras. É importante ressaltar que sempre se deve utilizar formão, facas e pinças devidamente desinfetados, entre colônias e entre apiários. Os materiais devem ser lavados com água e sabão, realizando esfregação mecânica e, em seguida submergir em álcool 70%.
Os materiais para coleta e envio de amostras a serem utilizados pelo serviço veterinário oficial são descritos no Manual Veterinário de colheita e envio de amostras: manual técnico. Capítulo 4: ABELHAS Apis mellifera Cooperação Técnica MAPA/OPAS PANAFTOSA Saúde Animal do Brasil. Disponível em: https://www.gov.br/agricultura/pt-br/assuntos/sanidade-animal-e-vegetal/saude-animal/programas-de-saude-animal/ManualdecolheitadeamostrasABELHAS.pdf
Para auxiliar na preparação do atendimento às notificações de suspeitas de doenças de abelhas de controle oficial, foi elaborado checklist disponibilizado no Anexo I deste documento.
Demais recomendações de procedimentos que podem ser adotados pelo Serviço Veterinário Oficial, visando minimizar o risco de transmissão de doenças por meio de produtos de abelhas e métodos de desinfecção de materiais relacionados aos apiários, podem ser encontrados no Código de Animais Terrestres da OIE (https://www.oie.int/en/standard-setting/terrestrial-code/).
¶ 5. BOAS PRÁTICAS DE PRODUÇÃO E MANEJO DE IMPORTÂNCIA PARA A SAÚDE DAS ABELHAS
O conjunto das melhores técnicas ou procedimentos para realizar determinada atividade é chamado de “boas práticas de produção” ou BPP, e visam à segurança na condução de um processo produtivo, com aplicação de princípios higiênicos e sanitários. Para a atividade de criação de abelhas, serão descritas neste capítulo as práticas reconhecidas e recomendadas que estão diretamente relacionadas à saúde das colônias, sejam A. mellifera ou meliponíneos, de maneira a prevenir ou controlar pragas e doenças.
A criação de abelhas e obtenção de seus produtos podem ser divididas em três setores que são trabalhados em locais distintos pelo criador. O primeiro local é a sede, onde todo material é preparado para ir ao campo, o segundo é o próprio apiário ou meliponário, enquanto o terceiro é chamado de área limpa, no qual os produtos são processados e encaminhados para comercialização. Em cada lugar ou setor se realizam atividades com cuidados específicos, sendo importante esse tipo de divisão para ter um controle higiênico sanitário eficiente. Neste capítulo iremos discorrer sobre esses locais como “Setores I, II e III”, como descrito no esquema abaixo:
.jpg)
¶ 5.1 Setor I – Sede, oficina e estoque
É o local onde o apicultor ou meliponicultor armazena, limpa e prepara as colmeias. Normalmente é constituído por um barracão ou por um anexo na própria residência, que, muitas vezes, situa-se em área urbana.
Os documentos relacionados à atividade, anotações como controle de estoque, fichas de campo, livro-diário, notas fiscais de compra e venda, manual de boas práticas, devem ali ser cuidadosamente guardados. Nesse local deve haver um ambiente para derreter cera, limpar e desinfetar as colmeias, armazenar ingredientes e utensílios para o preparo de alimentação das abelhas, assim como disponibilidade de água potável. O controle de pragas deve ser rigoroso e o dimensionamento do ambiente dependerá da quantidade de colmeias que o apicultor e/ou meliponicultor dispõe, e se planeja expandir a atividade.
- Separação e armazenamento de materiais: as colmeias, tanto para abelhas A. mellifera como para abelhas sem ferrão, constituem os principais materiais desse setor e devem ser separadas conforme seu estado e origem. Colmeias prontas para ir a campo limpas e desinfetadas não podem estar armazenadas junto às colmeias que vieram do campo para limpeza, em virtude de envolver perda das abelhas por motivos nem sempre conhecidos.
As melgueiras com favos prontos são normalmente armazenadas para reutilização na próxima safra. Portanto, esses favos devem ser isentos de cria e pólen estocado, para evitar a proliferação de pragas como o pequeno besouro das colmeias -PBC (Aethina tumida). A traça da cera pode se multiplicar nesses favos e provocar prejuízos diretos como a perda da cera e favos. Pode, também, redundar em perda indireta de rendimento, devido ao tempo investido para limpeza dos caixilhos (quadro onde o favo é construído) que tiveram os favos danificados, em alguns casos até os caixilhos de madeira podem ser perfurados pelas larvas da traça da cera (Galleria melonella e Achroia grisella).
Favos novos, que só tiveram uso para estoque de mel, são menos susceptíveis ao ataque da traça da cera, sendo recomendado separar os favos novos de favos mais antigos e escurecidos. Para conservação dos favos, o armazenamento deve proporcionar ventilação e luminosidade, inibindo o desenvolvimento das traças da cera, sendo uma ótima alternativa para criadores que possuem poucas melgueiras. Para apicultores com grande quantidade de material pode ser necessário uso de técnicas como a fumigação com enxofre, não sendo recomendado o uso de produtos químicos à base de fosfeto de alumínio, que é percursor da fosfina, pois são altamente tóxicos para abelhas.
- Limpeza e desinfeção de materiais: As colmeias, mesmo quando novas, devem ser limpas e desinfetadas. A limpeza normalmente é feita com o uso da espátula para raspar o material orgânico aderido e escova ou vassourinha. Essas ferramentas devem ser limpas com frequência e especialmente quando usadas em colmeias que foram habitadas por abelhas que morreram ou abandonaram por motivos não esclarecidos. Nesse caso, o material deve ser limpo e desinfectado com álcool 70%. Para a desinfecção das colmeias é recomendado o uso de vassoura de fogo para fundo, tampa e corpo da colmeia, os caixilhos podem ser fervidos em água ou limpos com o uso de derretedores de cera à vapor.
- Processamento da cera: Na apicultura a cera é um dos principais insumos, porém pode conter patógenos ou resíduos químicos (contaminantes). Colmeias recolhidas do campo sem abelhas, ou favos de abelhas capturadas sem origem conhecida, com suspeita de doenças, ou apresentando sinais de contaminação por agrotóxicos, devem ter sua cera descartada ou processada separadamente para comercialização com finalidade fora da apicultura ou meliponicultura. A depender da doença, a cera pode ser reutilizada na apicultura, desde que tenha um processamento adequado de acordo com as recomendações do Código de Animais Terrestres da OIE.
- Armazenamento e preparo de suplementação alimentar para as abelhas: A principal matéria-prima utilizada na suplementação alimentar das abelhas é o açúcar. Por isso, todo açúcar utilizado para esse fim deve ser de boa procedência, não sendo recomendado o uso de açúcar de varredura, uma vez que pode conter resíduos do controle de pragas aplicado nas usinas e locais de distribuição. Na formulação e preparo de alimentação para suprir a carência por pólen são utilizados ingredientes proteicos, como por exemplo, o extrato de soja e levedura de cerveja, que assim como o açúcar, devem ser adquiridos de fornecedores idôneos, registrados nos órgãos de fiscalização.
Os ingredientes devem ser armazenados em local protegido da luz solar, seco, ventilado e suspenso do solo. Os utensílios para o preparo e transporte do alimento devem ser de fácil higienização, que não liberem substâncias tóxicas, odores e sabores. O local de preparo deve também ser de fácil higienização para evitar riscos de contaminação, seja por meio físico, químico ou biológico. O processo de limpeza dos equipamentos e utensílios deve ser feito com água e sabão neutro e a desinfecção com solução sanitizante de iodo (2%) ou hipoclorito de sódio (1% em contato por 10 minutos) conforme descritos por Nascimento et al. (2010).
O uso de produtos das abelhas como ingredientes no preparo do alimento deve ser evitado. A exceção é quando os ingredientes são do mesmo produtor, pois o mel e o pólen podem conter contaminantes e levar doenças para outra colônia ou apiário. Para aumentar a durabilidade do alimento pronto pode se trabalhar com menor teor de umidade no produto acabado e, se possível, armazenar em ambiente refrigerado. Não se recomenda o uso de conservantes ou medicamentos de qualquer natureza no preparo do alimento para as abelhas.
¶ 5.2 Setor II – Apiários e/ou meliponários
A escolha do local de instalação dos apiários e meliponários, assim como as atividades ali realizadas, devem seguir alguns princípios que fazem parte do conjunto de boas práticas para promover a saúde das abelhas.
- Apiário e/ou meliponário de triagem: é uma área destinada à quarentena de colônias adquiridas de outras regiões, de origem incerta (captura de enxames longe dos apiários/meliponários conhecidos pelo criador) ou com suspeita de doenças e pragas. Essa área é uma recomendação de boas práticas para mitigar a propagação de pragas e doenças. Deve ser instalado em local afastado dos demais e com registro de entrada e saídas de colônias.
- Escolha do local do apiário ou meliponário: Na escolha do local deve se observar a presença de água potável disponível para as abelhas em até, no máximo, 200 metros de distância, sombreamento parcial (nos horários mais quentes do dia), solo limpo, seco e firme, disponibilidade de plantas que oferecem recursos como néctar e pólen em quantidade, qualidade e diversidade, facilidade de acesso, e, no caso de apiários, uma distância de pelo menos 500 metros de casas, animais e estradas, por questões de segurança de pessoas e animais. O local deve estar distante dois quilômetros de fábricas de doces ou engenhos de cana-de-açúcar, como boa prática relacionada à qualidade do mel.
- Cadastro do apiário e/ou meliponário no órgão executor de sanidade animal: Para instalar um apiário ou meliponário em propriedade de terceiros, é necessária autorização do proprietário, e o cadastro na unidade veterinária local – UVL ou no escritório de atendimento à comunidade - EAC, no município onde se localiza a propriedade rural e para meliponários com mais de 50 colônias ou que comercialize colônias ou partes dela é também necessário cadastro no órgão ambiental conforme Resolução Conama nº 496, de 19 de agosto de 2020. Essa formalização é considerada uma boa prática na produção, pois o criador de abelhas é reconhecido pelo proprietário da área onde estão situadas suas abelhas e facilita a atuação do serviço veterinário oficial para verificação de eventuais problemas sanitários.
É importante destacar que o cadastro é obrigatório, conforme a legislação sanitária vigente, para todos os produtores rurais. Mesmo para os produtores que não comercializam a produção em entrepostos, ou não transportam colônias, o cadastro deve estar atualizado de forma a viabilizar as atividades de defesa sanitária.
- Limpeza do apiário e/ou meliponário: O local escolhido deve ser mantido limpo, resíduos de favos ou colmeias vazias devem ser removidos para limpeza, devendo permanecer apenas colmeias e melgueiras limpas prontas para uso. Não usar herbicidas para limpeza do local do apiário, porque estes podem permanecer como resíduos nos produtos da colônia (mel, cera, própolis).
- Controle de movimentação: Quando verificada a suspeita de doenças de controle obrigatório, deve ser suspendida a movimentação animal. No caso de infestação por Aethina tumida, por exemplo, o transporte de colmeias ou suas partes (povoadas ou não) e de abelhas rainhas oriundas de apiários infestados pode ser proibido a critério do OESA. Todos os carregamentos de melgueiras (ou sobrecaixas) com mel devem ser envoltos em tela com malha de 2mm ou menos.
- Manejo de colônias de abelhas: Ao chegar ao apiário ou meliponário, o criador de abelha deve realizar uma primeira avaliação geral observando os alvados (entrada da colmeia), verificando possíveis anormalidades com base no comportamento da espécie de abelha. Essa primeira avaliação irá determinar a sequência de abertura das colmeias, devendo deixar por último as com sinais de debilidade, evitando assim contaminar as colônias saudáveis.
Para as colônias de A. mellifera o uso de fumaça é fundamental para o manejo adequado e deve ser utilizada logo após a primeira observação do alvado. O material de combustão utilizado no fumigador deve ser limpo, livre de contaminantes e que não lance fagulhas. Uma técnica comum para fortalecer colônias fracas é trocá-las de lugar com colônias fortes do mesmo apiário. Esse procedimento, assim como transferir favos ou discos de cria, só deve ser feito se estas não apresentarem sintomas de doenças (descritas nos próximos capítulos) com risco de propagar doenças ou pragas para as demais colônias.
Como as colônias fracas são mais susceptíveis a doenças e pragas, a padronização do plantel faz parte das boas práticas para promover a sanidade na criação de abelhas. A união de colônias fracas é também uma excelente opção, formando uma única colônia, que será mais produtiva e resistente (NOGUEIRA-COUTO e COUTO, 2006). Uma prática importante é a troca de favos velhos e escuros por lâminas de cera alveolada, retirada de favos com crias com suspeita de doenças e substituição periódica das rainhas (anualmente). Se as rainhas forem importadas devem ser acompanhadas da certificação veterinária internacional, emitida pelo país exportador.
As colmeias vazias devem ser retiradas do apiário, limpas e desinfectadas para o repovoamento. Deve-se evitar colmeias com buracos e frestas, respeitar o espaço abelha, de maneira que elas possam patrulhar e remover qualquer praga, raspar periodicamente o acúmulo de própolis e de cera na tampa, nas molduras dos quadros, paredes e fundo das colmeias.
- Alimentação: A alimentação é fornecida às abelhas como forma de suprir a ausência ou baixo suprimento de néctar ou pólen na colônia, devido à escassez natural em algumas épocas do ano. Quando falta néctar, a demanda por energia deve ser suprida com xarope de água com açúcar. A concentração do xarope está relacionada à fermentação do mesmo, que ocorre mais rápido quanto menor o teor de açúcares (menos concentrado). A fermentação pode afetar a saúde das abelhas e provocar diarreia. Esse tipo de alimentação pouco concentrada deve ser fornecido em quantidades proporcionais ao tamanho da população de abelhas, para que não fiquem sobras até o dia seguinte. Eventuais sobras devem ser removidas e o alimentador limpo e desinfectado, caso o alimento esteja fermentado ou se forem observadas abelhas mortas.
A alimentação em forma de xarope só deve ser fornecida para colônias em desenvolvimento e manutenção, e quando não estão com melgueiras, evitando assim que as abelhas misturem esse xarope com o mel. Para garantir a pureza pode ser necessário retirar esse alimento quando estocado em excesso nos favos do ninho e da melgueira se eventualmente for deixada sobre uma colônia que está sendo alimentada.
O uso do xarope em alimentadores coletivos pode colaborar com a disseminação de doenças e parasitas, sendo seguro apenas para apiários isolados, com o plantel reconhecidamente livre de doenças. Para as abelhas nativas sem ferrão ainda não se conhece o impacto que alimentadores coletivos podem ocasionar na saúde, pois além de colônias manejadas, é comum um mesmo meliponicultor possuir mais de uma espécie de abelha. Portanto, alguma enfermidade que não apresenta risco para a saúde de uma determinada espécie pode acabar apresentando grande impacto em outras espécies.
Alimentação proteica pastosa deve ser oferecida em local com espaço suficiente para que as abelhas patrulhem, cobrindo toda a superfície. As sobras devem ser retiradas, devendo ser fornecida apenas uma quantidade equivalente ao consumo.
¶ 5.3 Setor III – Extração e preparo de produtos das abelhas para comercialização
Este local deve ser projetado respeitando-se as normas e legislação para estabelecimentos de extração e beneficiamento de produtos das abelhas, descrito no Decreto N° 9.013, de 29 de março de 2017 (BRASIL, 2017). O serviço veterinário oficial deve atentar, principalmente, para as melgueiras que aguardam processamento, e para o tratamento de opérculos resultantes da desoperculação dos favos para extração do mel.
A filtragem do mel deve ser feita utilizando peneiras com malhas de diferentes tamanhos. A peneira mais fina deve ser capaz de reter ovos de A. tumida, com malha não superior a 0,42 mm (OIE, 2019). Além disso, para controle do A. tumida o resíduo da filtragem do mel deverá ser tratado imediatamente com procedimentos que possam assegurar a sua completa desinfestação. Recomenda-se o congelamento em temperatura igual ou inferior à -12º C, pelo período mínimo de 24 horas ou qualquer procedimento de eficácia equivalente, reconhecido pela autoridade veterinária.
Pólen, Geleia Real e Própolis: Para evitar a propagação de A. tumida nestes produtos, congelar no mínimo de 2 a 5 dias à temperatura abaixo de zero grau.
Cera: deverá ser processada termicamente – derretida – antes de ser usada novamente, para inviabilizar possíveis ovos de A. tumida.
Extração do mel: Após a colheita, a extração do mel deve ser feita com a maior brevidade possível. Após a extração, os quadros devem ser devolvidos para as colônias, evitando-se a exposição desse material sem a devida vigilância das abelhas. A cera dos opérculos deve ser fundida imediatamente após a extração do mel. As instalações devem ser mantidas sempre limpas, sem resíduos de mel, cera, abelhas mortas e outros produtos do apiário.
Mesmo após a filtragem algumas impurezas podem permanecer no mel, por isso é muito importante deixar o produto em decantação por cinco a sete dias. Como o mel apresenta alta densidade, as impurezas irão acumular-se na parte de cima, facilitando sua retirada.
¶ 6. DOENÇAS E PRAGAS NA APICULTURA E MELIPONICULTURA
Assim como os demais seres vivos, as abelhas criadas racionalmente na apicultura e meliponicultura também estão sujeitas a doenças, que podem acometer as abelhas em fase de cria (larvas e pupas) ou adultas. A gravidade das doenças e os sintomas dependem do agente causal. De modo geral, as doenças que atingem as crias não provocam danos diretos às abelhas adultas, porém, o contato das abelhas adultas com o agente causador pode se tornar fonte de contaminação, disseminando a doença para as demais colônias do apiário (WIESE, 1995).
As abelhas sociais são os insetos mais estudados no mundo devido sua importância socioeconômica e ambiental. A relevância desses insetos no agronegócio e na manutenção dos ecossistemas naturais ocasionou sua distribuição em diversas regiões do mundo, contribuindo para a propagação das doenças (MARTIN et al., 2020). O nível de susceptibilidade das abelhas às doenças varia de acordo com diversos parâmetros, tais como: estado nutricional da colônia, período do ano, subespécie, seleção natural das populações, presença de agroquímicos no ambiente, entre outros. Os principais agentes causadores de doenças nas abelhas são as bactérias, fungos e vírus. Grande parte das doenças podem ser propagadas por meio dos equipamentos e produtos da colônia, como mel, cera, favos, entre outros.
No Brasil, os critérios para que as doenças sejam classificadas pela legislação sanitária como de notificação oficial estão relacionados com a necessidade de intervenção oficial para realização do diagnóstico, investigação ou atendimento de medidas previstas em normas estabelecidas pelos programas oficiais do MAPA, visando o controle ou erradicação das doenças alvo da vigilância. Nessas categorias estão enquadradas as doenças exóticas ou erradicadas no país, doenças que estão sujeitas a programas oficiais de vigilância e doenças de ocorrência esporádica em zonas limitadas do país.
Por outro lado, algumas doenças de abelhas são endêmicas no país, e seu impacto na produção e saúde animal podem ser gerenciados em nível local com uso de medidas sanitárias e de manejo pelos produtores, não havendo normas federais específicas de intervenção oficial ou determinação de ação do SVO para diagnóstico ou investigação.
Ressaltamos que a definição das doenças alvo de vigilância pelo MAPA não deve ser uma barreira para que os Estados implantem programas de vigilância complementares para doenças com importância local para a produção de abelhas. Essa decisão deve ser tomada pelos gestores em nível estadual, uma vez que as condições para a apicultura e meliponicultura podem ser muitos diversas em cada bioma do nosso país. Esta preocupação é ainda mais relevante para a meliponicultura, que está intimamente ligada à região de origem das abelhas nativas e, portanto, representa um universo com grande variação em território nacional.
Para proporcionar um melhor entendimento sobre as principais enfermidades, serão abordadas separadamente as doenças que afetam as crias (larvas e pupas) e as abelhas adultas, em seguida, pragas e parasitas.
¶ 6.1 Bactérias, fungos e vírus
¶ 6.1.1 Doenças da fase de cria (larvas e pupas)
As doenças que acometem as crias prejudicam o desenvolvimento da colônia, uma vez que, dependendo da gravidade da doença, a população da colônia será comprometida. As doenças das crias matam as larvas ou inibem seu desenvolvimento, afetando o indivíduo no estágio de larva ou de pupa, conforme o agente. O desequilíbrio populacional, além de prejudicar a produção, pode ocasionar a mortalidade da colônia.
¶ 6.1.1.1Cria pútrida europeia ou loque europeia
A cria pútrida europeia – CPE ou loque europeia (European foulbrood – EFB, na sigla em inglês) é uma doença causada pela bactéria anaeróbica gram-positiva Melissococcus plutonius, que acomete as crias de abelhas A. mellifera. Sua ocorrência é de notificação obrigatória e imediata de qualquer caso suspeito de acordo com as normas sanitárias nacionais vigentes. Teixeira et al. (2020) observaram sintomas da doença e identificaram a bactéria em colônias de abelhas Melipona spp. no estado do Espírito Santo, causando prejuízo ao desenvolvimento da colônia e mortalidade nos casos mais severos.
No ano de 2020 foram iniciados 6 atendimentos de ocorrências de Loque Europeia pelo Serviço Veterinário Oficial com registro no e-SISBRAVET, nos Estados de São Paulo e Bahia. Porém, sabe-se que a doença é endêmica e está distribuída em todo o território nacional.
O nome comum da doença se deve ao fato de que as larvas infectadas são acometidas por infecções secundárias de outras bactérias que causam odores desagradáveis, tais como Enterococcus faecalis e Paenibacillus sp. (ARAI et al., 2012). O ciclo da vida da bactéria M. plutonius é bastante semelhante ao ciclo de vida da bactéria que provoca a loque americana, por isso, os sintomas dessas doenças costumam ser confundidos pelos apicultores (MUELLER et al., 2019).
A M. plutonius chega até as larvas por meio da alimentação (ELLIS, 2008). Quando as abelhas nutrizes entram em contato com alimento contaminado e utilizando esse mesmo produto para alimentar as larvas, as bactérias presentes nesse alimento podem acabar contaminando as larvas. A bactéria, por sua vez, aloja-se no intestino médio das larvas, competindo pelos mesmos nutrientes. A falta de nutrientes provoca redução do peso larval e sua morte.
As colônias fortes e populosas normalmente conseguem remover as larvas com sintomas de infecção por M. plutonius antes de se tornar um problema generalizado. Contudo, colônias com baixa população ou baixa taxa de comportamento higiênico podem acabar apresentando problemas mais graves da doença.
Os principais sintomas observados nas larvas infectadas são mudanças na coloração e posição irregular dentro do alvéolo. As larvas saudáveis são brancas, enquanto as larvas com loque europeia apresentam coloração que varia do amarelo claro até marrom (Figura 6.1). Além disso, as larvas podem ter aspecto flácido, desidratado, encolhida e/ou com sistema traqueal evidente (TOMKIES et al., 2008). O odor gerado pela presença de saprófitos pode ser ácido, semelhante ao vinagre ou até mesmo não apresentar odores específicos, dependendo o grau da infecção (OIE, 2018).
_(pdf.io).jpg)
Em nível macroscópico, um dos sintomas de infecção por M. plutonius é a cria falhada ou salteada (alvéolos sem cria) no favo. Isso ocorre porque as larvas sintomáticas não são operculadas pelas abelhas operárias (MUELLER et al., 2019). No entanto, somente a cria falhada não pode ser utilizada para determinar a infecção por loque europeia, uma vez que outras doenças ou problemas na colônia também podem ocasionar falhas nas áreas de cria.
O serviço veterinário oficial, durante a investigação a campo, pode usar como ferramenta para direcionar sua suspeita o teste do palito de madeira. Nesse teste, utiliza-se um palito de madeira ou qualquer material que possa ser inserido e retirado do opérculo contendo a larva com sintomas. O palito de madeira ou similar deve então ser levemente mexido para entrar em contato com a larva e retirado lentamente do alvéolo. Se a larva apresentar aspecto pegajoso possivelmente a contaminação se deu por loque americana e não por loque europeia (SHIMANUKI, 1997).
Caso o teste do palito apresente resultado positivo para loque americana, é imprescindível o diagnóstico laboratorial para confirmação, uma vez que infecções por outras bactérias secundárias podem apresentar resultado falso positivo no teste do palito. O diagnóstico laboratorial pode ser realizado por meio de isolamento da bactéria, detecção do antígeno, microscopia, PCR (polymerase chain reaction) ou Real-time PCR (OIE, 2019).
Não há uma forma de prevenção totalmente eficiente para evitar a infecção das colônias pela bactéria M. plutonius. Porém, é recomendado sempre manter a assepsia do ferramental e do local de trabalho, limpando frequentemente com água e sabão os materiais e equipamentos utilizados no cotidiano do apiário. Adicionalmente, recomenda-se realizar seleção de colônias com bom comportamento higiênico e, principalmente, manter colônias fortes e populosas por meio das boas práticas apícolas. Também é recomendável eliminar os favos contendo cria doentes (como descrito no capítulo anterior).
¶ 6.1.1.2 Cria pútrida americana ou loque americana
A cria pútrida americana – CPA ou loque americana (American foulbrood – AFB, na sigla em inglês) é uma doença causada pela bactéria gram-positiva Paenibacillus larvae (anteriormente denominada Bacillus larvae). A loque americana é uma doença altamente contagiosa e de difícil tratamento, por isso sua ocorrência é de notificação obrigatória e imediata de qualquer caso suspeito de acordo com as normas sanitárias nacionais vigentes.
A doença loque americana, até há alguns anos considerada exótica no país, possui status perante à Organização Mundial de Saúde Animal - OIE de “doença suspeita, porém não confirmada e limitada a uma ou mais zonas”, uma vez que foram detectados em laboratório esporos da bactéria em mel de prateleira coletado no varejo, porém sem correlação com sinais clínicos em apiários.
Da mesma forma que a loque europeia, a loque americana é transmitida, principalmente, pelas abelhas nutrizes ao alimentar as larvas com alimento contaminado (LINDSTROM et al., 2008). A gravidade da CPA ocorre porque cada larva infectada morta pode deixar bilhões de esporos da bactéria (SPIVAK e REUTER, 2001). Além disso, os esporos podem permanecer viáveis hibernando na sua forma de resistência (endósporo) por décadas (Hasemann, 1961), até as condições ficarem favoráveis ao seu desenvolvimento no trato digestivo das larvas.
As principais formas de propagação dos esporos da loque americana ocorrem por meio da enxameação, pilhagem (Figura 6.2) e troca de favos de uma colônia com outras por parte do apicultor (DATTA et al., 2013). Uma das maiores dificuldades em relação a CPA é que os sintomas da doença se tornam visíveis quando uma grande quantidade de pupas mortas não são removidas, transformando-se em escamas, momento em que os esporos já se encontram na fase de resistência ou endósporo (STEPHAN et al., 2020), que é a fase de contaminação de larvas sadias.
.jpg)
A maioria das ocorrências de loque americana foi registrada em países onde a criação de abelhas A. mellifera de subespécies europeias são predominantes, que geralmente apresentam menor comportamento higiênico quando comparada às abelhas africanizadas. No caso da infecção por loque americana, foi observado que somente a remoção das pupas sintomáticas pelas abelhas operárias não foi suficiente para eliminar a doença, devido à grande formação de esporos (GENERSH, 2010). Gillard et al. (2008) observaram que 25% das colônias infectadas com P. larvae com formação de esporos não são diagnosticadas, o que aumenta o risco de dispersão da doença.
A loque americana provoca grande impacto econômico em apiários comerciais devido à letalidade da doença para as colônias (EBELING et al., 2016), uma vez que as pupas morrem de acordo com a progressão do agente infeccioso (STEPHAN et al., 2020). A alta mortalidade das pupas diminui a quantidade de população de abelhas adultas na colônia e, consequentemente, pode acarretar o colapso e morte da colônia. A virulência da CPA depende diretamente do genótipo da bactéria (OIE, 2018).
A campo, o serviço veterinário oficial, pode utilizar o teste do palito de madeira para direcionar a suspeita de loque americana (Figura 6.3). Inserindo-se o palito ou material similar no alvéolo contendo as pupas sintomáticas e retirando o conteúdo lentamente, se ele apresentar aspecto pegajoso (esticado acima do alvéolo) significa um forte indício de contaminação por P. larvae, que deve ser confirmado por meio de análises laboratoriais.
.jpg)
Os demais sintomas da doença são semelhantes aos provocados pela loque europeia. Contudo, na infecção por loque americana as larvas morrem em um estágio mais tardio de desenvolvimento, até mesmo depois de operculadas (WIESE, 1995), por esta razão para realizar o teste do palito é na maioria das vezes necessário remover o opérculo (Figura 6.4). Os esporos de P. larvae entram no intestino médio das larvas por meio da alimentação contaminada e somente conseguem atravessar o epitélio do intestino larval no estágio pré-pupa. Ao sair do intestino a bactéria ingressa na hemolinfa e prolifera formando milhões de esporos, matando a pupa e aumentando a propagação da doença (YUE et al., 2008).
.jpg)
¶ 6.1.1.3 Cria giz
A cria giz é uma das doenças que acomete as crias das abelhas (ARONSTEIN e MURRAY, 2010) e pode causar prejuízos ao desenvolvimento da colônia, produção apícola e polinização (NIE et al., 2020). A doença é causada pelo fungo heterotálico Ascophaera apis, tendo sido primeiramente descrito infectando abelhas da espécie A. mellifera e, posteriormente, em abelhas Apis cerana e Xylocopa sp. (CHEN et al., 2018).
Da mesma forma que a CPE e CPA, a contaminação pelo fungo A. apis ocorre via alimentação larval contaminada com esporos. O fungo infesta o intestino médio da larva competindo pelos nutrientes, provocando a morte da larva por desnutrição. Após a morte da larva, o fungo se alimenta dos órgãos internos da larva, deixando-a desidratada com aspecto mumificado, com aparência de giz (FLORES et al.; 2005). Os mesmos autores verificaram que o escurecimento da larva após a morte indica que ocorreu a formação dos esporos do fungo.
FLORES et al. (1996) concluiu que as larvas no 5° instar (etapas dos estágios larvais, delimitado pelo período entre duas mudas) são as mais susceptíveis à infecção. Como há formação de esporos, o manejo de favos entre uma colônia e outra e o contato com qualquer material contaminado podem auxiliar na propagação da doença para outras colônias (HEATH, 1982).
Os sintomas clínicos da doença são crias com aspectos mumificados, bem como cria falhada (alvéolos vazios nos favos de cria). Em casos de crias infectadas durante a operculação do alvéolo, ao sacudir o favo é possível escutar um barulho lembrando um chocalho, devido ao fato de as larvas secas baterem contra as paredes do alvéolo (Figura 6.5). Em colônias com alta taxa de comportamento higiênico, é possível observar as crias infectadas removidas no alvado ou no solo abaixo deste (Figura 6.6). O diagnóstico laboratorial é realizado em microscopia, onde é possível observar o micélio do fungo.
Normalmente, a letalidade da cria giz é baixa em colônias higiênicas, embora a presença do fungo provoque uma queda na quantidade de crias (ARONSTEIN et al., 2010). A doença deve ser controlada por meio da aplicação de boas práticas apícolas, uma vez que não existem medicamentos aprovados/registrados para uso em apicultura no Brasil.
No Brasil os primeiros surtos de cria giz ocorreram em Botucatu/SP, em 1997 (ROCHA et al, 1998), e em São Gabriel/RS, em 1998 (SATTLER et al, 1998), com repercussão na produção apenas no primeiro ano. Nos anos seguintes, foram relatadas ocorrências esporádicas em apiários de apicultura migratória no Rio Grande do Sul, mas sem qualquer expressão econômica na atividade, fenômeno que pode ser atribuído à maior resistência das abelhas africanizadas.
.jpg)
.jpg)
¶ 6.1.1.4 Cria ensacada
A cria ensacada é uma doença causada pelo vírus anteriormente chamado de Morator aetatulas, que afeta as larvas da colônia (BAILEY, 1969). Em inglês é conhecido pela siga SBV (sacbrood virus), constituído por uma fita simples de RNA. Foi o primeiro vírus identificado em abelhas Apis mellifera (WHITE, 1917), atualmente a espécie é chamada de Sacbrood vírus, do gênero Iflavirus da família Iflaviridae conforme classificação específica para vírus do ICTV - International Committee on Taxonomy of Viruses (ICTV, 2020).
Nas larvas, o vírus impede o desenvolvimento, ocasionando a morte do indivíduo antes da fase de pupa (BAILEY, 1975). Nas abelhas adultas, embora não apresente sintomas clínicos, Anderson e Gibbs (1989) observaram redução na longevidade de abelhas infectadas pelo vírus. As larvas infectadas apresentam coloração amarelada até marrom escuro (BAILEY, 1975).
A propagação do vírus pode ocorrer na troca de favos entre colônias, enxameação e pelo contato entre as abelhas adultas da colônia (YONGSAWAS et al., 2020), sendo que o vírus pode sobreviver por até quatro semanas em ambientes propícios como pólen e mel (JIN et al., 2020). O vírus já foi encontrado tanto em abelhas A. mellifera quanto em abelhas A. cerana, contudo a virulência é muito mais severa nas abelhas asiáticas.
O principal sintoma é a cria com aspecto de ensacada (Figura 6.7) e pode ser confundida com a cria ensacada brasileira (CEB), doença também conhecida como mal de outono ou mal do barbatimão. No entanto, a CEB não é causada por vírus, e sim por toxinas encontradas em pólen de algumas espécies de plantas, como o barbatimão (Stryphnodendron sp.) e o falso barbatimão (Dimorphandra mollis), por exemplo. A toxina (grupo dos taninos) presente no pólen dessas espécies impede que as larvas cheguem à fase de pupa.
.jpg)
¶ 6.1.2 Doenças da fase de adulto
São diversas doenças que podem acometer as abelhas adultas e seus sintomas podem ser confundidos entre uma doença e outra, ou até mesmo com intoxicações.
¶ 6.1.2.1 Nosemose
A nosemose é uma doença causa pelos fungos microsporidia Nosema apis e N. ceranae, cujos sintomas a campo são diferentes e o nível de infecção é sazonal. As técnicas de microscopia e análise molecular permitem distinguir as espécies de Nosema (Figura 6.8).
Embora o mecanismo de ação seja semelhante, as espécies de fungos causam prejuízos à colônia de forma diferente. A N. apis diminui a longevidade das abelhas operárias e aumenta a taxa de mortalidade na entressafra (FRIES, 1993), enquanto a N. ceranae provoca queda da população de abelhas adultas e morte da colônia em regiões onde as temperaturas são mais elevadas ( HIGES et al., 2008).
O nível de infecção por nosemose é avaliado pela quantidade de esporos por abelha ( OIE, 2019). No entanto, alguns autores evidenciaram ser mais preciso avaliar a quantidade de abelhas infectadas na colônia ( BOTÍAS et al., 2011).
Em regiões de clima temperado o nível de infecção por N. apis apresenta-se baixo no verão, aumentando gradativamente no outono e inverno, com rápido aumento durante a primavera devido à maior quantidade de abelhas emergidos (FRIEST et al.; 2013). Com relação à infecção em áreas de clima tropical, o nível se mantém baixo ao longo do ano (FRIES et al., 2003), possivelmente devido às temperaturas mais elevadas. Enquanto os níveis de infecção por N. ceranae apresentam menor variação ao longo do ano (Higes et al., 2008).
Assim como loque europeia e loque americana, a infecção por nosemose ocorre no trato digestivo devido à alimentação contaminada com esporos. Contudo, os esporos de Nosema se desenvolvem melhor no intestino de abelhas com mais de 15 dias de vida. Ao entrar no organismo do hospedeiro, os esporos danificam a parede epitelial do intestino, dificultando a digestão e absorção dos nutrientes da dieta. O principal sintoma da dificuldade de assimilação alimentar é a diarreia (FRIES, 2010). Portanto, em colônias com alta infecção por Nosema apis é comum observar fezes no interior da colmeia e no alvado (Figura 6.9), não sendo observado nas infecções por N. ceranae.
.jpg)
¶ 6.1.3 Doenças Causadas por vírus
As doenças causadas por vírus não são de notificação oficial, porém as principais serão brevemente abordadas neste manual, para o conhecimento de seus sinais clínicos pelo Serviço Veterinário Oficial. Existem mais de 20 vírus identificados que podem acometer as abelhas Apis mellifera, no entanto, no Brasil foram identificados os vírus, APV (sigla em inglês para o vírus da paralisia aguda), DWV (sigla em inglês para o vírus das asas deformadas), BQCV (sigla em inglês para o vírus da realeira negra), CWV (sigla em inglês para o vírus das asas opacas), IAPV (sigla em inglês para o vírus da paralisia aguda israelense), e FV (sigla em inglês para o vírus filamentoso) (MESSAGE et al., 2011).
¶ 6.1.3.1 Vírus da paralisia aguda
Acute paralysis virus (APV da sigla em inglês), é conhecido como vírus da paralisia aguda. Foi descoberto em 1963 por Bailey et al. em testes laboratoriais. No entanto, não há relatos de doenças ou mortalidade de abelhas devido à presença do vírus nas abelhas. Geralmente sua presença na colônia está diretamente relacionada à alta taxa de infestação por V. destructor (BÉKÉSI et al., 1999).
¶ 6.1.3.1 Vírus das asas deformadas
O vírus das asas deformadas é conhecido pela sigla DWV, do inglês deformed wing vírus. Pertencente ao gênero Iflavirus, família Iflaviridae e ordem Picornavirales (TANTILLO et al., 2015). Esse vírus afeta tanto as abelhas melíferas quanto o ácaro Varroa destructor, que atua também como vetor, transmitindo o vírus para outras abelhas e colônias. O ácaro V. destructor parasita as pupas e essas, ao emergirem, já apresentam as asas atrofiadas, reduzindo sua longevidade e capacidade de trabalho (Figura 6.10).
Shen et al. (2005) observaram que 70% das pupas são naturalmente infectadas pelo DWV ou outros vírus. A presença do vírus em grande quantidade (BOWEN-WALKER et al., 1999) está associada com sintomas de má formação das asas de abelhas Apis mellifera durante a fase de pupa, geralmente em colônias com alta taxa de infestação V. destructor (BAILEY e BALL, 1991). Além disso, reduz a longevidade das abelhas infectadas, geralmente sendo inferior a 48 horas (DE MIRANDA e GENERSH, 2010). Entre os demais vírus, o DWV é responsável pelos maiores danos à colônia (FRANCIS et al., 2013).
.jpg)
¶ 6.1.3.3 Vírus da realeira negra
O vírus da realeira negra é conhecido pela sigla BQCV, do inglês Black queen cell vírus. Em alguns países, é o principal causador de morte prematura em pupas de abelhas rainhas, deixando-as com coloração negra (ANDERSON, 1993). O BQCV pertence ao gênero Cripavirus da família Dicistroviridae (TANTILLO et al., 2015).
O BQCV foi descoberto em larvas e pupas de abelhas rainhas (BAILEY e WOODS, 1977), sendo comumente encontrado em colônias de abelhas infestadas por N. apis (ALLEN e BALL, 1996). O vírus é constituído por 8.550 nucleotídeos em uma fita simples de RNA (LEAT et al., 2000).
¶ 6.1.3.4 Vírus das asas opacas
O cloudy wing virus, em inglês, ou vírus das asas opacas é frequentemente observado em colônias extremamente fracas devido à alta infestação por V. destructor. Ainda é pouco estudado e nem sempre os sintomas são visíveis. Acomete principalmente as abelhas adultas, incluindo a rainha e os machos, porém sua presença também foi confirmada nas larvas e pupas (BAILEY e BALL, 1991).
¶ 6.1.3.5 Vírus israelense da paralisia aguda
O vírus israelense da paralisia aguda é conhecido pela sigla IAPV, do inglês Israeli acute paralysis virus. Sua classificação está dentro da ordem Picornavirales e família Dicistroviridae (MAORI et al., 2007). Os sintomas ainda não foram definidos em nível de indivíduos ou até mesmo em nível de colônia, sendo observada alta virulência somente em laboratório quando uma grande carga viral é colocada diretamente sobre as pupas ou sobre os adultos (DE MIRANDA et al., 2010; BAILEY e BALL, 1991).
¶ 6.1.3.6 Vírus filamentoso
O vírus filamentoso, também conhecido como “A. mellifera filamentous vírus (AmFV)” em inglês, é o único vírus descrito até o momento em abelhas que possui fita dupla de DNA. A transmissão na colônia ocorre tanto pela troca de alimento entre os indivíduos, comportamento conhecido como trofalaxis, bem como pela transmissão direta da rainha para os ovos (HARTMANN et al, 2015). Uma das alterações observadas em laboratório é a lipólise do tecido gorduroso das abelhas infestadas, enquanto um dos sinais clínicos é a presença de abelhas rastejando próximo ao alvado da colmeia (CLARK, 1977). Contudo, apesar da infestação pelo AmFV ter sido confirmada em diversos países, raramente está associado à perda de colônias (SITAROPOULOU et al., 1989).
¶ 6.2 Ácaros, lepidópteros, coleópteros e dípteros
As abelhas podem ser afetadas por diferentes pragas e parasitas. A acariose, varroose, aetinose e tropilaelapsose são consideradas doenças segundo a OIE e podem causar prejuízo econômico aos apicultores. Pragas como formigas não são inimigos específicos das abelhas, mas podem atacar e causar prejuízos, assim como outros animais que oportunamente atacam as colônias não serão abordados nesse manual.
¶ 6.2.1 Acariose
A acariose ocorre por infestação de abelhas A. mellifera pelo endoparasita Acarapis woodi, descrito primeiramente na ilha Wight na Inglaterra (RENNIE,1926). Este ácaro que vive nas traqueias torácicas das abelhas onde completa seu ciclo reprodutivo é encontrado em todos os continentes, com exceção da Oceania (SAMMATARO et al., 2013).
O ciclo de vida do parasita inicia com a entrada do A. woodi na traqueia das abelhas adultas jovens, onde se alimenta da hemolinfa e se reproduz (Figura 6.11 e 6.12). O ácaro perfura o epitélio traqueal e suga a hemolinfa, causando uma série de problemas, tais como: diminuição do fluxo de ar (MORISON, 1927), infecções secundárias devido aos danos ao epitélio (BAILEY, 1965), danos à musculatura das asas (Schneider, 1941) e liberação de toxinas provocando paralisia (MORGENTHALER, 1944). O contágio ocorre por meio do contato físico entre uma abelha infestada com as demais abelhas da colônia (SAMMATARO et al., 2000).
No Brasil, os primeiros relatos da presença do ácaro A. woodi em colônias de abelhas africanizadas foram apontados por Nascimento et al. (1971). Peixoto et al. (2020) realizaram um estudo para verificar a presença do ácaro em colônias de abelhas africanizadas em 15 estados brasileiros e nenhum deles apresentou a presença do parasita. No Japão, Sakamoto et al. (2020) observaram que o A. woodi não representa um problema para as abelhas A. mellifera, mas para outras espécies, como a A. cerana japônica, a infestação do ácaro pode se tornar um problema grave.
O principal sintoma da infestação por A. woodi são as asas disjuntas com dificuldade para voar. Geralmente as abelhas sintomáticas ficam no alvado da colmeia ou rastejam sobre os favos (BAILEY, 1985). O diagnóstico somente pode ser confirmado por meio da análise das traqueias em microscópio ótico, pois os sintomas clínicos podem ser confundidos com outras doenças ou intoxicações, e a visualização do ácaro no campo é impossível de se realizar a olho nu.
.jpg)
.jpg)
90
¶ 6.2.2 Tropilaelapsose
A infestação por ácaros do gênero Tropilaelaps provocam a tropilaelapsose. Os ácaros desse gênero são parasitas naturais das abelhas gigantes asiáticas Apis dorsata, Apis breviligula e Apis laborisosa, convivendo em equilíbrio com o hospedeiro, sem causar grandes prejuízos (ANDERSON e ROBERTS, 2013).
Após a introdução das subespécies de abelhas europeias A. mellifera pelos apicultores na Ásia, o ácaro se propagou para as colônias desta espécie (DAINAT et al., 2009) e se tornou uma preocupação iminente devido à possibilidade desse ácaro se propagar em nível global e causar enormes prejuízos econômicos como a Varroa. Isso porque o ciclo de vida de ambos os parasitas é semelhante, em que a fêmea acasalada invade um alvéolo de cria ainda não operculada e, após a operculação, inicia a oviposição e alimentação a partir da hemolinfa do hospedeiro (ANDERSON e ROBERTS, 2013).
No momento da emergência da abelha parasitada, os descendentes do ácaro fêmea deixam o alvéolo para invadir outras crias (WOYKE, 1994). Fora do alvéolo o período de sobrevivência do ácaro é de apenas um ou dois dias (WOYKE, 1984). No entanto, a quantidade de Tropilaelaps sp. encontrados em colônias infestadas geralmente é maior do que a população de Varroa destructor (ANDERSON e MORGAN, 2007).
Tanto os danos físicos causados pelo Tropilaelaps sp. quanto V. destructor representam portas de entrada para infecções e vírus (MIRANDA et al., 2013). Porém, de acordo com Khongphinitbunjong et al. (2015) o principal prejuízo à saúde da colônia devido à infestação por Tropilaelaps sp. é causada pelo próprio ácaro.
Atualmente o ácaro se encontra somente em países do continente asiático e o risco de sua dispersão para outros continentes é baixo devido ao curto período de sobrevivência do ácaro nas abelhas adultas (ANDERSON e ROBERTS, 2013). Portanto, por meio da enxameação é pouco provável que o ácaro Tropilaelaps sp. chegue a qualquer país das Américas (Figura 6.13). A tropilaelapsose é uma doença de notificação obrigatória imediata diante de qualquer caso suspeito, segundo as normas sanitárias vigentes no Brasil.
.jpg)
¶ 6.2.3 Varroose
Atualmente é uma doença existente em todo o mundo, considerada como impossível de se erradicar, que causa os maiores e mais graves prejuízos para apicultura mundial (CAP, 2007). O ácaro Varroa destructor encontrado no Brasil (anteriormente classificado como Varroa jacobsoni) é um parasita de abelhas adultas e de suas crias a partir da fase de pré-pupa. O gênero Varroa compreende quatro espécies de ácaros ectoparasitários obrigatórios, sendo eles Varroa jacobsoni, V. destructor, V. underwoodi e V. rindereri. Esses ácaros são os responsáveis pelo quadro conhecido como varroose (ANDERSON e TRUEMAN, 2000).
Em alguns países de clima temperado e frio o desenvolvimento desse parasita pode ser letal, diferentemente do que ocorre em algumas áreas tropicais, a exemplo o Brasil, onde as abelhas africanizadas desenvolveram mecanismos de tolerância ao ácaro Varroa destructor (MEDINA e MARTIN, 1999 ; TORRES e BARRETO, 2013).
Ramsey et al. (2019) demonstraram uma visão diferente da aceita até agora, em que o ácaro penetra as membranas intersegmentais para ingerir a hemolinfa. Os novos estudos relatam que o parasita não consome hemolinfa, mas gordura corporal (corpo adiposo), que se caracteriza como um tecido análogo ao fígado de mamíferos.
Esses novos estudos sugerem que o ácaro Varroa está explorando o corpo gorduroso como sua fonte primária de sustento. Podem se alojar entre a esclera abdominal em abelhas adultas e as vezes também podem ser encontrados entre a cabeça e tórax da abelha. Para a reprodução, o ácaro tem preferência por células de cria de zangões comparativamente às células de cria de operárias, pois as larvas dos zangões são maiores e permanecem mais tempo operculadas para completar o desenvolvimento, o que garante uma maior disponibilidade de alimento para os ácaros.
A fêmea fundadora do ácaro entra nas células pouco antes de serem operculadas. Após dois a três dias da operculação, a fêmea fundadora deposita seus primeiros ovos, que geralmente, produzem machos. Decorrido um intervalo de um a dois dias, até sete ovos são postos na célula de abelha operculada e, geralmente, são ovos que produzem fêmeas. Das ninfas que eclodem, uma pequena porcentagem completa o desenvolvimento, apenas duas a três chegam à fase adulta.
O número de parasitas aumenta constantemente com o crescimento da população de abelhas, especialmente no final do verão, quando os primeiros sinais clínicos de infestação podem ser reconhecidos. O ciclo biológico do ácaro depende da temperatura, da umidade e da população de abelhas adultas na colônia, que pode ser seriamente danificada pelos ácaros parasitas.
As abelhas infestadas e as crias que foram invadidas por apenas um ácaro parasita apresentam efeitos nocivos como mudanças no comportamento, redução da longevidade e aumento da suscetibilidade a doenças. Se mais de um ácaro invadir a célula de cria para realizar sua reprodução, o parasitismo se torna crítico. Apenas na fase letal, que antecede ao colapso das colônias, aparecem os sinais clínicos, tais como asas encolhidas e abdome encurtado (Figura 6.14).
.jpg)
O ácaro fêmea é de cor marrom-avermelhada escuro e tem corpo achatado e oval de aproximadamente 1,1 mm × 1,5 mm (Figura 6.15). É um parasita comum das abelhas melíferas que pode ser visto a olho nu (Figura 6.16). Geralmente os ácaros são visíveis sobre as abelhas adultas, comumente encontradas no tórax (fase forética).
.jpg)
.jpg)
Ao emergirem dos alvéolos as abelhas apresentam-se muitas vezes com as asas deformadas, menores e de peso mais baixo. Os quadros de cria apresentam-se com o aspecto em mosaico ou com a disposição dos opérculos de cria não uniforme, com espaçamentos entre eles. Cria fechada com um rasgo na borda do opérculo ou furo no centro pode indicar infestação pelo ácaro Varroa, embora esse sinal também possa indicar que a cria está morta.
O diagnóstico para varroose consiste na observação do ácaro adulto sobre o corpo das operárias quando revisamos favos de cria (Figura 6.17). Dependo do grau de infestação, as varroas podem ser observadas no fundo da colmeia.
.jpg)
O problema pode ser analisado de forma quantitativa, que consiste na inferência da taxa de invasão e da taxa de infestação por ácaros. Esse tipo de análise deve ser realizada em pelo menos três colônias, ou em 10% das colônias do apiário, escolhidas de forma aleatória.
Métodos para fazer a contagem de varroas nas colônias:
- Teste de invasão: Seguindo o método proposto por Gonçalves et al. (1981), consiste em desopercular os alvéolos e retirar as pupas de operárias de dentro desses e proceder à contagem do número de ácaros presente nesta célula (Figura 6.18). Desopercular cerca de 100 alvéolos, sendo 50 de cada lado do favo, obtendo-se a porcentagem de invasão para se ter uma ideia aproximada do estado da colônia. O processo de diagnóstico é eficaz e não ocasiona grandes consequências para a colônia.
.jpg)
- Teste de infestação:
Coleta de amostra de abelhas utilizando álcool para desprender as varroas das abelhas: Coloque álcool a 70% em um frasco plástico de 500 ml com tampa (cerca de 1/3 da capacidade do frasco), e adicione 5 gotas de detergente; colete entre 100 e 300 abelhas jovens que estejam aderidas a três quadros de cria diferentes; numere o frasco, identificando a colônia da qual as abelhas foram coletadas; feche o frasco, realize agitação mecânica por aproximadamente dois minutos para que os ácaros se desprendam do corpo das abelhas; separe os ácaros das abelhas com a ajuda de uma tela ( ̴5x9 mm); conte o número de abelhas e de ácaros e anote.
Coleta de amostra de abelhas quando se utiliza água quente para desprender as varroas do corpo das abelhas: Coloque água fria em um frasco de 500 ml com tampa (no mínimo 1/3 da capacidade do frasco); colete no mínimo 150 abelhas jovens que estejam aderidas a três quadros de cria diferentes; numere o frasco, identificando a colônia da qual as abelhas foram coletadas; em outro local tranquilo, substitua a água fria do pote por água quente, com um volume que atinja, no mínimo, 2/3 do pote; feche o frasco, agite um pouco e espere no mínimo 10 minutos para os ácaros se desgrudarem das abelhas; agite o frasco e separe os ácaros das abelhas com a ajuda de uma tela ( ̴5x9 mm) ou retire as abelhas do pote com o auxílio de uma pinça ou outro objeto; conte o número de abelhas e anote no papel; conte os ácaros e anote no papel.
Cálculo: A utilização de um pano branco facilita a visualização das varroas. Para encontrar a porcentagem de infestação com varroa, conta-se o número de ácaros, divide-se pelo número de abelhas e multiplica-se por 100.
Exemplo: Foram contados 22 ácaros e 271 abelhas.
Cálculo:
Porcentagem de infestação = (22 ÷ 271) x 100 = 0,0811 x 100 = 8,11
Portanto a infestação é de 8,11%.
O índice considerado tolerável de infestação de varroa é menor que 10%, pois não foi relatado prejuízo econômico até este nível. Na entressafra, aceita-se até 7% em abelhas operárias, sendo de 3% na safra. A seleção genética de colônias com alto comportamento higiênico permite manter baixas taxas de infestação.
Para infestações menores que 10% não é recomendado tratamento. Antes de decidir pela aplicação de produtos para o controle, deve-se avaliar no apiário os fatores que podem estar contribuindo para o aumento da infestação.
Alguns apicultores costumam utilizar produtos listados para apicultura orgânica, na tentativa de controlar a infestação do ácaro. Em sua maioria esses produtos podem atuar por via de contato e por evaporação, por exemplo: ácido oxálico, ácido fórmico, mentol, timol, cianol, entre outros. Mesmo sendo produtos orgânicos, se mal utilizados podem causar problemas, deixando resíduos no mel ou causando efeitos tóxicos para as abelhas e para o apicultor, se em contato direto com a pele no momento do preparo ou da aplicação do produto e se ocasionalmente inalado. A utilização desses produtos pode mascarar a doença e dificultar a seleção genética de linhagens de abelhas mais resistentes ou com maior taxa de comportamento higiênico.
Como medidas de prevenção trocar os favos velhos (escuros) por lâminas de cera alveolada completas; substituir as rainhas no máximo a cada dois anos, dando preferência por rainha nova e selecionada com bom comportamento higiênico; na divisão de colônias, utilizar quadros de cria oriundos de colônias com alta produtividade e livres de pragas e doenças; instalar o apiário em local com boa incidência de sol nas colmeias no período de inverno; não instalar apiários em locais úmidos e muito sombreados e em épocas de pouca florada nutrir as abelhas com alimento proteico.
¶ 6.2.4 Traça da cera
As traças são insetos da ordem Lepidoptera, que compreendem duas espécies: Galleria mellonella (traça maior) e Achroia grisella (traça menor). São as principais destruidoras das ceras velhas e escuras. Os indivíduos adultos das duas espécies depositam ovos nos favos ou em pequenas frestas dos quadros e caixas, principalmente em colônias enfraquecidas por doenças, perda da rainha ou má nutrição. Podem se desenvolver dentro das colmeias, bem como em favos estocados.
As larvas de traça possuem cor branca, com a cabeça castanha (Figura 6.19). Preferem favos mais escuros, pois contém maior quantidade de nutrientes, devido aos restos de pólen ou de larvas de abelha. O seu crescimento é rápido, deslocando-se para os cantos dos quadros ou das caixas onde tecem seu próprio casulo para completar seu desenvolvimento (Figura 6.20). Os prejuízos ocorrem com a passagem das larvas pelo interior dos favos, alimentando-se de cera, pólen e mel, construindo ao longo dos favos galerias com fios de seda.
.jpg)
.jpg)
Dependendo do grau de infestação, as larvas das traças destroem os favos, danificam a madeira da caixa e dos quadros, podendo afetar diretamente as crias, com a presença de quadros cobertos com grande quantidade de fios de seda e fezes. As colônias fracas com poucas abelhas ou caixas/colmeias construídas com medidas incorretas que não respeitam o espaço abelha de 0,6 a 0,9 cm, dificultam a passagem das abelhas para fazer a limpeza, principalmente entre os caixilhos e a tampa, e entre as laterais do caixilho e a parede da caixa, favorecendo a infestação.
O controle químico não é recomendado, uma vez que os produtos utilizados podem deixar resíduos na cera, os quais poderão ser transferidos para o mel. Desse modo, recomenda-se a adoção de medidas de manejo preventivas. Manter sempre colônias fortes no apiário; reduzir o alvado em épocas de entressafra e de frio; não deixar colmeias vazias (não habitadas) nem restos de cera no apiário; construir as caixas dentro das medidas padrão; se encontrar foco de infestação nas colônias, derreter os favos afetados (Figura 6.21); trocar periodicamente os quadros com cera velha; nas colônias com baixa população retirar as melgueiras com favos vazios no período de inverno; armazenar favos ou lâminas de cera em locais bem arejados, com claridade e, se possível, protegidos com tela, evitando armazenar favos velhos que são preferidos pelas traças; temperaturas abaixo de 7ºC também ajudam no controle; se observadas colônias que frequentemente apresentam alta infestação da traça, deve-se realizar a substituição de rainhas, visando aumentar a resistência. Portanto, a forma mais eficaz para prevenir os estragos provocados pela traça é manter colônias fortes, pois as abelhas de colônias fortes conseguem remover as larvas de traça e reparar os estragos provocados nos favos, à medida que vão surgindo.
.jpg)
¶ 6.2.5 Pequeno Besouro das Colmeias - PBC / Aetinose
O pequeno besouro das colmeias – PBC, Aethina tumida (Murray, 1867), foi oficialmente registrado no Brasil no ano de 2016 no Estado de São Paulo, em seguida Rio de Janeiro, Mato Grosso do Sul, Minas Gerais, Paraná e Goiás. É uma praga recente no Brasil e devido a sua facilidade de dispersão e adaptação é de notificação obrigatória e imediata de qualquer caso suspeito, de acordo com as normas sanitárias nacionais vigentes.
O ciclo da postura dos ovos até a emergência do indivíduo adulto leva entre 3 a 12 semanas. A cópula ocorre dentro da colônia, onde a fêmea realiza a postura dos ovos dispostos em aglomerações, em locais protegidos como nas bordas dos quadros, em frestas ou rachaduras das caixas, dentro dos alvéolos de cria ou de mel. Este comportamento dificulta a identificação, pois os ovos do besouro são bem menores que os ovos das abelhas, sendo de difícil visualização. As fêmeas podem colocar de 1.000 a 2.000 ovos numa única colmeia durante o seu ciclo reprodutivo (Figura 6.22).
.jpg)
Após a eclosão, as larvas se alimentam de cria de abelhas, pólen e mel (Figura 6.23). Ao final da fase larval, estas saem da colmeia e penetram no solo para realizarem o processo de empupamento, geralmente ao redor da colmeia, a uma profundidade média de 10 a 20cm (Figura 6.24). No solo os insetos completam seu ciclo biológico emergindo como besouros adultos, que assim retornam às colmeias atraídos pelo cheiro dos produtos da colônia. Os adultos podem viver por até seis meses e voar em média por até 10 Km para infectar novas colônias.
_(pdf.io).jpg)
_(pdf.io).jpg)
Os adultos, dentro da colmeia, se alimentam das crias das abelhas, mel e pólen. Fora da colmeia, alternativamente podem se alimentar de frutas. As larvas adicionam secreções próprias causando a fermentação do pólen e do mel, o qual se decompõe e se transforma em uma massa viscosa, que transborda dos alvéolos com um cheiro característico de laranja podre. Em dias quentes o mel pode escorrer pelo alvado da caixa devido à sua viscosidade mais baixa em decorrência dos processos fermentativos.
A larva é branco-amarelada e pode ser facilmente confundida com a larva da traça. No entanto, é possível a distinção entre ambas. A larva do A. tumida tem três pares de pernas muito finas, logo depois da cabeça, apresentando fileiras de espículas ao longo do dorso e duas longas espículas no final do mesmo.
O besouro adulto é de coloração castanho escuro a preto, sendo de cor clara quando emergem da pupa e tem o tamanho aproximado de 6mm, aproximadamente um terço do tamanho da uma abelha operária (Figura 6.25). Possuem antenas características da espécie, com formato em sua extremidade de pequenas esferas. Suas asas anteriores (élitros) são menores que o abdômen, tornando-se visível a parte terminal do mesmo. Podem ser vistos facilmente a olho nu, porém existem outras espécies de besouros bastante parecidos com os quais podem ser confundidos, necessitando de uma análise mais detalhada realizada em laboratório. Geralmente os besouros são encontrados nos cantos e/ou no fundo da colônia, ou andando sobre os favos ou na tampa das colmeias.
_(pdf.io).jpg)
Podem causar grandes prejuízos nos apiários, especialmente em condições favoráveis de clima para o desenvolvimento do besouro; enxames fracos podem ser acometidos afetando a sua estrutura e organização; podem destruir os favos de mel, pólen e crias da colônia, além de provocar a fermentação do mel já estocado e principalmente, diminuindo a imunidade da colônia. A infestação pode se tornar incontrolável, levando à destruição de colônias e apiários, já que a propagação desse besouro é reforçada pelo trânsito de abelhas, trânsito das colmeias e colônias, por meio de enxames, pelos favos de mel, pela cera, pela importação irregular de rainhas e pelo próprio equipamento do apicultor.
A identificação de suspeitas é feita através da inspeção visual cuidadosa na tampa, nos favos, área de cria, fundo, frestas, laterais da colmeia e outros locais escuros, buscando identificar o besouro adulto ou as larvas. Em caso de suspeita, o Serviço Veterinário Oficial deve realizar a coleta dos adultos e larvas e encaminhar para diagnóstico na rede laboratorial oficial do MAPA. Em alguns casos, não serão encontradas larvas, o que não comprometerá a realização do exame diagnóstico, que pode ocorrer somente a partir de indivíduos adultos. Quando a infestação da colmeia é pequena, a inspeção visual deve ser ainda mais cuidadosa para que se consiga observar os ovos, larvas e adultos, que se movimentam com grande agilidade, buscando esconderijos em cantos escuros das colmeias.
O tratamento deve ser mecânico, com limpeza e retirada das larvas e besouros. Evitar caixas úmidas, podres, com rachaduras e fendas que possam servir de local de abrigo para a sobrevivência do besouro. Em casos positivos, coletar o besouro (Figura 6.26), condicionando-o em frasco limpo e bem fechado contendo álcool 70% (até cobrir os besouros e/ou larvas), alternativamente, pode-se colocar o frasco em congelador, sem álcool, para viabilizar posterior confirmação. O acionamento do Serviço Veterinário Oficial deve ser feito de forma imediata, caso a coleta do material para diagnóstico tenha sido realizada pelo próprio apicultor ou meliponicultor.
_(pdf.io).jpg)
Para realizar a verificação da presença do coleóptero nos apiários, diversos tipos de armadilhas têm sido adotadas. O modelo mais simples é o de plástico corrugado, com orifícios de 4 mm, cortado em tiras medindo 7,5 x 50cm. Nessas armadilhas, os besouros adultos entram nos pequenos “túneis” do corrugado (Figura 6.27), em busca de proteção e abrigo, ficando fora do alcance das abelhas. As armadilhas são retiradas para verificação após 24 a 72 horas (Figura 6.28). Havendo a presença do besouro em armadilhas, acondicionar as armadilhas com os besouros em saco plástico transparente hermeticamente fechado e armazenar em freezer por 10 horas para que ocorra a morte dos besouros e possíveis larvas presentes, evitando desta forma sua disseminação.
_(pdf.io).jpg)
_(pdf.io).jpg)
Para controlar a infestação pelo Aethina tumida é necessário que os produtores rurais implantem ou reforcem em seus apiários e meliponários as boas práticas, que consistem em:
- Uso de macacão de apicultor completo e roupas claras para que o apicultor não transporte o PBC em suas roupas para outros apiários sem perceber;
- Após uso dos equipamentos no apiário revisar e acondicionar em bolsa bem fechada para limpeza cuidadosa;
- Realizar a substituição de favos velhos periodicamente, especialmente os quadros com pólen velho;
- Manter as colônias fortes e com bastante cria; o xarope do alimentador deve ser removido caso esteja fermentado ou com abelhas mortas;
- Realizar o manejo de inspeção das colônias regularmente, observando atentamente, principalmente em frestas na tampa, nas laterais, no fundo, nos quadros e favos para detectar a presença ou não do besouro;
- Realizar movimentação legal observando normas oficiais para o transporte de abelhas para qualquer finalidade e em qualquer local;
- Manter rainhas jovens com boa postura (de preferência com até um ano de idade);
- Buscar a melhoria da genética dos apiários com abelhas que apresentem um bom comportamento higiênico e maior resistência a pragas e doenças;
- Raspar periodicamente o acúmulo de própolis e de cera na tampa (figura 6.29), nas paredes, fundo das colmeias e molduras dos quadros, que podem servir de abrigo para o besouro;
- O apiário deve ser mantido limpo e deve ser instalado em local de solo seco. As caixas devem ficar sobre cavaletes para permitir a ventilação e iluminação nas horas mais frescas do dia;
- As colmeias devem estar em bom estado, pois o besouro pode se esconder em rachaduras e frestas, quando não povoadas devem ser retiradas do apiário e sua cera deve ser fundida;
- Após a extração do mel, todos o equipamento deve ser higienizado e os opérculos devem ser fundidos.
- Novas colônias e materiais devem ser adquiridos de áreas não infestadas;
- Informações adicionais podem ser consultadas na Nota Técnica e Ficha de Campo de Aethina tumida disponíveis no sítio eletrônico do MAPA.
_(pdf.io).jpg)
¶ 6.2.6 Piolho da abelha
Popularmente conhecido como piolho da abelha, o Braula coeca é uma espécie pertencente à família Braulidae que, embora seja um díptero, durante o processo de evolução perdeu seu par de asas e se comporta como um comensal nas abelhas A. mellifera (Figura 6.30). O piolho parasita instala-se no tórax das abelhas e alimenta-se diretamente dos órgãos bucais da hospedeira, com preferência pela rainha da colônia. Essa mosca é comumente confundida com o ácaro Varroa, mas com o auxílio da microscopia é possível diferenciá-los pelo número de pares de pernas.
_(pdf.io)_(1).jpg)
Causam desconforto e irritação sobre o corpo das abelhas parasitadas. Pode ocorrer contaminação do mel com a presença larvas do piolho, pois as fêmeas do parasita podem ovipositar nos alvéolos ainda não operculados de mel.
Para identificar se há a presença desses parasitas, deve-se retirar uma amostra de abelhas adultas, da mesma maneira como descrito para varroatose, e identificar o piolho (braquícero) em exame direto por microscopia. As implicações da utilização de produtos químicos como meio de controle desse parasita são as mesmas já descritas para controle de Varroa.
¶ 6.2.7 Forídeo
Os forídeos são pequenas moscas pertencentes à ordem Diptera, da família Phoridae (Figura 6.31), sendo a principal espécie que causa danos às abelhas a Pseudohypocera kerteszi (Enderlein, 1912). São insetos oportunistas que invadem as colônias de abelhas e depositam seus ovos, especialmente em colônias fracas, quando há excesso de pólen nos favos e poucas abelhas para defesa. A ocorrência de forídeos também é comum quando é fornecida alimentação proteica em excesso e a população de abelhas é pequena para fazer a defesa da colônia e consumir a proteína no prazo máximo de 15 dias. Esse inseto é conhecido como o pior inimigo das abelhas sem ferrão por destruírem facilmente toda uma colônia.
_(pdf.io).jpg)
A presença do forídeo, larvas e adultos nas colônias é o principal indicativo do problema. A recomendação para o controle do forídeo em colônias de A. mellifera infestadas inclui a remoção de todos os favos atacados e o deslocamento dos demais favos para o centro da colmeia. Os espaços vazios em ambas as laterais, deverão ser preenchidos por novos quadros com cera alveolada ou com favos prontos provenientes de colônias sadias, pode também ser feita a troca da colmeia antiga por uma nova ou limpa-la. Alimentação artificial e o reforço da colônia com abelhas provenientes de outra colônia, ou a união com outra colônia, são procedimentos positivos para eliminar rapidamente o problema, pois não são acometidas colônias fortes.
Para o controle em abelhas nativas sem ferrão, deve ser removido os discos e potes de alimento danificados ou com larvas, e as moscas assopradas para fora da colmeia. Os meliponicultores utilizam iscas com vinagre dentro e fora das colmeias (Figura 6.32), adesivos (papel com cola entomológica) com acesso apenas para forídeos (uso de tela), tuneis de tela na entrada da colmeia e realizam a limpeza diária de áreas afetadas.
_(pdf.io).jpg)
¶ 7. INTOXICAÇÕES
Interações entre insetos polinizadores e flores são datadas desde o final do Período Cretáceo. As abelhas dependem essencialmente de recursos florais como pólen e néctar para a manutenção das colônias. Assim como as abelhas e flores coevoluíram, organismos indesejados, a exemplo de pragas urbanas e agrícolas, também acompanharam o processo evolutivo, fazendo-se presentes nos ecossistemas. Medidas de controle são adotadas para minimizar a ocorrência, empregando-se produtos químicos como inseticidas, fungicidas, herbicidas, dentre outros. Por serem insetos, as abelhas compartilham com as pragas os sítios de ação de muitos desses produtos, que as afetam de forma adversa. Existem plantas que produzem, de forma natural, substância que são tóxicas às abelhas, o que significa outra rota de intoxicação para abelhas.
Frente a essas ocorrências, é essencial que se conheçam as principais rotas de intoxicações e como identificá-las a campo. Por isso, nesse capítulo serão abordados os principais problemas relacionados à saúde das colônias devido a fatores como contaminação por recursos alimentares tóxicos, e produtos para controle de pragas urbanas e agrícolas.
¶ 7.1 Plantas tóxicas para abelhas
Insetos que utilizam partes das plantas para sua sobrevivência e de sua cria e que, acabam por danificá-las, são ditos herbívoros. Esses são distintos dos polinizadores, pois precisam das folhas (ou outras partes) para se alimentar e/ou abrigar sua prole. Nesse grupo, são conhecidos os fitófagos, galhadores, dentre outros. Dessa forma, evolutivamente, as plantas precisaram desenvolver estratégias que as protegessem dos ataques contra herbívoros.
Muitas plantas desenvolveram compostos secundários comumente associados com a defesa contra herbívoros, produzem néctar que é tóxico ou repelente para alguns visitantes florais. Outros meios de intoxicação são via pólen, secreção dos nectários extraflorais, seiva ou “honeydew” (BARKER, 1990; ADLER, 2000).
De acordo com Barker (1990), as plantas que apresentam propriedades tóxicas para abelhas geralmente são pouco visitadas por elas, significando redução do risco de intoxicação. Entretanto, em períodos de baixa disponibilidade de recursos, as abelhas podem coletá-los mesmo em plantas tóxicas. Segue-se uma lista das principais espécies de plantas (com seus nomes populares e suas respectivas famílias) relacionadas a intoxicação de abelhas, reportados em trabalhos científicos:
120
¶ 7.1.1 Espatódea, bisnagueira, tulipa-africana
A espatódea (Sphatodea campanulata, Bignoniaceae) (Figura 7.1) é uma planta de origem africana, que foi introduzida no Brasil como árvore ornamental. Além do uso paisagístico, também contém propriedades medicinais e para controle de certas pragas. Apesar dos seus benefícios, essa planta é conhecida como grande vilã para apicultores e meliponicultores: muitos são os relatos e trabalhos científicos acerca dos prejuízos relacionados à visita de abelhas a estas plantas. Possui flores com formato de tulipa, de coloração amarelo-a vermelhado. Seus botões florais apresentam grande quantidade de néctar, que foi denominado de mucilagem por autores como Nogueira-Neto (1997) e Trigo e Santos (2000).
_(pdf.io).jpg)
Portugal-Araújo (1963) relatou os efeitos tóxicos de S. campanulata, a partir da contagem de cerca de 200 insetos mortos (incluindo abelhas) em apenas uma inflorescência, sugerindo que a toxicidade estava relacionada à presença da mucilagem misturada ao néctar (Figura 7.2). Nogueira-Neto (1997) também constatou toxicidade, a partir da contagem periódica dos insetos encontrados em flores caídas de S. campanulata, reportando a morte de diversas abelhas africanizadas e as nativas sem ferrão (Plebeia droryana, Tetragonisca angustula, Scaptotrigona postica, Trigona spinipes, Friesella schrottky e Melipona quadrifasciata).
_page-0001.jpg)
Em 445 flores de S. campanulata, Trigo e Santos (2000) registraram 345 insetos mortos, em sua maioria meliponíneos. Em laboratório, a mucilagem pura, coletada de botões florais, e concentração de 25%, reduziu a longevidade de larvas de S. postica em 95,2% e 52,9%, respectivamente. Também em bioensaios de laboratório, Calligaris (2001) reportou efeitos tóxicos do néctar de espatódea sobre operárias de A. mellifera, através da redução da sobrevivência. No mesmo estudo, o pólen na concentração de 5%, não mostrou efeito tóxico para A. mellifera e S. postica.
Em meliponário da Embrapa Amazônia Oriental, observações feitas em 2012 permitiram constatar a toxicidade de pólen e néctar de espatódea em colônias de Melipona seminigra e M. fasciculata. As abelhas apresentaram sintomas de envenenamento, que incluíam morte de larvas e operárias adultas (QUEIRÓZ et al., 2017). As primeiras observações constataram que, em um estágio inicial, as abelhas conseguiam limpar as primeiras células com sintomas, mas, após alguns dias, a mortalidade de operárias adultas também era intensa, não havendo mais limpeza, atraindo forídeos, formigas e outros insetos oportunistas. Os autores constataram, experimentalmente, a relação destes sintomas com a coleta de pólen e néctar de espatódea, enfatizando os riscos de introdução destas árvores em locais onde se pratica a meliponicultura.
¶ 7.1.2 Barbatimão
(Stryphnodendron spp., Fabaceae) (Figura 7.3): o gênero é típico do Cerrado brasileiro e áreas de transição entre Mata Atlântica e Cerrado, e as árvores possuem alto valor econômico na produção madeireira, farmacológica e industrial. As flores disponibilizam um pólen considerado tóxico para abelhas, o qual pode reduzir em até 50% a longevidade das abelhas operárias.
_page-0001.jpg)
Para Lorenzi (1992), em sua obra de referência sobre as plantas arbóreas nativas do Brasil há dois tipos de barbatimão: Stryphnodendron adstringens (conhecido popularmente como barbatimão verdadeiro) e Dimorphandra mollis (popularmente dito barbatimão-de-folha miúda ou barbatimão falso). Apesar de pertencerem a gêneros diferentes, ambas as espécies apresentam período de florescimento muito próximo. O barbatimão verdadeiro floresce a partir de meados de setembro, prolongando-se até o final de outubro, enquanto o barbatimão falso floresce a partir do final de outubro, prolongando-se até janeiro.
No Brasil, as duas espécies de “barbatimão verdadeiro” que disponibilizam pólen tóxico são S. adstringens e S. polyphyllum (CARVALHO e MESSAGE, 2004). A espécie Dimorphandra mollis também possui pólen tóxico capaz de matar abelhas adultas, devido à presença do flavonoide astilbina (CINTRA et al., 2002).
Em estudos desenvolvidos com extrato aquoso de inflorescência e de nectário, o primeiro apresentou redução significativa na taxa de longevidade de operárias de abelhas melíferas. No segundo caso (extrato de nectário) não houve toxicidade (ALVEZ et al., 1996; 1998). Cintra et al. (2003) utilizaram inflorescências desidratadas de barbatimão de S. adstringens e D. mollis, incorporadas ao alimento para abelhas, verificando que, apesar de não ter havido repelência ao alimento tratado, as abelhas tiveram menor taxa de sobrevivência.
A exposição de abelhas ao barbatimão está diretamente relacionada à doença denominada “Cria Ensacada Brasileira” (CEB), um problema significativo para a atividade apícola brasileira. Nas regiões do cerrado brasileiro, Message et al. (1995) identificou sintomas semelhantes a doença conhecida como “cria ensacada” nas larvas, no entanto, sem nenhuma associação a vírus ou outro patógeno. Em função dos sintomas serem semelhantes e a doença não ser causada pelo vírus, Message (1997) passou a denominar essa doença no Brasil como Cria Ensacada Brasileira.
Carvalho (1998), demonstrou que essa doença ocorre na mesma época do florescimento do barbatimão (S. polyphyllum) e que, fornecendo pólen dessa planta na dieta de larvas de operárias em bioensaios, os mesmos sintomas eram reproduzidos. Posteriormente, Santos e Message (1998) verificaram que alimentando larvas de abelhas em laboratório com ácido tânico, os sintomas da doença também podiam ser reproduzidos e, então sugeriram que os taninos normalmente encontrados em grande quantidade no barbatimão, seriam os causadores da Cria Ensacada Brasileira. Os sintomas da CEB são: perfurações nos favos de cria fechada, morte dos indivíduos entre a fase de larva e pupa, formação de líquido ecdisial entre a ecdise e a epiderme da larva em formação, e coloração cinza ou marrom das larvas/pupas.
A intoxicação ocorre a partir do momento em que as abelhas nutrizes utilizam o pólen do barbatimão para alimentar as larvas. As larvas não conseguem se desenvolver até a fase de pupa. Os indivíduos afetados mostram acúmulo de líquido da ecdise entre sua epiderme e a última cutícula desenvolvida, sendo que as larvas acabam por ficar em formato de sacos, de onde vem o nome da doença.
No caso de abelhas sem ferrão, a susceptibilidade aos efeitos tóxicos do barbatimão pode variar em função da espécie de abelha (SILVA, 2012). Silva et al. (2012) testaram diferentes concentrações do pólen (1, 2 e 3%), incorporado ao alimento larval de 3 espécies: em Scaptotrigona depilis não houve mortalidade; Nannotrigona testaceicornis não apresentou mortalidade significativa apenas na concentração de 1%; e em Tetragonisca angustula houve mortalidade significativa das crias a partir da concentração de 1%. Já para os testes realizados com abelhas A. mellifera, ocorreu mortalidade em todas as concentrações testadas. Os autores associaram a questão de que as abelhas A. mellifera são exóticas no país e sua adaptação e resistência a plantas nativas brasileiras, que produzem substâncias tóxicas, pode ser menor quando comparada às abelhas nativas.
¶ 7.1.3 Neem
O grupo de pesticidas conhecido como bioinseticida é formado por componentes de plantas, animais, fungos ou bactérias, possuindo ação alelopática em vários organismos. Inseticidas reguladores do crescimento são bioinseticidas que possuem como alvo características específicas ou estágio específico de desenvolvimento do inseto, mantendo uma margem de segurança para as demais espécies, sendo relativamente seguro para humanos e animais domésticos (DESNEUX et al., 2007).
O consumo de azadirachtin, um terpenóide extraído da árvore Azadirachta indica (Neem, Figura 7.4), vem crescendo no Brasil, principalmente por ser natural e pela crença prevalecente entre os agricultores que tais produtos oferecem grande margem de aplicação no campo (FREITAS E PINHEIRO, 2010). O Neem é considerado um inseticida regulador de crescimento dos insetos, causando inibição do desenvolvimento e mudanças na metamorfose desses indivíduos. Esse componente pode ser usado como inseticida natural com efeitos específicos em diferentes estágios de crescimento dos insetos (SILVA-ZACARIN et al., 2006), porém sua ação tóxica pode provocar inibição da alimentação e redução da fecundidade dos insetos (STEVENSON E WALTER, 1983).

Embora todos os efeitos possam ser considerados em nível molecular, a interação molecular entre o princípio ativo e o alvo pode resultar em impacto macroscópico que pode ser observado em células, tecidos, órgãos, indivíduos ou em níveis populacionais como na colônia de abelhas (BELZUNCES et al., 2010).
Um dos possíveis efeitos subletais do uso do inseticida Neem em abelhas Apis mellifera são danos causados às glândulas hipofaringeanas. Em operárias nutrizes essas glândulas produzem a maior parte da proteína da geleia real (PATEL et al., 1960) e a redução no tamanho dessas glândulas pode acarretar vários efeitos na saúde e desenvolvimento da colônia (SMODIS SKERL E GREGORC, 2010).
Inseticidas mimetizadores da ação de hormônios juvenis, como o azadirachtin, são considerados de baixa toxicidade e, apesar de geralmente não apresentarem efeitos visíveis no indivíduo, podem gerar efeitos subletais. Melanthoupolos et al. (2000) detectaram que aplicações de azadirachtin no campo, em intervalos de seis dias, reduziu severamente a área de cria e causou grande mortalidade de rainhas nas colônias.
Baixos níveis de doses e/ou aplicações, principalmente à longo prazo, são pouco conhecidos e não tem sido considerado nos estudos de risco para fins de discussão (MALASPINA E SILVA-ZACARIN, 2006). Espécies de abelhas menores, como a Partamona sp. por exemplo, são mais susceptíveis que abelhas maiores.
As abelhas são animais que vivem em contato próximo à natureza coletando pólen, néctar, água e resinas para a colônia, e para isso é necessário que todas as fontes desses recursos sejam puras e sem contaminantes (CHAMBÓ et al., 2010). De modo geral, o neem não causa repelência às abelhas em laboratório (mesmo sendo repelente e fagoinibidor a vários insetos). Logo, as abelhas não evitam áreas pulverizadas e nem deixam de ingerir alimento contaminado.
Naturalmente as abelhas melíferas preferem forragear outras plantas apícolas ao invés do neem. No entanto, se houver falta de pólen no ambiente, a colônia não irá hesitar em coletar esse recurso floral no neem ou até mesmo em outras plantas que podem ser tóxicas para a saúde da colônia, colocando em risco seu desenvolvimento. Geralmente as abelhas adultas não apresentam problemas devido à baixa toxicidade do neem, o maior prejuízo ocorre nas crias em desenvolvimento.
¶ 7.2 Produtos para controle de pragas
De acordo com a Vigilância Ambiental em Saúde (2001), o controle químico é a última alternativa de controle a ser utilizada, uma vez que outras ações menos agressivas e eficazes devem ser prioritárias. Assim, recomenda-se que se evite ao máximo o uso de agrotóxicos, e que sua utilização seja restrita a emergências ou quando não se dispuser de outra ferramenta de intervenção.
¶ 7.2.1 Produtos para controle de pragas urbanas
Em função da adaptação ao convívio com o homem, da capacidade reprodutiva e da quantidade de abrigos e alimentos encontrados em áreas urbanizadas, muitas espécies animais são consideradas pragas urbanas. Esses organismos podem ter ação nociva ao homem, ocasionar prejuízos econômicos, ou ainda, simplesmente causar incômodo.
De acordo com a Vigilância Ambiental em Saúde (2001), dá-se o nome genérico de praguicidas aos compostos orgânicos ou inorgânicos, de origem natural ou sintética, que podem ser usados puros ou misturados no controle de pragas (animais ou vegetais) com eventuais efeitos deletérios ao homem, animais domésticos ou plantas cultivadas. De acordo com a finalidade para a qual são usados, classificam-se em: acaricidas, inseticidas, fungicidas, rodenticidas, moluscicidas, herbicidas, entre outros.
É cada vez mais comum que, em função do desmatamento e a consequente perda de hábitat para nidificação de abelhas, tanto melíferas quanto as nativas, esses organismos busquem por estes locais, muitas vezes em centros urbanos. Embora não sejam o alvo, elas acabam sofrendo a ação dos produtos, se estiverem presentes no ambiente.
No Brasil, os produtos químicos mais usados, atualmente, no controle dos vetores das doenças são: fosforados (controle de dengue e malária), carbamatos (peste bubônica) e piretróides (malária, Chagas e Calazar). Todos os ingredientes ativos mencionados contam com estudos muito bem fundamentados, relatando sérios problemas de intoxicação às abelhas, tanto melíferas quanto nativas (BOMBARDI, 2017), além, é claro, das intoxicações com seres humanos. Dessa forma, reitera-se que estas medidas em centros urbanos sejam tomadas como última alternativa.
A quantidade de grupos de praguicidas usados em saúde pública é bem menor que aqueles disponíveis para uso agrícola, assim como são menores os casos de intoxicação de abelhas.
¶ 7.2.2 Produtos para controle de pragas agrícolas
A quantidade registrada e aplicada de produtos químicos em cultivos contra pragas agrícolas é, proporcionalmente, muito superior àqueles utilizados em centros urbanos. Entretanto, por questões ambientais, também é altamente recomendável que as medidas de intervenção química sejam vistas como as últimas alternativas a serem tomadas. São inúmeros os grupos químicos disponíveis para utilização na agricultura brasileira, com seus mais diversos ingredientes ativos, com seus diferentes níveis de toxicidade (MAPA, 2019).
O controle químico de pragas e doenças está centrado principalmente no uso de diversas classes de agrotóxicos, como herbicidas, fungicidas, inseticidas etc. O alto uso de produtos químicos é apontado como uma das causas do declínio dos polinizadores, principalmente nas áreas de monocultivo (FREITAS et al., 2009). De acordo com Malaspina et al. (2008), os inseticidas podem afetar as abelhas por três vias de contaminação: 1) por contato durante o forrageamento, através da presença de partículas de inseticida depositadas nas flores; 2) pela ingestão de pólen e néctar contaminados por inseticidas sistêmicos, que é absorvido pelo tecido vegetal; e 3) pela fumigação com partículas de inseticidas suspensas aplicadas nas áreas agrícolas, onde os efeitos de toxicidade estão relacionados as concentrações administradas somado ao tempo de exposição, podendo provocar morte e alterações fisiológicas.
¶ 7.2.2.1 Diversidade de agrotóxicos no Brasil
Da diversidade de agrotóxicos utilizados no Brasil, o fipronil (pirazol) e os neonicotinoides, têm chamado a atenção, pois são compostos que possuem baixa toxicidade para a espécie humana e animais superiores, e longo tempo de ação (KRUPKE et al., 2012). Entretanto, podem prejudicar as funções cognitivas das abelhas a curto, médio e a longo prazo. A maioria dos trabalhos relacionados aos efeitos de agrotóxicos e abelhas estão centrados nos neonicotinoides e fipronil (LUNDIN et al., 2015; HOLDER et al., 2018). Há relatos de mortalidades em massa de abelhas que, na maioria dos casos, decorre do uso incorreto de fipronil, associado a outros produtos. Os principais grupos químicos dos inseticidas de ação neurotóxica, seus respectivos sítios de ação e características serão listados a seguir.
Organofosforados
Os inseticidas organofosforados já estiveram entre os agrotóxicos mais utilizados no mundo, sendo considerados como altamente tóxicos ao meio ambiente (PENA et al., 2003), e devido ao seu amplo espectro de ação são considerados tóxicos a qualquer inseto, incluindo àqueles não-alvo, a exemplo de abelhas (STANLEY et al., 2015). A maior parte dos produtos organofosforados teve seu registro cancelado, tanto no Brasil, quanto em outros países, em função de sua toxicidade aguda e baixa seletividade.
Dos diversos representantes de organofosforados, o clorpirifós, de ação inseticida-acaricida, é amplamente utilizado, principalmente devido a sua maior persistência e eficácia contra uma ampla gama de pragas que atacam culturas economicamente importantes (AGROFIT, 2020). No Brasil este produto químico é empregado em culturas que ocupam extensas áreas, a exemplo do algodão, café, citros, maçã, milho e soja (AGROFIT, 2019).
É provável que esse inseticida esteja em contato com as abelhas em diferentes níveis de exposição, uma vez que resíduos de clorpirifós foram detectados no pólen, no mel e em favos de cria de A. mellifera, porém não foi observada letalidade nos estudos de Naggar et al. (2015). Os organofosforados atuam no sistema nervoso dos insetos, inibindo a acetilcolinesterase (AChE). Essa enzima regula o nível do neurotransmissor acetilcolina, uma substância que atua no mecanismo de transmissão de impulsos nervosos (THOMPSON, 1999).
Neonicotinoides
Inseticidas neonicotinoides foram desenvolvidos nos anos 90, sendo derivados da nicotina, para apresentar menor toxicidade e impacto ambiental. Estão registrados para uso em uma ampla variedade de culturas, sendo eficazes, contra insetos mastigadores e sugadores, tais como besouros, alguns lepidópteros e hemípteros (FAIRBROTHER et al., 2014). Esse grupo engloba os produtos imidacloprido, acetamiprido e tiametoxam. Através da sua ação neurotóxica, os neonicotinoides atuam no sistema neurológico de insetos, incluindo aqueles não alvos, tais como abelhas (DESNEUX et al., 2007). A ação agonística nos receptores nicotínicos mimetiza a acetilcolina em seus sítios de encaixe, causando efeitos subletais como perda de memória e orientação das abelhas (VAN DER SLUIJS et al., 2013). Pettis et al. (2013) acrescentam que esses efeitos a longo prazo podem ocasionar a morte dos indivíduos ou tornar a colônia mais suscetível a doenças.
De acordo com pesquisas, os neonicotinoides podem ocasionar sérios efeitos adversos para abelhas, e o declínio de populações possui relação direta com seu uso indiscriminado (SOARES, 2012), por vias de aplicação no solo, sementes, folha e tronco das plantas (AGROFIT, 2020). Os neonicotinoides podem ser aplicados via pulverização foliar, tratamento de sementes, ou aplicação no solo, de culturas como algodão, citros, alface, arroz, batata, tomate, eucalipto, girassol, maçã, morango e ainda em outros cultivos que ofertam flores atrativas para as abelhas (GODFRAY et al., 2014).
Os neonicotinoides são agonistas da acetilcolina e se ligam aos receptores nicotínicos de acetilcolina (nAChRs) e, ao contrário da acetilcolina, que é hidrolisada pela acetilcolinesterase, esses compostos não são degradados imediatamente, ou seja, os impulsos nervosos são transmitidos de uma forma contínua. Dessa forma, o resultado é a hiperexcitação do sistema nervoso do inseto, acarretando desorientação e consequente morte (GALLO et al., 2002). Por atuarem na neurofisiologia dos insetos, acabam por atingir organismos não alvo, como as abelhas, que também são insetos (DESNEUX, 2007).
Por ser tratar de um inseticida sistêmico, o ingrediente ativo pode ser deslocado pela seiva da planta de uma parte para a outra, atingindo o pólen e néctar onde traços residuais são encontrados (BLACQUIÈRE et al., 2012). Então, é nesse instante em que o contato com as abelhas pode ocorrer, além das possibilidades de aplicação sobre as abelhas forrageiras no campo, via deriva e inversão térmica.
Particularidades dos Neonicotinoides no Brasil e no mundo
Mundialmente, é crescente a utilização dessa nova classe de inseticidas em cultivos que ofertam flores atrativas para abelhas (BLACQUIÈRE et al., 2012). Nesse contexto, a perda de populações de abelhas em diversas partes do mundo tem sido alvo de inúmeras especulações e atribuída, pelo menos parcialmente, ao uso de inseticidas neonicotinoides (GODFRAY et al., 2014). Em evidência na literatura desde 2006, a síndrome denominada “Colony Collapse Disorder” (CCD na sigla em inglês) (Desordem do Colapso da Colônia) intensificou a busca por respostas quanto ao desaparecimento de abelhas, havendo menção de associação de uso de neonicotinoides a essas ocorrências. Porém, é importante ressaltar que as hipóteses das causas do CCD passaram a ser consideradas multifatoriais, ou seja, a perda de habitats, o uso de agrotóxicos, e ocorrência de doenças, por exemplo, deixariam as abelhas mais vulneráveis (GOULSON et al., 2015).
A síndrome “CCD” foi primeiramente constatada em colônias de A. mellifera e é caracterizada pelo desaparecimento repentino de operárias forrageiras, enquanto a rainha e as crias permanecem vivas nas colônias (FAIRBROTHER et al., 2014).
No Brasil, a aplicação foliar de inseticidas neonicotinoides, nas sementes e/ ou no solo, é permitida e indicada para diversas culturas, incluindo algodão, soja, citros, tomate, eucalipto, girassol, maçã e morango, as quais ofertam flores atrativas para abelhas. Os produtos devem vir acompanhados de informações como a indicação de não aplicação em períodos de floração, dos limites de aplicação e respectivos intervalos de segurança (AGROFIT, 2020). Em 2012, após uma sequência de protestos na Europa com a finalidade de banir toda e qualquer forma de aplicação dos neonicotinoides imidacloprido, tiametoxam e clotianidina, em cultivos que ofertam flores para abelhas, o Instituto Brasileiro do Meio Ambiente e dos Recursos Naturais Renováveis (IBAMA) declarou temporariamente a restrição do uso desses mesmos inseticidas e deu início a um processo de reavaliação dessas substâncias. Essas substâncias passaram a ser comercializadas com suas respectivas indicações de uso, que incluem as restrições impostas pelos órgãos reguladores (AGROFIT, 2020).
Nos Estados Unidos, são registrados oito ingredientes ativos neonicotinoides, dos quais, imidacloprido é o mais utilizado. FATE et al. (2012) elaboraram um planejamento quanto ao uso dessas substâncias ativas, alertando sobre a questão das abelhas e outros polinizadores nas embalagens dos produtos comerciais, mas não baniu ou suspendeu a utilização desses ingredientes (FAIRBROTHER et al., 2014).
Em 2013, a European Food Safety Authority (EFSA) publicou um documento contendo uma compilação de estudos que apontaram valores residuais de neonicotinoides encontrados em materiais armazenados nas colônias de abelhas, bem como no pólen e néctar de culturas que ofertam flores atrativas a elas. Inferências foram realizadas quanto aos potenciais riscos que os resíduos poderiam oferecer para abelhas. Com base nos resultados evidenciados, concluiu-se que muitas lacunas sobre os perigos que os neonicotinoides oferecem para abelhas e outros polinizadores ainda devem ser preenchidas. Assim, a posição definitiva da União Europeia foi banir o uso de inseticidas neonicotinoides por dois anos (2013- 2015) (EFSA, 2013). Sgolastra et al. (2020) defendem que os próprios esquemas de avaliação de risco com abelhas apresentam muitas lacunas que devem ser preenchidas, para que resultados mais consistentes sejam apresentados.
Fipronil
O inseticida fipronil faz parte do grupo químico fenilpirazol de segunda geração, desenvolvido no fim da década de 80. Por seu modo de ação diferir dos clássicos, é considerado um inseticida de nova geração, além de possuir amplo espectro e atuar em todas as fases de desenvolvimento do inseto, sendo eficaz até mesmo em baixas concentrações (THOMPSON, 2010).
No Brasil, o fipronil possui autorização de uso e comercialização em diversas formulações, tais como isca granulada (formicida em aplicação terrestre), suspensão concentrada (tratamento de sementes), granulado aplicado diretamente no solo, granulado dispersível e suspensão concentrada (aplicação terrestre e aérea) (ANVISA, 2016), para o controle de pragas nas culturas de algodão, arroz, batata, cana de açúcar, milho, soja, cevada, feijão, trigo, pastagens e eucalipto. Nas abelhas e demais insetos este princípio ativo age no bloqueio pré e pós-sináptico do sistema nervoso, causando hiper-exitação dos músculos e nervos levando o inseto à morte, é considerado um dos principais causadores de mortalidade em massa de abelhas (HOLDER et al., 2018).
De acordo com a sua fórmula de comercialização, os produtos decorrentes da sua degradação no solo, produzem o fotoproduto desulfinil, oxidação produzindo sulfona, hidrólise produzindo amida e processo de redução com a formação de sulfido. A meia vida do ingrediente ativo e seus metabólitos no solo indicam que são persistentes, com a degradação variando de 111 – 350 dias dependendo das condições do solo, sendo o desulfinil e o sulfido os metabólitos mais abundantes (GUNASEKARA et al., 2007).
¶ 7.2.2.2 Efeitos adversos de agrotóxicos em abelhas
Para Brittain e Potts (2011), a sensibilidade entre os diferentes grupos de abelhas a pesticidas irá depender de uma série de fatores, como por exemplo, o tamanho do corpo, a socialidade, o período de voo, o voltinismo, a especialização floral e comportamento do ninho. Assim, enfatiza-se a importância da correlação entre as características apresentadas por cada grupo de abelha e as condições ambientais oferecidas. Por exemplo, o conhecimento da duração da atividade de forrageio de uma abelha e o período de floração de determinada planta, possibilitará a apresentação de indícios quanto aos riscos da exposição e consequente susceptibilidade para cada espécie de abelha.
Por serem majoritariamente de ação neurotóxica, os primeiros sintomas de intoxicação observados em campo por agrotóxicos são, comumente, tremores e voos desorientados. Alguns comportamentos considerados anormais para abelhas podem fornecer indícios de que a colônia está sob intoxicação por agrotóxicos: o grande número de abelhas mortas próximo as colmeias/colônias, desenvolvimento tardio dos indivíduos, má formação das larvas, autolimpeza excessiva, variação de temperatura na colônia, diminuição da atividade de forrageamento, comprometimento da capacidade de retorno para a colmeia e paralisia (WU et al., 2011; NOCELLI et al., 2012; ROSA et al., 2016).
Até recentemente, os níveis de intoxicação de abelhas por agrotóxicos eram relacionados apenas à exposição letal (intoxicação aguda), que resulta em indivíduos mortos próximos às colônias (Figura 7.5). Esses índices são medidos através dos valores de concentrações/ doses letais que matam 50% de uma população. Atualmente, as preocupações aumentaram, sobretudo por causa do grande número de estudos que demonstram os efeitos subletais, ou seja, aqueles em que as abelhas não morrem (ao menos imediatamente), mas manifestam diversos sintomas como desorientação, diminuição da capacidade reprodutiva, redução no combate de doenças, dentre tantos outros, ocasionados pela exposição prolongadas aos produtos (WHITEHORN et al., 2012).

Essas e outras evidências, podem ainda conduzir a consequências mais graves, como a depressão do sistema imunológico, tornando o indivíduo mais suscetível a doenças. A exposição de abelhas da espécie A. mellifera a pesticidas enfraquece as colônias, tornando-as mais suscetíveis a infecções, como ao patógeno Nosema sp. (Pettis et al., 2013). Di Prisco et al. (2013) reportaram que a clotianidina, um dos metabólitos do neonicotinoide tiametoxam é tóxica para a espécie A. mellifera, tornando o organismo do espécime intoxicado mais suscetível à replicação de um patógeno viral que deforma as asas e induz a infecções não detectadas facilmente. Além disso, Fauser-Misslin et al. (2014) demonstraram a relevância que a interação da exposição a inseticidas neonicotinoides com a infecção pelo parasita Crhitidia bombi implica adversamente para colônias de Bombus terrestris.
O método do reflexo de extensão da probóscide (REP) visa reproduzir a interação entre abelha e planta. Durante o forrageio de uma abelha, ao atingir a flor ela estende sua probóscide como reflexo dos receptores gustativos na antena, tarso ou outras partes que são estimuladas pelo néctar. Esse reflexo induz a abelha a coletar o recurso floral e memorizar o odor ali presente (DECOURTYE et al., 2005). Dessa forma, alterações comportamentais, avaliadas através de ensaios do REP, indicam o quanto os produtos químicos podem afetar adversamente o comportamento olfatório. Além disso, o processo de polinização também será severamente afetado. Para Nocelli et. al (2012), o número de indivíduos afetados por esses efeitos adversos está diretamente relacionado ao impacto na colônia como um todo, uma vez que os mecanismos para o sucesso de organismo sociais estão centrados, em grande parte, na capacidade de aprendizagem e orientação das abelhas campeiras.
¶ 7.2.2.3 Considerações gerais sobre intoxicações
É de extrema importância identificar potenciais riscos de substâncias tóxicas para abelhas, tanto aquelas presentes em plantas tóxicas, quanto pelos compostos sintéticos. A compreensão sobre o impacto que os mesmos têm sobre a diversidade de abelhas e, consequentemente, sobre o processo de polinização, é de suma importância para os planejamentos de proteção a esses organismos.
O uso inadequado de agrotóxicos pode submeter os polinizadores a situações de estresse graves, com consequentes prejuízos econômicos. Esse fato vem sendo reportado pela conjunção entre perdas de populações de abelhas, e pela sua valoração em termos de serviços ecossistêmicos que, em cifras, equivale a cerca de 43 bilhões de reais anuais (WOLOWSKI et al., 2019).
Nos casos relacionados às intoxicações de abelhas por agrotóxicos é relevante o envolvimento de profissionais engenheiros agrônomos dos OESAs para que ocorra a atuação conjunta e sinérgica da saúde animal com a sanidade vegetal visando melhores resultados, especialmente em ações de comunicação e educação em saúde, tanto aos criadores de abelhas quanto aos agricultores.
Entender o papel dos polinizadores como serviços ambientais dos ecossistemas, efetivo e necessário à produção agrícola mundial e, portanto, à segurança alimentar, é fator-chave na sustentabilidade das gerações futuras.
¶ 8. DIAGNÓSTICO DIFERENCIAL DAS DOENÇAS DE ABELHAS
Para um adequado tratamento ou procedimento sanitário é importante identificar corretamente o agente patogênico que está acometendo a colônia de abelhas. O diagnóstico diferencial consiste em um método de identificação de doenças por eliminação. Isto é, o médico veterinário responsável, com base na sintomatologia (sinais e sintomas), por meio de um exame clínico de campo restringe o diagnóstico a um grupo de possibilidades classificadas como prováveis. Ainda assim, podem ser necessários exames complementares ou testes laboratoriais para obtenção do diagnóstico final.
O diagnóstico diferencial exige a avaliação do estado da colônia como um todo para identificação correta do problema. Por exemplo, se foi identificada mortalidade de cria, essa mortalidade pode ter ocorrido devido a problemas sanitários, manejo inadequado ou até mesmo devido às condições ambientais adversas, como frio em excesso, por exemplo.
A seguir, estão relacionados os diagnósticos diferenciais das principais doenças que acometem as abelhas:
Cria pútrida europeia ou loque europeia (CPE): pode ser confundida com loque americana, cria ensacada e cria morta pelo frio. A principal diferença entre loque europeia e loque americana é que na europeia a contaminação e morte ocorre na fase larval, enquanto, na loque americana, a contaminação ocorre na fase inicial de larva, mas a morte só ocorre na fase de pupa.
Cria pútrida americana ou loque americana (CPA): embora seja bastante semelhante à loque europeia, na infecção por loque americana os sinais clínicos gerais que incluem favos falhados com opérculos afundados, muitas vezes apresentando aspecto gorduroso, perfurações ou remoção total; cria morta nas fases de pré-pupa e pupa (nessa fase um sinal pode ser a língua projetada acima da cabeça), além de alterações de cor, consistência viscosa e odor característico (Figura 8.1). Uma forma de direcionar a suspeita em campo ocorre por meio do teste do palito de madeira. Nesse teste, utiliza-se um palito de madeira ou qualquer material que possa ser inserido e retirado do alvéolo contendo a larva com sintomas. O palito de madeira ou similar deve então ser levemente mexido para entrar em contato com a larva e retirado lentamente do opérculo, se a larva apresentar aspecto pegajoso provavelmente a contaminação se deu por loque americana e não por loque europeia. O material suspeito deverá ser encaminhado ao laboratório oficial para diagnóstico.
_(pdf.io).jpg)
Cria ensacada: afeta as larvas antes de se tornarem pupas. As crias acometidas pelo vírus Morator aetatulas não apresentam odor característico como na loque europeia e loque americana. A região da cabeça da larva apresenta aspecto enegrecido, destacando-se do corpo. Outra característica bastante marcante ocorre quando as larvas são removidas do alvéolo cuidadosamente sem que haja danos na cutícula, dessa forma apresentam aspectos que lembram um saco contendo água em seu interior.
Cria giz: o fungo Ascophaera apis também acomete as crias das abelhas. Contudo, diferentemente das demais doenças de cria (loque europeia, loque americana e cria ensacada), o corpo das larvas infectadas é severamente desidratado, apresentando aspecto mumificado. Ao sacudir o favo é possível escutar um barulho lembrando um chocalho, devido ao fato de as larvas secas baterem contra as paredes do alvéolo.
Pequeno besouro das colmeias (Aethina tumida): o pequeno besouro das colmeias pode ser confundido com outros coleópteros de mesmo porte e características morfológicas semelhantes, mas que não se desenvolvem em colônias de abelhas. O Aethina tumida não parasita as abelhas, no entanto, alimentam-se das crias, pólen e do mel encontrados nas colônias. Nos casos acompanhados pelo Serviço Veterinário Oficial a campo no estado de São Paulo, raramente foram encontradas larvas. É possível que isto ocorra devido ao comportamento higiênico da abelha africanizada, pois as larvas eram encontradas somente em colônias fracas ou em colmeias abandonadas. As larvas de Aethina tumida além das características morfológicas, são diferentes das larvas de traça da cera por não produzirem fios de ceda antes de empupar. O diagnóstico deve ser laboratorial devido as semelhanças entre algumas espécies de besouros (teste de morfologia realizada por um especialista ou teste molecular).
_(pdf.io).jpg)
Vírus: as doenças provocadas pelos diferentes vírus que acometem as abelhas são de difícil identificação baseado nos sinais clínicos de campo. Isso porque os sintomas são parecidos entre si e, por isso, é necessário a realização de exames laboratoriais para confirmação do agente causador. Normalmente, as doenças virais ocorrem em colônias com alta taxa de infestação por Varroa destructor. Isso ocorre porque o ácaro atua como vetor, auxiliando na propagação do vírus entre as abelhas e entre colônias. A metodologia para avaliar a taxa de infestação da V. destructor está descrita no capítulo 07.
Acariose: a acariose é outra doença onde o diagnóstico diferencial em campo é muito difícil. O principal sintoma dessa doença é a presença de abelhas na frente da colônia com as asas desconjuntadas. Podendo apresentar paralisia, sintoma também observado em infecções virais.
Nosemose: um dos sintomas da nosemose é a diarreia no interior e frente da colônia. No entanto, esse sintoma não é exclusivo dessa doença, podendo ser ocasionado também pelo consumo de xarope fermentado pelas abelhas e outras enfermidades. Portanto, é necessária a confirmação em laboratório. Além disso, as abelhas podem apresentar tremores, dificuldade para voar, rastejar pelos favos, que também são sintomas provocados por alguns vírus e intoxicações.
Tropilaelaps: o ácaro Tropilaelaps spp pode ser confundido com o ácaro Varroa destructor que ainda não atingiu a fase adulta. Pior isso, é importante coletar amostras de pupas infestadas para identificação morfológica do ácaro ou PCR. O Tropilaelaps é menor (0,4 a 0,5 mm) e possui o corpo alongado, enquanto a Varroa mede cerca de 1,5 mm e seu corpo possui formato ovalado (Figura 8.2).

¶ 9. GUIAS DE DOENÇAS DE ABELHAS
O presente Manual traz informações importantes no formato de “Guias de Doenças de Abelhas” sobre as principais doenças. O material técnico deverá servir como referência para ações de defesa sanitária animal no âmbito do Programa Nacional de Saúde das Abelhas e para o desenvolvimento de estratégias regionais de controle ou erradicação por parte do serviço veterinário estadual ou setor privado quando pertinente.
As doenças de abelhas que requerem intervenção do serviço veterinário oficial ou fazem parte da vigilância ou monitoramento do Programa Nacional de Saúde das Abelhas estarão listadas na legislação de saúde animal.
|
Infestação por Aethina tumida (Pequeno besouro das colmeias) |
|
|---|---|
| AGENTE |
Família: Nitidulidae Gênero: Aethina Espécie: Aethina tumida (Murray, 1867) |
| ESPÉCIES SUSCEPTÍVEIS | Os besouros infestam, principalmente, colmeia de abelhas da espécie Apis mellifera, no entanto, também existem relatos de infestação em colmeias de Abelhas Nativas sem Ferrão. |
| POPULAÇÃO ALVO DO PROGRAMA DE VIGILÂNCIA | Colônias de abelhas. |
| COBERTURA GEOGRÁFICA | Todas as áreas de exploração de apicultura e meliponicultura, incluindo as áreas referentes às rotas de apicultura e meliponicultura migratórias. |
|
SINAIS CLÍNICOS/LESÕES
|
Os principais danos à colmeia são causados pelas larvas do besouro, que se alimentam das crias, do pólen e do mel. As larvas, ao se movimentarem, perfuram as células de mel levando a sua fermentação, tornando-os, dessa forma, impróprios para consumo humano. Além deste prejuízo, a infestação das colônias de abelhas pode causar a fuga do enxame e o abandono da colmeia O objetivo do besouro nas colmeias não é o de parasitar diretamente as abelhas, mas buscar alimento, alguns autores os consideram um cleptoparasita, pois roubam alimento de outros animais. Período de Incubação: Não se aplica |
| TRANSMISSÃO |
O besouro tem capacidade de deslocamento amplo (de até 13 km, mas não é possível precisar sua amplitude de voo), sendo capaz de se dispersar rapidamente e invadir novas colmeias. A movimentação das colmeias, favos de mel, ceras de abelhas e outros produtos apícolas, vestimentas utilizadas em diferentes apiários, utensílios comuns como: formões, fumigadores, além de troca de quadros entre colônias, são as formas mais comuns de transmissão da infestação. Colônias capturadas em caixas-isca, abrigos naturais e artificiais (colônias naturais não manejadas), podem ser um vetor de transmissão, caso estejam infestadas. |
| CRITÉRIO DE NOTIFICAÇÃO | A infestação pelo pequeno besouro das colmeias - Aethina tumida - requer notificação imediata ao Serviço Veterinário Oficial de qualquer caso suspeito ou diagnóstico laboratorial positivo. |
| DIAGNÓSTICO DIFERENCIAL |
Larvas podem ser confundidas com as da traça da cera, porém, possuem diferenças morfológicas conforme Anexo. Outras espécies de besouros que apresentam características morfológicas semelhantes (foto do A. tumida adulto pode ser observada no Anexo). |
| RECOMENDAÇÃO PARA DIAGNÓSTICO LABORATORIAL |
Identificação de insetos através de caracteres morfológicos e microscopia de luz por um taxonomista, OU; Entomologia molecular - Reação da cadeia da polimerase (PCR) em tempo real. Particularmente útil para identificação de larvas quando os espécimes estão danificados. |
| LABORATÓRIO RECOMENDADO |
Identificação do agente através de caracteres morfológicos: qualquer laboratório privado ou público, independente se pertencente à rede oficial de laboratórios do MAPA, capaz de realizar a identificação entomológica. Atualmente, o Instituto Biológico de São Paulo está realizando, rotineiramente, esta análise. Entomologia molecular - Reação da cadeia da polimerase (PCR) através da identificação de pragas por DNA barcoding: Laboratório Federal de Defesa Agropecuária-LFDA/GO. |
| ORIENTAÇÃO PARA COLETA DE AMOSTRAS |
Entomologia molecular - Reação da cadeia da polimerase (PCR) ou Identificação do agente através de caracteres morfológicos. Tanto a forma adulta quanto o estágio de larva permitem a identificação. Os espécimes devem ser coletados e acondicionados em frasco limpo e bem fechado contendo álcool 70 % (até cobrir besouros e/ou larvas). Essa forma de conservação permite a análise tanto por entomologia molecular quanto a identificação morfológica (ver foto em Anexos). As amostras podem ser conservadas e enviadas para o laboratório em temperatura ambiente. |
| AÇÕES RECOMENDADAS |
Manter as colônias fortes, selecionando-as para comportamento higiênico, aumentando as chances de eliminação de ovos e larvas por parte das abelhas. Ações preventivas como boas práticas de manejo apícola; medidas de vigilância para detecção precoce; controle do ingresso de abelhas e seus produtos quando oriundos de locais onde já foi detectada sua presença. Evitar repovoamento de apiários por meio da captura de colônias em caixas-isca. Aplicar as demais medidas presentes na Nota Técnica sobre Aethina tumida, disponível no site do MAPA. Link: NotaTcnica9Aethinatumida.pdf (www.gov.br). |
| PRAZO PARA ENCERRAMENTO DE FOCO/CONCLUSÃO DAS INVESTIGAÇÕES | Após o recebimento do resultado laboratorial confirmatório, o SVO deve estabelecer um Termo de Compromisso com o apicultor responsável para que ele implante em seu apiário as boas práticas elencadas na Nota Técnica sobre Aethina tumida, preencher o Form-Com de encerramento e finalizar a investigação. |
| REGULAMENTAÇÃO OFICIAL | Instrução Normativa SDA nº 16 de 8 de maio de 2008: Instituiu o Programa Nacional de Sanidade Apícola. |
| LITERATURA CONSULTADA |
ANSES - Identification of the small hive beetle Aethina tumida, morphological examination (OIE method). 2015. Disponível em: https://www.izsvenezie.com/documents/reference-laboratories/beekeeping/aethina-tumida/documentation/ANSES-identification-OIE-method.pdf BRASIL. Ministério da Agricultura Pecuária e Abastecimento. Nota técnica Nº 9/2019/DSE/CAT/CGSA/DSAIP_2/DAS/MAPA. Infestação de colmeias pelo Aethina túmida, Brasília, 2019. Disponível em: https://www.gov.br/agricultura/pt-br/assuntos/sanidade-animal-e-vegetal/saude-animal/programas-de-saude-animal/NotaTcnica9Aethinatumida.pdf EURL/ANSES – Guidelines for the surveillance of the small hive beetle (Aethina tumida) infestation. 2015. Disponível em: https://www.anses.fr/fr/system/files/Guidelines_SHB_surveillance_EURL.pdf Manual – nuevos manejos en la apicultura para el control del pequeño escarabajo de la colmena - SAGARPA - México – 2014. Disponível em: https://www.researchgate.net/publication/265292604_Manual_de_Nuevos_Manejos_en_la_Apicultura_para_el_Control_del_Pequeno_ Manual práctico de operaciones en la lucha contra Aethina tumida y Tropilaelaps spp - Ministerio de Agricultura, Alimentación y Medio Ambiente - España – 2015. Disponível em: https://www.mapa.gob.es/es/ganaderia/temas/sanidad-animal-higiene-ganadera/manual_operaciones_contra_aethina_tumida_y_tropilaelaps_spp_junio2017_tcm30-423142.pdf Nota Técnica CDA - Aethina tumida. https://www.defesa.agricultura.sp.gov.br/arquivos/sanidade-animal/nota-tecnica-Aethina-tumida.pdf OIE - Terrestrial Animal Health Code - Cap. 9.4 – 2019. Disponível em: https://www.oie.int/fileadmin/Home/eng/Health_standards/tahc/current/chapitre_aethina_tumida.pdf OIE - Manual of Diagnostic Tests and Vaccines for Terrestrial Animals - Cap. 3.2.5 – 2018. Disponível em: https://www.oie.int/fileadmin/Home/eng/Health_standards/tahm/3.02.05_SMALL_HIVE_BEETLE.pdf EFSA - Small hive beetle diagnosis and risk management options. European Food Safety Authority. 2015. Disponível em: https://www.efsa.europa.eu/en/efsajournal/pub/4048 TEIXEIRA, E. W.; De JONG, D.; SATTLER, A.; MESSAGE, D. Aethina tumida Murray (Coleoptera, Nitidulidae), o pequeno besouro das colmeias chega ao Brasil: NOTA AO APICULTOR. Mensagem Doce. 2016. Disponível em: http://apacame.org.br/site/revista/mensagem-doce-n-136-maio-de-2016/nota-tecnica/ |
ANEXOS:
_(pdf.io).jpg)
_(pdf.io).jpg)
_(pdf.io).jpg)
|
Infecção por Paenibacillus larvae (Cria pútrida americana ou Loque Americana) |
|
|---|---|
| AGENTE |
Família: Paenibacillaceae Gênero: Paenibacillus Espécie: Paenibacillus larvae (Ash et al. 1994; Hendrickx et al., 1996) Também conhecida por Cria Pútrida Americana. Causa graves perdas econômicas. A doença não representa ameaça à saúde humana. |
| ESPÉCIES SUSCEPTÍVEIS |
Estágios de larva e pupa das abelhas da espécie Apis mellifera. Abelhas adultas (são vetores da bactéria), outras espécies de animais e o homem não são susceptíveis. |
| POPULAÇÃO ALVO DO PROGRAMA DE VIGILÂNCIA | Colônias de abelhas. |
| COBERTURA GEOGRÁFICA | Áreas de exploração de apicultura incluindo as áreas referentes às rotas de apicultura migratória. |
|
SINAIS CLÍNICOS/LESÕES
|
Nas colônias com sinais clínicos de loque americana, as crias são normalmente encontradas mortas nos estágios finais de larva e durante toda fase de pupa, depois que as células de cria são operculadas (foto em Anexos). O opérculo pode estar afundado e escurecido e até mesmo perfurado irregularmente nesses casos. Estes opérculos são muitas vezes perfurados pelas abelhas que tentam fazer a limpeza destas células. Os quadros de cria em uma colônia afetada apresentam grande quantidade de falhas na cria (alvéolos vazios). O padrão das crias também é bastante disperso devido a remoção das pupas infectadas. As larvas e pupas mortas pela loque americana tornam-se marrons e sofrem um lento processo de desidratação e decomposição, diminuindo de volume dentro de cada alvéolo. Neste estágio pode-se aplicar o teste do palito como primeiro indicativo da doença. Para tal, utiliza-se um ramo seco afilado, palito de fósforo ou mesmo um palito de dentes para remover o opérculo e na sequência a pupa suspeita. Caso a pupa fique presa no fundo do alvéolo e com a retirada do palito ocorra a formação de um fio elástico (viscoso) com mais de 2 cm, confirma-se a suspeita da doença (foto em Anexos). Quando uma grande quantidade de pupas morrem simultaneamente, pode-se sentir um odor desagradável ao abrirmos a colmeia. Após 25 a 30 dias da morte da pupa, forma-se uma escama seca e preta aderida à parede inferior e ao fundo das células/alvéolos (fundo do favo). Nesta fase de escama, em alguns casos, percebe-se a extremidade da glossa (língua) ainda aderida na parede superior do alvéolo (Foto em Anexos). Sinais clínicos gerais incluem, nas crias, favos falhados com opérculos afundados, muitas vezes apresentando aspecto gorduroso, perfurações ou remoção total dos operculos; cria morta nas fases de pré-pupa e pupa, além de alterações de cor, consistência viscosa, odor característico e desidratação. Período de Incubação: no caso desta doença o processo de incubação é totalmente peculiar. Os esporos da bactéria são transmitidos pelas operárias nutrizes junto com o alimento larval e depois de 4 a 5 dias desencadeiam o processo doença, já na fase de pré-pupa ou pupa. Como a postura da rainha é diária, o surgimento de larvas suscetíveis será contínuo e caso a fonte de alimento contaminado persistir, teremos uma mortandade de pupas continuada. Para efeito do código sanitário o período de incubação é de 15 dias. |
| TRANSMISSÃO |
A transmissão primária ocorre por alimento (mel ou pólen) ou água contaminados, além de restos de crias mortas. Já na fase de escama (após 25 a 30 dias da morte da pupa), as abelhas operárias e nutrizes podem se contaminar por meio da trofalaxia, que é o processo de troca de alimentos entre as abelhas. Os esporos também podem ser transmitidos pelas abelhas adultas encarregadas da limpeza dos favos e da trofalaxia. O intercâmbio de quadros entre colônias é a causa mais comum de dispersão no apiário. As abelhas espalham a doença dentro da colmeia, especialmente as faxineiras, que ao eliminarem as escamas de pupas mortas, espalham os esporos por toda a colônia. As principais rotas de infecção entre diferentes colmeias e entre apiários são a pilhagem de colônias doentes, erros de voo (deriva – abelhas que entram nas colônias que não a de sua origem), manejo pouco cuidadoso por parte do apicultor, alimentação com mel de origem desconhecida, e utilização da caixa-isca no povoamento de apiários. A transmissão também ocorre por meio da comercialização de produtos e material vivo, tais como venda de colônias ou rainhas. Além destas vias “naturais” de transmissão horizontal entre colônias, existem outras vias artificiais introduzidas pelo apicultor. É comum no manejo apícola realizar a troca entre colônias de materiais da colmeia como mel ou células de cria, reutilizar materiais da colmeia antiga quando se prepara uma nova caixa e juntar colônias fracas para formar uma mais forte. Se estes materiais da colmeia estiverem contaminados com esporos de Paenibacillus larvae e/ou os produtos das abelhas estiverem contaminados com esporos ou infectados, isso irá caracterizar uma outra forma de transmissão horizontal de CPA, o que não ocorreria em colônias naturais. |
| CRITÉRIO DE NOTIFICAÇÃO | A Loque Americana requer notificação imediata ao Serviço Veterinário Oficial de qualquer caso suspeito ou diagnóstico laboratorial positivo. |
| DIAGNÓSTICO DIFERENCIAL | Loque Europeia, cria ensacada, cria morta pelo frio e cria giz (semelhança na característica cria salteada ou falhada). |
| RECOMENDAÇÃO PARA DIAGNÓSTICO LABORATORIAL |
Confirmação diagnóstica através do isolamento por cultivo ou PCR. É possível a realização de uma prova de campo – teste do palito de madeira (descrito no Manual do PNSAb), que se realiza diretamente sobre os restos de pupas mortas. Caso o teste do palito dê positivo ou o SVO encontre outros sinais clínicos compatíveis com a Loque americana, devem ser coletados favos contendo mel dos quadros de crias e enviados para o laboratório oficial para diagnóstico definitivo (quantidade mínima de 50 mL de mel). |
| LABORATÓRIO RECOMENDADO | Laboratório Federal de Defesa Agropecuária-LFDA/RS. |
| ORIENTAÇÃO PARA COLETA DE AMOSTRAS |
Coletar favos de mel, cortes de 6x6 cm que devem apresentar aproximadamente 50 mL de amostra (sem considerar o favo). As amostras podem ser encaminhadas em temperatura ambiente ao LFDA-RS. Antes do envio do material, o OESA deve informar ao laboratório a quantidade de amostra a ser enviada e a data prevista de chegada. Informações adicionais de acondicionamento podem ser obtidas no Manual Veterinário de colheita e envio de amostras. Manual Veterinário de colheita e envio de amostras: manual técnico. Disponível em: https://www.gov.br/agricultura/pt-br/assuntos/sanidade-animal-e-vegetal/saude-animal/programas-de-saude-animal/ManualdecolheitadeamostrasABELHAS.pdf |
| MEDIDAS A SEREM APLICADAS |
Imediatamente após a notificação da suspeita da doença, o serviço oficial de defesa sanitária deve adotar todos os procedimentos de investigação epidemiológica, estabelecer uma zona de vigilância, e adotar ações de restrição de trânsito de colmeias de Apis mellifera e produtos de risco. Destruição do material vivo e inerte infectado, através da queima das colônias infectadas, enquanto as caixas e as melgueiras podem ser passados a fogo (utilizando um maçarico, por exemplo) para seu reaproveitamento. Somente o conteúdo do interior (abelhas e favos) deve ser destruído. Investigação epidemiológica, ampliação da vigilância, identificando os contatos diretos do apiário foco, apiários de outros proprietários, compra e venda de materiais vivos e inertes, e os contatos com parceiros polinizadores. Não existe nenhum produto veterinário aprovado para uso em colmeias no Brasil. Os antibióticos não são eficazes, pois não destroem os esporos e não impedem a doença de se manifestar mais tarde. A utilização de antibióticos também não é recomendada por deixar resíduos no mel e na cera. Além disso, a utilização de antibióticos pode mascarar o surgimento de linhagens resistentes. Em geral, é também indicado que as colônias sejam colocadas em locais com abundância de pólen e néctar, que seja feita a substituição de rainhas por linhagens resistentes, que materiais utilizados no manejo sejam sempre limpos e que as abelhas sejam alimentadas durante a época que não há pasto apícola. Como os esporos de CPA podem ser encontrados algumas vezes em méis de colônias sem sinais clínicos, é aconselhável alimentar as colmeias apenas com méis que foram testados laboratorialmente e estejam livres de esporos. Da mesma forma, deve-se coletar pólen para uso futuro, de colônias que foram examinadas e encontram-se livres da infecção. A substituição regular dos favos de mel e quadros de cria é geralmente recomendada para prevenir focos de CPA, não devendo ser utilizados os mesmos por mais de três anos. Em alguns países, como nos escandinavos, é prática comum não utilizar estes materiais por mais de um ano. Como medida de prevenção e vigilância, os apicultores devem ser instruídos sobre boas práticas apícolas, como: inspecionar os seus apiários periodicamente, com atenção especial aos quadros de cria, evitar a transferência de quadros de cria e todo o material a ser usado deve ser limpo e desinfetado. Os apicultores devem ser instruídos que, sempre que optar por alimentar as suas colônias com mel, usar mel da sua própria exploração. Evitar repovoamento de apiários por meio da captura de colônias naturais ou enxames em caixas-isca, ou quando capturar enxames na natureza submetê-los à quarentena em área separada antes de incorporar as novas colônias ao apiário. |
| PRAZO PARA ENCERRAMENTO DE FOCO/CONCLUSÃO DAS INVESTIGAÇÕES | 30 dias após a destruição de todo o material infectado (vivo e inerte), inicia o repovoamento das colmeias com o alojamento de 10 % da população inicial. Após 30 dias sem ocorrência da doença, segue-se para o alojamento total, suspensão da interdição e conclusão da investigação. |
| REGULAMENTAÇÃO OFICIAL | Instrução Normativa SDA nº 16 de 8 de maio de 2008: Instituí o Programa Nacional de Sanidade Apícola. |
|
LITERATURA CONSULTADA
|
Manual de Sanidade Apícola. Enero 2021. Disponível em: https://www.sag.gob.cl/sites/default/files/f_tecnica_loque_americana_ene-2021.pdf Manual Veterinário de colheita e envio de amostras: manual técnico. Capítulo 4: ABELHAS Apis mellifera Cooperação Técnica MAPA/OPAS PANAFTOSA Saúde Animal do Brasil. Disponível em: https://www.gov.br/agricultura/pt-br/assuntos/sanidade-animal-e-vegetal/saude-animal/programas-de-saude-animal/ManualdecolheitadeamostrasABELHAS.pdf OIE - Manual of Diagnostic Tests and Vaccines for Terrestrial Animals – Cap. 3.2.2. 2018. Disponível em: https://www.oie.int/fileadmin/Home/eng/Health_standards/tahm/3.02.02_AMERICAN_FOULBROOD.pdf OIE - Terrestrial Animal Health Code - Cap. 9.2. - 2019. Disponível em: https://www.oie.int/fileadmin/Home/eng/Health_standards/tahc/current/chapitre_paenibacillus_larvae.pdf |
ANEXOS:
_(pdf.io).jpg)
_(pdf.io)_(2).jpg)
_(pdf.io).jpg)
|
Infecção por Melissococcus plutonius (Cria pútrida europeia ou Loque europeia) |
|
|---|---|
| AGENTE |
A Loque Europeia ou Cria Pútrida Europeia é uma doença que ataca as larvas e pupas de abelhas. O agente causador é uma bactéria Melissococcus plutonius não formadora de esporos. Está espalhada por todo o globo, mas é considerada menos perigosa que a Loque Americana. Ainda assim, em algumas zonas e sob certas condições climáticas, a Loque Europeia pode causas grandes perdas de criação e consequentemente menores produções de mel, ou consequências mais graves como a morte de algumas colônias. Tem apresentado prejuízos em colmeias de Abelhas Nativas sem Ferrão. A doença não representa ameaça à saúde humana. |
| ESPÉCIES SUSCEPTÍVEIS |
Estágios de larva e pupa das abelhas da espécie Apis mellifera. Recentemente diagnosticada em algumas espécies de Abelhas Nativas sem Ferrão. Abelhas adultas, outras espécies de animais e o homem, não são susceptíveis. |
| POPULAÇÃO ALVO DO PROGRAMA DE VIGILÂNCIA | Colônias de abelhas. |
| COBERTURA GEOGRÁFICA | Áreas de exploração de meliponicultura e apicultura incluindo as áreas referentes às rotas de meliponicultura e apicultura migratória. |
|
SINAIS CLÍNICOS/LESÕES
|
Favos com muitas falhas, opérculos perfurados. A morte ocorre geralmente na fase de larva, antes que os alvéolos sejam operculados. Frequentemente, quando acomete as larvas, não permite a conclusão da metamorfose à pupa. As larvas doentes ficam em posições anormais, podendo ficar contorcidas, nas paredes dos alvéolos (fotos em Anexos). As larvas desoperculadas serão retiradas dos alvéolos pelas abelhas faxineiras sem necessidade de interferências nas estruturas das células. Quando as larvas morrem depois da operculação, aparecem opérculos escurecidos, afundados e perfurados. Mudança de cor das larvas que passam de branco pérola para amarelo até marrom, semelhante ao da Loque Americana. A putrefação das crias gera um odor pútrido de caráter ácido ou rançoso, embora haja casos em que não há nenhum cheiro. A grande diferença entre as duas loques é que na loque europeia a contaminação e morte ocorre na fase larval, enquanto, na loque americana, a contaminação ocorre na fase inicial de larva, mas a morte só ocorre na fase de pupa. Quando as abelhas operárias detectam larvas mortas, rapidamente elas limpam as células dos favos, então, observa-se a distribuição desuniforme das crias no favo. As larvas ficam flácidas, e formam um goma filamentosa inferior a 2,5 cm (filamento menor que o identificado na cria pútrida americana) quando tocadas com um palito. Outra característica é que é possível retirar com facilidade a larva de dentro do alvéolo, pois não fica grudada no fundo da célula como no caso da cria pútrida americana. |
| TRANSMISSÃO |
Semelhante a contaminação ocorrida na Loque Americana, a Loque Europeia também se instala com a ingestão de alimentos contaminados pelas larvas. Colônias capturadas em caixas-isca podem ser um vetor de transmissão da doença, caso estejam contaminadas. |
| CRITÉRIO DE NOTIFICAÇÃO | A Loque Europeia requer notificação imediata ao Serviço Veterinário Oficial de qualquer caso suspeito ou diagnóstico laboratorial positivo. |
| DIAGNÓSTICO DIFERENCIAL | Loque Americana, cria ensacada, cria morta pelo frio e cria giz. |
| RECOMENDAÇÃO PARA DIAGNÓSTICO LABORATORIAL | Confirmação diagnóstica através do isolamento por cultivo ou PCR. |
| LABORATÓRIO RECOMENDADO | Qualquer laboratório público ou privado, pertencente ou não a rede de laboratórios oficiais do Ministério da Agricultura, Pecuária e Abastecimento; |
| ORIENTAÇÃO PARA COLETA DE AMOSTRAS | Manual Veterinário de colheita e envio de amostras: manual técnico. Disponível em: https://www.gov.br/agricultura/pt-br/assuntos/sanidade-animal-e-vegetal/saude-animal/programas-de-saude-animal/ManualdecolheitadeamostrasABELHAS.pdf |
| AÇÕES RECOMENDADAS |
Remoção dos quadros com cria doente. Trocar rainha suscetível por outra mais resistente. Evitar uso de equipamentos contaminados quando manejar colmeias sadias. Não há tratamento específico para essa enfermidade. A doença já apresentou ocorrências em diversos pontos do país, o que caracteriza uma disseminação do agente. As implicações do uso de antibióticos são as mesmas já apresentadas para loque americana. Não existe nenhum medicamento aprovado para uso em colmeias no Brasil. O ideal é a eliminação dos materiais contaminados (favos de crias) e desinfecção das colmeias ou substituição dessas por estruturas novas, promovendo a esterilização e/ou o longo vazio sanitário nas contaminadas que foram retiradas do apiário. Evitar repovoamento de apiários por meio da captura de colônias naturais ou enxames em caixas-isca, ou quando capturar enxames na natureza submetê-los à quarentena em área separada antes de incorporar as novas colônias ao apiário. |
| REGULAMENTAÇÃO OFICIAL | Instrução Normativa SDA nº 16 de 8 de maio de 2008: Instituí o Programa Nacional de Sanidade Apícola. |
| LITERATURA CONSULTADA |
Manual Veterinário de colheita e envio de amostras: manual técnico. Capítulo 4: ABELHAS Apis mellifera Cooperação Técnica MAPA/OPAS PANAFTOSA Saúde Animal do Brasil. Disponível em: https://www.gov.br/agricultura/pt-br/assuntos/sanidade-animal-e-vegetal/saude-animal/programas-de-saude-animal/ManualdecolheitadeamostrasABELHAS.pdf OIE - Terrestrial Animal Health Code - Cap. 9.3. - 2019. Disponível em: https://www.oie.int/fileadmin/Home/eng/Health_standards/tahc/current/chapitre_melissococcus_plutonius.pdf OIE - Manual of Diagnostic Tests and Vaccines for Terrestrial Animals - Cap. 3.2.3. – 2018. Disponível em: https://www.oie.int/fileadmin/Home/eng/Health_standards/tahm/3.02.03_EUROPEAN_FOULBROOD.pdf SILVA, F. S. Revisão das Doenças que podem acometer Apis melífera. Universidade Federal do Rio Grande do Sul. Faculdade de Veterinária. Metodologia aplicada à conclusão do curso. Porto Alegre. 2010/2012. Disponível em https://www.lume.ufrgs.br/handle/10183/39035 |
ANEXOS:
_(1)_(pdf.io).jpg)
_page-0001.jpg)
|
Infestação por Tropilaelaps sp. (Tropilaelapsose) |
|
|---|---|
| AGENTE |
Família: Laelapidae Gênero: Tropilaelaps Espécie: Tropilaelaps mercedesae e Tropilaelaps clareae |
| ESPÉCIES SUSCEPTÍVEIS | Os ácaros infestam, principalmente, abelhas gigantes asiáticas Apis dorsata, Apis breviligula e Apis laboriosa. No entanto, após a introdução das abelhas Apis mellifera no continente asiático, o ácaro se propagou para essas colônias. |
| POPULAÇÃO ALVO DO PROGRAMA DE VIGILÂNCIA | Colônias de abelhas. |
| COBERTURA GEOGRÁFICA | Todas as áreas de exploração de apicultura, incluindo as áreas referentes às rotas de apicultura migratórias. |
| SINAIS CLÍNICOS/LESÕES |
Os danos causados pelo ácaro Tropilaelaps sp. permitem a entrada de outras infecções e vírus na colônia. A quantidade de Tropilaelaps sp. encontrados em colônias infestadas geralmente é maior do que a população de Varroa destructor. Após a operculação do alvéolo, a fêmea inicia a oviposição e parasita a larva/pupa. Quando infestada, os ácaros podem ser observados nas pupas operculadas. |
| TRANSMISSÃO |
Atualmente o ácaro se encontra somente em países do continente asiático e o risco de sua dispersão para outros continentes por meio da enxameação é baixo devido ao curto período de sobrevivência do ácaro nas abelhas adultas. As abelhas forrageiras atuam como meio de transporte do ácaro. Portanto, o contato físico entre as abelhas infestadas pode dar início à propagação do ácaro, como ocorre na enxameação. A troca de favos de uma colônia saudável com uma colônia infestada contribui para a propagação do parasita. Colônias capturadas em caixas-isca podem ser um vetor de transmissão da doença caso estejam contaminadas. |
| CRITÉRIO DE NOTIFICAÇÃO | A infestação por Tropilaelaps sp. requer notificação imediata ao Serviço Veterinário Oficial de qualquer caso suspeito ou diagnóstico laboratorial positivo. |
| DIAGNÓSTICO DIFERENCIAL | Pode ser confundido morfologicamente com o ácaro Varroa destructor que não atingiu a fase adulta. Porém, o ácaro Tropilaelaps sp possui cerca de 0,5 mm e o corpo mais alongado, enquanto a Varroa adulta pode chegar a 1,5 mm e o formato do corpo é ovalado (fotos em anexo). |
| RECOMENDAÇÃO PARA DIAGNÓSTICO LABORATORIAL |
Identificação dos ácaros através de caracteres morfológicos e microscopia de luz, OU; Análise molecular - Reação da cadeia da polimerase (PCR). Particularmente útil quando os espécimes estão danificados. |
| LABORATÓRIO RECOMENDADO | Laboratório a ser definido pelo Departamento de Saúde Animal e Coordenação Geral de Apoio Laboratorial DSA e CGAL/ MAPA em caso de ocorrência de suspeita. |
| ORIENTAÇÃO PARA COLHEITA DE AMOSTRAS |
Manual Veterinário de colheita e envio de amostras: manual técnico. Disponível em: https://www.gov.br/agricultura/pt-br/assuntos/sanidade-animal-e-vegetal/saude-animal/programas-de-saude-animal/ManualdecolheitadeamostrasABELHAS.pdf Coletar amostras de pupas infestadas para identificação morfológica ou PCR do ácaro. Os espécimes devem ser coletados e acondicionados em frasco limpo e bem fechado contendo álcool 70%. Essa forma de conservação permite a análise tanto por análise molecular quanto a identificação morfológica. As amostras podem ser armazenadas e enviadas ao laboratório em temperatura ambiente. |
| MEDIDAS A SEREM APLICADAS |
Imediatamente após a notificação da suspeita da doença, o serviço oficial de defesa sanitária deve adotar todos os procedimentos de investigação epidemiológica, estabelecer uma zona de vigilância, e adotar ações de restrição de trânsito de colmeias de Apis mellifera e produtos de risco. Destruição do material vivo e inerte infectado, através da queima das colônias infectadas, enquanto as caixas e as melgueiras podem ser passados a fogo (utilizando um maçarico, por exemplo) para seu reaproveitamento. Somente o conteúdo do interior (abelhas e favos) deve ser destruído. Investigação epidemiológica, ampliação da vigilância, identificando os contatos diretos do apiário foco, apiários de outros proprietários, compra e venda de materiais vivos e inertes, e os contatos com parceiros polinizadores. Manter as colônias fortes, selecionando-as para comportamento higiênico, aumentando as chances de eliminação de larvas e pupas infestadas com o ácaro, por parte das abelhas. Ações preventivas como boas práticas de manejo apícola; medidas de vigilância para detecção precoce; controle do ingresso de abelhas e seus produtos quando oriundos de locais onde já foi detectada sua presença. |
| PRAZO PARA ENCERRAMENTO DE FOCO/CONCLUSÃO DAS INVESTIGAÇÕES |
30 dias após a destruição de todo o material infectado (vivo e inerte), inicia o repovoamento das colmeias com o alojamento de 10 % da população inicial. Após 30 dias sem ocorrência da doença, segue-se para o alojamento total, suspensão da interdição e conclusão da investigação. Preencher o Form-Com de encerramento e finalizar a investigação. |
| REGULAMENTAÇÃO OFICIAL | Instrução Normativa SDA nº 16 de 8 de maio de 2008: Instituiu o Programa Nacional de Sanidade Apícola. |
| LITERATURA CONSULTADA |
ANDERSON, D. L.; ROBERTS, J. M. K. Standard methods for Tropilaelaps mies research. Journal of Apicultural Research, v. 52, n. 4, p. 1-16, 2013. doi: 10.3896/IBRA.1.52.4.21 Disponível em: https://www.tandfonline.com/doi/pdf/10.3896/IBRA.1.52.4.21?needAccess=true ANDERSON, D. L; MORGAN, M. J. Genetic and morphological variation of bee-parasitic Tropilaelaps mites (Acari: Laelapidae): new and re-defined species. Experimental and Applied Acarology, v. 43, p. 1-24, 2007. DE MIRANDA, J. R.; BAILEY, L.; BALL, B. V.; BLANCHARD, P.; BUDGE, G.; CHEJANOVSKY, N.; VAN DER STEEN, J. J. M. Standard methods for virus research in Apis mellifera. Journal of Apicultural Research, v. 52, n. 4, p. 1-56, 2013. OIE - Manual of Diagnostic Tests and Vaccines for Terrestrial Animals - Cap. 3.2.6. – 2018. Disponível em: https://www.oie.int/fileadmin/Home/eng/Health_standards/tahm/3.02.06_TROPILAELAPS.pdf |
ANEXO
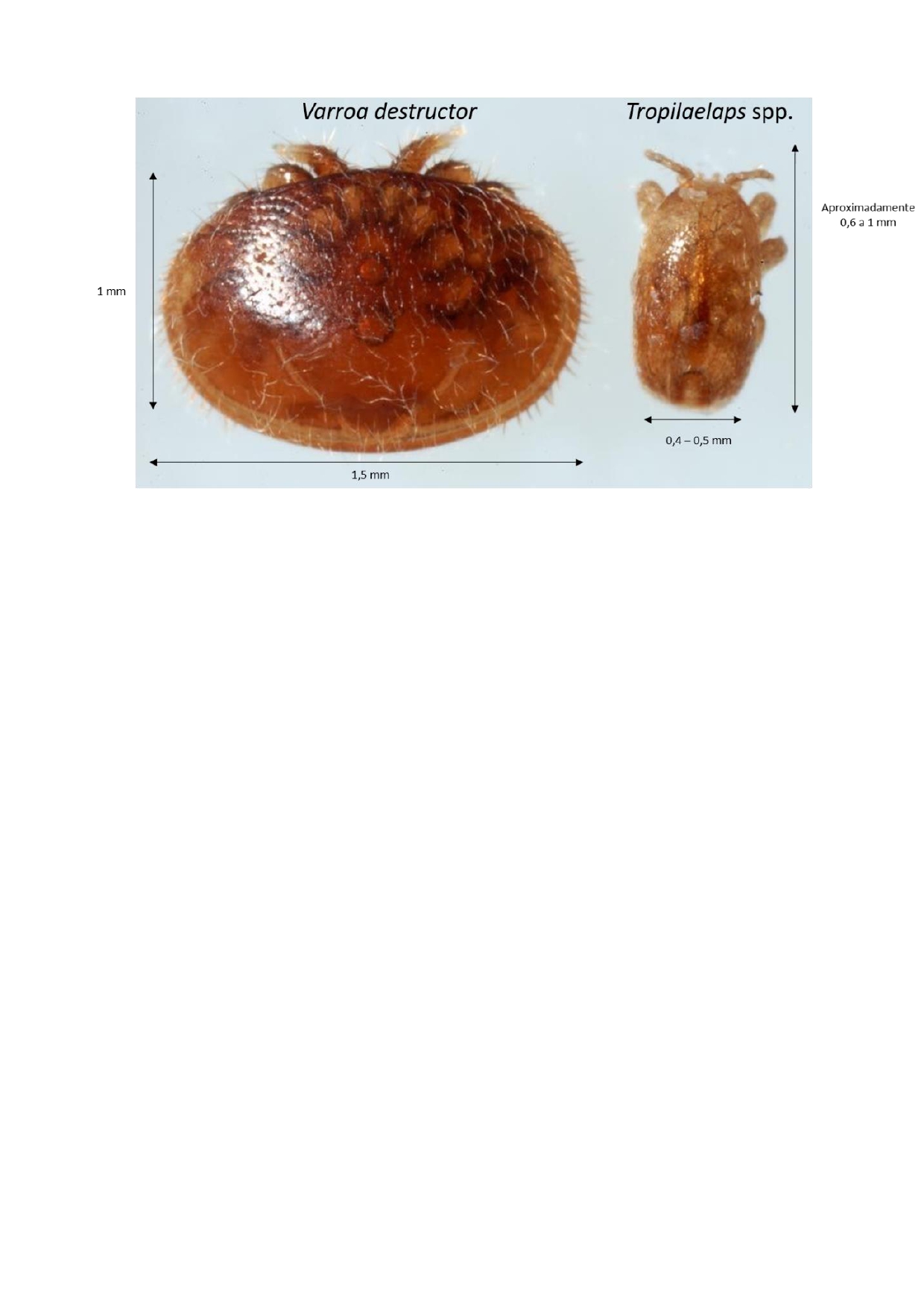
|
Infestação por Acarapis woodi (Acariose) |
|
|---|---|
| AGENTE |
Família: Tarsonemidae Gênero: Acarapis Espécie: Acarapis woodi (Rennie, 1921) |
| ESPÉCIES SUSCEPTÍVEIS | Os ácaros infestam, principalmente, colônias de abelhas da espécie Apis mellifera. |
| POPULAÇÃO ALVO DO PROGRAMA DE VIGILÂNCIA | Colônias de abelhas. |
|
COBERTURA GEOGRÁFICA
|
Todas as áreas de exploração de apicultura, incluindo as áreas referentes às rotas de apicultura migratórias. Já foi um problema no passado, porém, não mais relatada em trabalhos científicos recentes no Brasil. |
|
SINAIS CLÍNICOS/LESÕES
|
Sintomas difíceis de se detectarem. Abelhas com asas disjuntas e abdômen inchado impossibilitadas de voar. Em elevada infestação: traqueias das abelhas encontram-se claramente necrosadas e enegrecidas quando comparadas com traqueias saudáveis. Abelhas rastejando na frente da colmeia e no alvado, buscando subir nas folhagens na tentativa de alçar voo. |
| TRANSMISSÃO |
Trata-se de um ácaro que vive nas traqueias toráxicas das abelhas onde completa seu ciclo reprodutivo. O contágio ocorre por meio do contato físico entre uma abelha infestada com as demais abelhas da colônia, principalmente quando é realizada a trofaláxis (troca de alimento entre as operárias). As abelhas recém emergidas são mais susceptíveis. Colônias capturadas em caixas-isca podem ser um vetor de transmissão da doença caso estejam contaminadas. |
| CRITÉRIO DE NOTIFICAÇÃO | A infestação pelo ácaro – Acarapis woodi requer notificação obrigatória ao Serviço Veterinário Oficial de qualquer caso confirmado. |
| DIAGNÓSTICO DIFERENCIAL |
No campo é impossível de serem observados estes ácaros a olho nu. Seus sintomas podem se confundir com nosemose, porém na acariose as abelhas são mais ativas. Em intoxicações os movimentos das abelhas são mais erráticos, o sistema de defesa fica comprometido, e podem ser observadas abelhas limpando a glossa (língua) com as pernas anteriores, características que não aparecem nos casos de acariose. |
| RECOMENDAÇÃO PARA DIAGNÓSTICO LABORATORIAL | Confirmação diagnóstica através de identificação dos ácaros presentes nas traqueias de abelhas operárias. |
| LABORATÓRIO RECOMENDADO | Qualquer laboratório público ou privado, pertencente ou não a rede de laboratórios oficiais do Ministério da Agricultura, Pecuária e Abastecimento |
| ORIENTAÇÃO PARA COLETA DE AMOSTRAS |
As abelhas sintomáticas devem ser coletadas e acondicionados em frasco limpo e bem fechado contendo álcool 70 %. Essa forma de conservação permite a identificação dos ácaros presentes nas traqueias de abelhas operárias. Manual Veterinário de coleta e envio de amostras: manual técnico. Cooperação Técnica MAPA/OPAS PANAFTOSA Saúde Animal do Brasil. Disponível em: http://iris.paho.org/xmlui/handle/123456789/33893 |
| AÇÕES RECOMENDADAS |
Manter as colônias fortes. Ações preventivas como boas práticas de manejo apícola. Evitar repovoamento de apiários por meio da captura de colônias naturais ou enxames em caixas-isca, ou quando capturar enxames na natureza submetê-los à quarentena em área separada antes de incorporar as novas colônias ao apiário. |
| PRAZO PARA ENCERRAMENTO DE FOCO/CONCLUSÃO DAS INVESTIGAÇÕES | Não se aplica. |
| LITERATURA CONSULTADA |
Código Sanitário Animais Terrestres - OIE - Cap. 9.1 – 2018. CAP- Departamento Técnico. Manual de Sanidade Apícola, Sintomas – Profilaxia – Controlo, FNAP – Federação Nacional dos Apicultores de Portugal, 2007. Disponível em < http://fnap.pt/web/wp-content/uploads/documento_cnt_projectos_127.pdf > Acesso em: 20/08/2020. CELLA, I; CUNHA, R. D.; SEZERINO, A. A.; SATTLER, A.; COAN, L. F. B.; SCASSO, R. E. Manejos para o controle de doenças, pragas e predadores das abelhas no sul do Brasil. Florianópolis: Epagri, 2020. 72 p. (Boletim Didático, 151). |
|
Infecção por Ascosphaera apis (Cria giz) |
|
|---|---|
| AGENTE |
Família: Ascosphaeraceae Gênero: Ascosphaera Espécie: Ascosphaera apis (SPILTOIR, 1955; SPILTOIR & OLIVE, 1955) Também conhecida por cria giz. A doença não representa ameaça à saúde humana. |
| ESPÉCIES SUSCEPTÍVEIS | Primeiramente descrito infectando abelhas da espécie Apis mellifera e, posteriormente, abelhas Apis cerana e Xylocopa sp. |
| POPULAÇÃO ALVO DO PROGRAMA DE VIGILÂNCIA | Colônias de abelhas. |
| COBERTURA GEOGRÁFICA | Áreas de exploração de apicultura incluindo as áreas referentes às rotas de apicultura migratória. |
|
SINAIS CLÍNICOS/LESÕES
|
Crias com aspectos mumificados, bem como cria falhada (alvéolos vazios nos favos de cria). Em casos de crias infectadas durante a operculação do alvéolo, ao sacudir o favo é possível escutar um barulho lembrando um chocalho, devido ao choque das larvas secas contra as paredes do alvéolo. Em colônias com alta taxa de comportamento higiênico é possível observar as crias infectadas removidas no alvado da colmeia ou no solo abaixo do alvado. Normalmente, a letalidade da cria giz é baixa em colônias higiênicas, embora a presença do fungo provoque uma queda na quantidade de cria. |
| TRANSMISSÃO |
A contaminação pelo fungo A. apis ocorre via alimentação larval contaminada com esporos. O fungo infesta o intestino médio da larva competindo pelos nutrientes, provocando a morte da larva por desnutrição. Após a morte da larva, o fungo se alimenta dos órgãos internos da larva, deixando a larva desidratada com aspecto mumificado, com aparência de giz. Larvas no 5° instar (etapas dos estágios larvais, delimitado pelo período entre duas mudas) são as mais susceptíveis à infecção. Como há formação de esporos, o manejo de favos entre uma colônia e outra e o contato com qualquer material contaminado podem auxiliar na propagação da doença para outras colônias. Colônias capturadas em caixas-isca podem ser um vetor de transmissão da doença caso estejam contaminadas. |
| CRITÉRIO DE NOTIFICAÇÃO | A cria giz requer notificação de qualquer caso confirmado ao Serviço Veterinário Oficial. |
| DIAGNÓSTICO DIFERENCIAL | O sintoma de cria falhada (alvéolos vazios nos favos de cria), pode ser confundido com loque europeia, loque americana, cria ensacada e morte pelo frio, pois quando as abelhas reconhecem algum problema removem as crias suspeitas. |
| RECOMENDAÇÃO PARA DIAGNÓSTICO LABORATORIAL | O diagnóstico laboratorial é realizado por meio da microscopia, onde é possível observar o micélio do fungo. |
| LABORATÓRIO RECOMENDADO | Qualquer laboratório público ou privado, pertencente ou não a rede de laboratórios oficiais do Ministério da Agricultura, Pecuária e Abastecimento. |
| ORIENTAÇÃO PARA COLETA DE AMOSTRAS | Manual Veterinário de coleta e envio de amostras: manual técnico. Cooperação Técnica MAPA/OPAS PANAFTOSA Saúde Animal do Brasil. Disponível em: http://iris.paho.org/xmlui/handle/123456789/33893 |
| AÇÕES RECOMENDADAS |
Seleção de colônias com maior taxa de comportamento higiênico e resistência a doenças. Evitar repovoamento de apiários por meio da captura de colônias naturais ou enxames em caixas-isca, ou quando capturar enxames na natureza submetê-los à quarentena em área separada antes de incorporar as novas colônias ao apiário. |
| PRAZO PARA ENCERRAMENTO DE FOCO / CONCLUSÃO DAS INVESTIGAÇÕES | Não se aplica. |
| LITERATURA CONSULTADA |
ARONSTEIN, K.A.; MURRAY, K.D. Chalkbrood disease in honey bees, Journal of Invertebrate Pathology, 103(1), s20-s29, 2010. CHEN, D.; GUO, R.; XIONG, C.; ZHENG, Y.; HOU, C.; FU, Z. Morphological and molecular identification of chalkbrood disease pathogen Ascosphaera apis in Apis cerana cerana. Journal of Apicultural Research, 57(4), 2018. FLORES, J.M.; SPIVAK, M.; GUTIÉRREZ, I. Spores of Ascosphaera apis contained in wax foundation can infect honeybee brood. Veterinary Biology,108, 141-144, 2005. HEATH, L.A.F. Development of chalkbrood in a honeybee colony: a review. Bee World, 63, 119-130, 1982 HORNITZKY, M. Literature review of chalkbrood. A report for the RIRDC, 842, 2001. Manual Veterinário de colheita e envio de amostras: manual técnico. Capítulo 4: ABELHAS Apis mellifera Cooperação Técnica MAPA/OPAS PANAFTOSA Saúde Animal do Brasil. Disponível em: https://www.gov.br/agricultura/pt-br/assuntos/sanidade-animal-e-vegetal/saude-animal/programas-de-saude-animal/ManualdecolheitadeamostrasABELHAS.pdf OIE - Código Zoossanitário dos Animais Terrestres-. 2019. Disponível em: https://www.oie.int/index.php?id=169&L=0&htmfile=chapitre_paenibacillus_larvae.htm OIE - Manual de Testes Diagnósticos e Vacinas para Animais Terrestres. 2019. Disponível em: https://www.oie.int/en/standard-setting/terrestrial-manual/access-online/ |
|
Infestação por Varroa destructor (Varroose) |
|
|---|---|
| AGENTE |
Família: Varroidae Gênero: Varroa Espécie: Varroa destructor ( Anderson e Trueman, 2000) |
| ESPÉCIES SUSCEPTÍVEIS | Os ácaros infestam, principalmente, colônia de abelhas da espécie Apis mellifera. |
| POPULAÇÃO ALVO DO PROGRAMA DE VIGILÂNCIA | Colônias de abelhas. |
| COBERTURA GEOGRÁFICA | Todas as áreas de exploração de apicultura, incluindo as áreas referentes às rotas de apicultura migratórias. |
|
SINAIS CLÍNICOS/LESÕES
|
Parasita abelhas em duas fases: crias na fase pupal e em abelhas adultas. Sinais clínicos da fase de cria: cria fechada com um rasgo na borda do opérculo, ou um furo no centro pode indicar que a cria está infestada com o ácaro varroa, embora este sinal também pode indicar que a cria esteja morta; quadros de cria apresentam-se com o aspecto em mosaico ou com a disposição dos opérculos não uniformes; área de cria falhada ou salteada; larvas mortas castanhas ou castanhas claras e larvas mortas secas. Sinais clínicos em abelhas adultas: Asas deformadas e/ou atrofiadas; abelhas com abdômen menores, apresentando peso mais baixo ao emergirem dos alvéolos; presença do ácaro sobre as abelhas, geralmente no tórax. Parasita das abelhas melíferas que pode ser visto a olho nu. |
| TRANSMISSÃO |
O ácaro Varroa é encontrado em todo o ambiente onde vivem as abelhas. Esta doença entra em uma colônia saudável por meio da deriva de operárias campeiras parasitadas. São ácaros levados a outras colônias, especialmente pelos zangões que têm entrada livre em todas as colônias. Podem permanecerem por até 114 horas com vida sobre uma flor esperando a visita das abelhas. Os ácaros caminham e sobem nas abelhas, podendo ser visíveis no tórax das abelhas. Colônias capturadas em caixas-isca podem ser um vetor de transmissão da doença caso estejam contaminadas. Divisão e união de colônias infestadas pelo ácaro. |
| CRITÉRIO DE NOTIFICAÇÃO | A infestação pelo ácaro Varroa destructor requer notificação obrigatória ao Serviço Veterinário Oficial de qualquer caso confirmado. |
| DIAGNÓSTICO DIFERENCIAL |
Outras espécies de ácaro que apresentam características morfológicas semelhantes, como o Tropilaelaps spp, considerado exótico no Brasil até o momento. O diagnóstico para varroose pode ser qualitativo ou quantitativo. Diagnóstico qualitativo: observação do ácaro adulto sobre o corpo das operárias no momento da observação dos favos de cria das colônias; retirada das pupas de zangão de dentro dos alvéolos, para observar o ácaro. Verificar se há varroas mortas no fundo da colmeia. Diagnóstico quantitativo: contagem de ácaros adultos sobre o corpo das operárias para determinar a porcentagem de abelhas parasitadas na colônia. O processo deve ser realizado em pelo menos três colônias, ou em 10% das colônias do apiário, escolhidas de forma aleatória. |
| RECOMENDAÇÃO PARA DIAGNÓSTICO LABORATORIAL | Identificação do ácaro através de caracteres morfológicos. O ácaro fêmea é de cor marrom-avermelhada escuro e tem corpo achatado e oval de aproximadamente 1,1 mm × 1,5 mm. |
| LABORATÓRIO RECOMENDADO | Qualquer laboratório público ou privado, pertencente ou não a rede de laboratórios oficiais do Ministério da Agricultura, Pecuária e Abastecimento. |
| ORIENTAÇÃO PARA COLETA DE AMOSTRAS |
Coleta de amostra de abelhas utilizando álcool para desprender as varroas das abelhas: acondicionar em um frasco com tampa (cerca de 1/3 da capacidade do frasco) álcool a 70%, podendo ser utilizado um pote de plástico de 500 mL e adicione 5 gotas de detergente; colete entre 100 e 300 abelhas jovens que estejam aderidas a três quadros de cria diferentes; numere o frasco, identificando a colônia da qual as abelhas foram coletadas; feche o frasco, realizar agitação mecânica por aproximadamente dois minutos para que os ácaros se desprendam do corpo das abelhas; separe os ácaros das abelhas com a ajuda de uma tela; conte o número de abelhas e de ácaros e anote. Coleta de amostra de abelhas quando se utiliza água quente para desprender as varroas das abelhas: Colocar água fria em um frasco com tampa (no mínimo 1/3 da capacidade do frasco), podendo ser utilizado um pote de plástico de 500 mL; colete no mínimo 150 abelhas jovens que estejam aderidas a três quadros de cria diferentes; numerar o frasco, identificando a colônia da qual as abelhas foram coletadas; em outro local, substitua a água fria do pote por água quente, com um volume que atinja, no mínimo, 2/3 do pote; feche o frasco, agite um pouco e espere no mínimo 10 minutos para os ácaros se desprenderem das abelhas; agite o frasco e separe os ácaros das abelhas com a ajuda de uma tela ou retire as abelhas do pote com o auxílio de uma pinça ou outro objeto; conte o número de abelhas e anote no papel; conte os ácaros e anote no papel. A utilização de um pano branco facilita a visualização das varroas. Para encontrar a porcentagem de infestação com varroa, conta-se o número de ácaros, divide-se pelo número de abelhas e multiplica-se por 100. Índice tolerável de infestação de varroa: menor que 10% não foi relatado na literatura prejuízo econômico; Na entressafra: até 7% em abelhas operárias; Na safra: até 3% em abelhas operárias. |
| AÇÕES RECOMENDADAS |
Manter as colônias fortes, selecionando-as para maior comportamento higiênico, aumentando as chances de controle do ácaro por parte das abelhas. Aplicação de boas práticas de manejo apícola. Evitar repovoamento de apiários por meio da captura de colônias naturais ou enxames em caixas-isca, ou quando capturar enxames na natureza submetê-los à quarentena em área separada antes de incorporar as novas colônias ao apiário. A utilização excessiva pelos apicultores de produtos previstos na IN 46/2011 (apicultura orgânica) para controle do ácaro pode deixar resíduos nos produtos das abelhas, além de mascarar a doença, dificultando a seleção de enxames com melhores hábitos higiênicos e mais resistentes à varroose. |
| PRAZO PARA ENCERRAMENTO DE FOCO/CONCLUSÃO DAS INVESTIGAÇÕES | Não se aplica. |
| LITERATURA CONSULTADA |
ANDERSON D.L. & TRUEMAN J.W.H. (2000). Varroa jacobsoni (Acari: Varroidae) is more than one species. Exp. Appl. Acarol., 24, 165–189. Código Sanitário Animais Terrestres - OIE - Cap. 9.6 – 2018. RAMSEY, SD., OCHOA, R., BAUCHAN, G. et al. (2019). Varroa destructor feeds primarily on honey bee fat body tissue and not hemolymph. Proc Natl Acad Sci USA 116:1792–1801. https://doi.org/10.1073/pnas.1818371116. ROSENKRANZ, P., AUMEIER, P., & ZIEGELMANN, B. (2010). Biology and control of Varroa destructor. Journal of Invertebrate Pathology, 103, S96–S119. doi:10.1016/j.jip.2009.07.016 |
|
Infecção por Nosema sp. (Nosemose) |
|
|---|---|
| AGENTE |
Família: Nosematidae Gênero: Nosema Espécie: Nosema apis Zander, 1909 e N. ceranae Fries et al., 1996 Também conhecida por Nosemose. Causa graves perdas econômicas em países de clima temperado. A doença não representa ameaça à saúde humana. |
| ESPÉCIES SUSCEPTÍVEIS | Abelhas adultas da espécie Apis mellifera são as mais suscetíveis. |
| POPULAÇÃO ALVO DO PROGRAMA DE VIGILÂNCIA | Colônias de abelhas. |
| COBERTURA GEOGRÁFICA | Áreas de exploração de apicultura incluindo as áreas referentes às rotas de apicultura migratória. |
|
SINAIS CLÍNICOS/LESÕES
|
Aparecimento de manchas de cor escura no exterior da colônia, indicando o principal sintoma da dificuldade de assimilação alimentar, que é a diarreia. Em colônias com alta infecção por Nosema apis é comum observar fezes no interior da colmeia e no alvado. No entanto, para Nosema ceranae este sintoma não se confirmou. Sintomas inespecíficos como tremores e desorientação parecem estar mais associados com as colônias infectadas por N. ceranae. Alguns trabalhos sugerem, além de doença entérica, a afecção (edema) do pênis de zangões. |
| TRANSMISSÃO |
A infecção por nosemose ocorre no trato digestivo devido à alimentação contaminada com esporos. Os esporos de Nosema se desenvolvem melhor no intestino de abelhas com mais de 15 dias de vida. Ao entrar no organismo do hospedeiro, os esporos danificam a parede epitelial do intestino, dificultando a digestão e absorção dos nutrientes da dieta. Os esporos também podem ser transmitidos pelas abelhas adultas encarregadas da limpeza dos favos e por meio da trofalaxia (processo de troca de alimento entre as abelhas). Colônias capturadas em caixas-isca podem ser um vetor de transmissão da doença caso estejam contaminadas. |
| CRITÉRIO DE NOTIFICAÇÃO | A Nosemose requer notificação de qualquer caso confirmado ao Serviço Veterinário Oficial. |
| DIAGNÓSTICO DIFERENCIAL | O sintoma mais evidente é a diarreia no interior e frente da colmeia. No entanto, esse sintoma não é exclusivo dessa doença, podendo ser ocasionado também pelo consumo de xarope fermentado pelas abelhas e outras enfermidades. Além disso, as abelhas podem apresentar tremores, dificuldade para voar, rastejar pelos favos, que também são sintomas provocados por alguns vírus e intoxicações. |
| RECOMENDAÇÃO PARA DIAGNÓSTICO LABORATORIAL | Confirmação diagnóstica através de microscopia e análise molecular com identificação de Nosema por reações de PCR. |
| LABORATÓRIO RECOMENDADO | Qualquer laboratório público ou privado, pertencente ou não a rede de laboratórios oficiais do Ministério da Agricultura, Pecuária e Abastecimento. |
| ORIENTAÇÃO PARA COLETA DE AMOSTRAS |
Manual Veterinário de colheita e envio de amostras: manual técnico. Cooperação Técnica MAPA/OPAS PANAFTOSA Saúde Animal do Brasil. Disponível em: http://iris.paho.org/xmlui/handle/123456789/33893 Deve-se coletar abelhas forrageiras (abelhas acima de 20 dias de idade) que estão retornando do voo, pois são as abelhas que apresentam maior nível facilmente detectável de infecção por nosema. Para coleta, utilizar tela de tule ou outro tecido maleável, colocada no alvado da colmeia a ser analisada de maneira impedir a entrada das abelhas (Anexo). As abelhas forrageiras retornando do campo pousam na tela e podem ser coletadas utilizando um recipiente plástico contendo álcool 70%. |
| AÇÕES RECOMENDADAS |
As medidas de prevenção da Nosemose deverão ser efetuadas no final do outono, de forma a preparar as abelhas para o período do inverno em que há maior coesão para controle de temperatura (o que potencializa a contaminação). Recomenda-se evitar deixar, no apiário, recipientes com água que possam receber fezes de abelhas doentes e contaminar outras abelhas que acabem utilizando-o para coleta de água e refrigeração do ninho. É importante controlar infestações de mariposas de traças da cera, pois essas voam de colmeias em colmeias depositando seus ovos, e por isso podem servir com carreadores de fungos no seu corpo e asas. Evitar repovoamento de apiários por meio da captura de colônias naturais ou enxames em caixas-isca, ou quando capturar enxames na natureza submetê-los à quarentena em área separada antes de incorporar as novas colônias ao apiário. |
| PRAZO PARA ENCERRAMENTO DE FOCO/CONCLUSÃO DAS INVESTIGAÇÕES | Não se aplica. |
| LITERATURA CONSULTADA |
OIE - Manual de Testes Diagnósticos e Vacinas para Animais Terrestres. 2018. Disponível em: https://www.oie.int/fileadmin/Home/eng/Health_standards/tahm/3.02.04_NOSEMOSIS_FINAL.pdf FNAP – Federação Nacional dos Apicultores de Portugal. 2007. Manual de Sanidade Apícola Ficha Técnica – Nosemose. Disponível em http://fnap.pt/web/wp-content/uploads/documento_cnt_projectos_127.pdf Manual Veterinário de colheita e envio de amostras: manual técnico. Capítulo 4: ABELHAS Apis mellifera Cooperação Técnica MAPA/OPAS PANAFTOSA Saúde Animal do Brasil. Disponível em: https://www.gov.br/agricultura/pt-br/assuntos/sanidade-animal-e-vegetal/saude-animal/programas-de-saude-animal/ManualdecolheitadeamostrasABELHAS.pdf GUIMARÃES-CESTARO, L.; SERRÃO, J. E.; MESSAGE, D.; MARTINS, M. F.; TEIXEIRA, E.W. Simultaneous detection of Nosema spp., Ascosphaera apis and Paenibacillus larvae in honey bee products. Journal of Hymenoptera Research, v. 49, p. 43-50, 2016. SILVA, Felipe Silveira da. Revisão das Doenças que podem acometer Apis mellifera. 2010. Monografia de conclusão de curso – Faculdade de Veterinária, Universidade Federal do Rio Grande do Sul, 2010. TEIXEIRA, E. W.; SANTOS, L. G.; SATTLER, A.; MESSAGE, D.; ALVES, M. L. T. M. F.; MARTINS, M. F.; GRASSI-SELLA, M. F.; FRANCOY, T. M. Nosema ceranae has been present in Brazil for more than three decades infecting Africanized honey bees. Journal of Invertebrate Pathology, v. 114, p. 250-254, 2013. |
ANEXOS:

¶ Base legal e documentos de referência
- ABOU-SHAARA, H. F. Notes on water collection by honeybees. Bee World, v. 89, n. 4, p. 86-87, 2012.
- ADAB. Agência Estadual de Defesa Agropecuária da Bahia. Regulamento técnico de identidade e qualidade do mel de abelha social sem ferrão gênero Melipona. Portaria ADAB Nº 207 de 21 de novembro de 2014. Disponível em: https://www.legisweb.com.br/legislacao/?id=277684. Acesso em: 04 set. 2020
- ADAPAR/PR. Agência De Defesa Agropecuária Do Paraná. Regulamento Técnico de Identidade e Qualidade do Mel de Abelhas Sem Ferrão para o Estado do Paraná. Portaria
- n° 63 de 10 de março de 2017. Disponível em: http://www.adapar.pr.gov.br/arquivos/File/GABINETE/PORTARIAS/2017/63_17.pdf. Acesso em: 04 set. 2020. 00
- ADAMOU, M., & TCHUENGUEM FOHOUO, F. N. Foraging and pollination behavior of Apis mellifera adansonii Latreille (Hymenoptera, Apidae) on Brachiaria brizantha (Hochst. Ex A. Rich.) Stapf. 1919 flowers at Dang (Ngaoundere-Cameroon). Int J. Agro. Agric Res, 6(4), p. 62-74, 2014.
- ALLEN, M.; BALL, B. The incidence and world distribution of the honey bee viruses. Bee World, v. 77, p. 141–162, 1996. doi: 10.1080/0005772X.1996.11099306
- ANDERSON, D. L. Pathogens and queen bees. Australasian Beekeeper, v. 94, p. 292–296, 1993.
- ANDERSON, D. L.; ROBERTS, J. M. K. Standard methods for Tropilaelaps mites research. Journal of Apicultural Research, v. 52, n. 4, p. 1-16, 2013. doi: 10.3896/IBRA.1.52.4.21
- ARAI, R.; TOMINAGA, K.; WU, M.; OKURA, M.; ITO, K.; OKAMURA, N.; ONISHI, H.; OSAKI, M.; SUGIMURA, Y.; YOSHIYAMA, M.; TAKAMATSU, D. Diversity of Melissococcus plutonius from honey bee larvae in Japan and experimental reproduction of European foulbrood with cultured atypical isolates. PLoS One, v. 7, n. 3, p. e33708, 2012. doi: 10.1371/journal.pone.0033708
- ALICE PINTO, M.; SHEPPARD, W. S.; JOHNSTON, J. S.; RUBINK, W. L.; COULSON, R. N.; SCHIFF, N. M.; KANDEMIR, I.; PATTON, J. C. Honey bees (Hymenoptera: Apidae) of African origin exist in non-Africanized areas of the southern United States: evidence from mitochondrial DNA. Annals of the Entomological Society of America, v. 100, edição 2, p. 289-295, 2007.
- ARONSTEIN, K. A.; MURRAY, K. D. Chalkbrood disease in honey bees, Journal of Invertebrate Pathology, v. 103, n. 1, p. s20-s29, 2010. doi: 10.1016/j.jip.2009.06.018
- ARONSTEIN, K. A.; MURRAY, K. D.; SALDIVAR, E. Transcriptional responses in honey bee larvae infected with chalkbrood fungus. BMC Genomics, v. 11, n., 391, 2010. doi: 10.1186/1471-2164-11-391
- ASSAD, A. L. D.; ROCHA NETO, A. C. da.; MARINHO, B.; REHDER, C. P.; MATOS, C.; MENEZES, C.; BASSO, E. C.; KORS, J. A. M.; BRUNELLI JÚNIOR, J.; PIMENTEL, J. C. de C.; FONTES, J. L.; ALEIXO, K.; BARRETO, L.; GUIDO, M. C.; NICODEMO, M. L. F.; TAVEIRA, R. S.; CARVALHO, W. A. F. de. Plano de fortalecimento da cadeia produtiva da apicultura e da meliponicultura do Estado de São Paulo. São Paulo: Secretaria de Estado de Agricultura e Abastecimento, Embrapa Pecuária Sudeste - Outras publicações técnicas (INFOTECA-E), 2018. 60 p.
- ADLER, S.A. The ecological significance of toxic nectar. Oikos, n.91, p.409-420, 200
- AGROFIT. 2020. Disponível em: <http://extranet.agricultura.gov.br/agrofit_cons/principal_agrofit_cons>. Acesso em: 21 de ago. de 2020
- ALVES, M.M.B.M.; ALVES JUNIOR, V.V.; LOPES, M.N.T.; CARBONARI, V. Efeito do resíduo de extrato floral de Barbatimão, em soro fisiológico, na longevidade de Apis mellifera. In: CONGRESSO BRASILEIRO DE APICULTURA, 11., 1996, Teresina. Anais [...]. Teresina, 1996. p.325.
- ALVES, M.M.B.M.V.; C ARBONARI, V.; A LVES JUNIOR, V.V. Efeito tóxico do barbatimão (extrato/nectário em água destilada) na longevidade de abelhas operárias Apis mellifera confinadas. In: ENCONTRO DE BIÓLOGOS DA 1º REGIÃO DO CONSELHO REGIONAL DE BIOLOGIA, 9., 1998, Campo Grande. Anais [...]. Campo Grande, 1998. p.66.
- AGÊNCIA NACIONAL DE VIGILÂNCIA SANITÁRIA (ANVISA). Índice monográfico F43: Fipronil, 2016. Disponível em: <http://portal.anvisa.gov.br/documents/10181/2822901/CONSULTA+P%C3%9 ABLICA+N+201+GGTOX.pdf/dc7c63e0-9ae5-400a-ba85-5161ba95248a>. Acesso em: 21 de ago. de 2020.
- BALBINO, V. A.; BINOTTO, E.; SIQUEIRA, E. S. Apicultura e Responsabilidade Social: Desafios da Produção e Dificuldades em Adotar Práticas Social e Ambientalmente Responsáveis. REAd. Revista Eletrônica de Administração, Porto Alegre, v. 21, n. 2, p. 348-377, 2015.
- DOI: https://doi.org/10.1590/1413-2311.0442013.44185. Disponível em: https://www.scielo.br/scielo.php?script=sci_arttext&pid=S1413-23112015000200348&lng=pt&tlng=pt. Acesso em: 06 outubro 2020
- BAILEY, L. Acarapis woodi: a modern appraisal. Bee World, v. 66, n. 3, p. 99-104, 1985. doi: 10.1080/0005772X.1985.11098831
- BAILEY, L. Recent research on honey bee viruses. Bee World, v. 56, p. 55–64, 1975. doi: 10.1080/0005772X.1975.11097544
- BAILEY, L. Susceptibility of the honey bee, Apis mellifera Linnaeus, infested with Acarapis woodi (Rennie) to infection by airborne pathogens. Journal of Invertebrate Pathology, v. 7, p. 141-143, 1965.
- BAILEY, L. The multipliction and spread of sacbrood virus of bees. Annals of Applied Biology, v. 63, p. 483-491, 1969. doi: 10.1111/j.1744-7348.1969.tb02844.x
- BAILEY, L.; BALL, B. V. Honey Bee pathology, 2ª ed. Londres: Academic Press, 1991.
- BAILEY, L., GIBBS, A. J. and Woods, R. D. Two viruses from the adult honey bee (Apis mellifera Linnaeus). Virology v. 21, p. 390395, 1963.
- BAILEY, L.; WOODS, R. D. Two more small RNA viruses from honey bees and further observations on sacbrood and acute bee-paralysis viruses. Journal of General Virology, v. 25, p. 175–186, 1977. doi: 10.1099/0022-1317-37-1-175
- BALLIVIÁN, J. M. P. P. Abelhas nativas sem ferrão. São Leopoldo: Oikos, 2008. 128 p.
- BALL, B. V. Acute paralysis virus isolates from honeybee colonies infested with Varroa jacobsoni. Journal of Apicultural Research, v. 24, p. 115–119, 1985.
- BALL, B. V.; ALLEN, M. F. The prevalence of pathogens in honey bee (Apis mellifera) colonies infested with the parasitic mite Varroa jacobsoni. Annals of Applied Biology, v. 113, p. 237–244, 1998. doi: 10.1111/j.1744-7348.1988.tb03300.x
- BALL, B. V.; BAILEY, L. Viruses. In: Morse, R.A.; Flottum, K. (eds.), Honey Bee Pests, Predators, and Diseases. Medina: A.I. Root Company, 1997.
- BÉKÉSI, L., V. BALL, B., DOBOS-KOVÁCS, M., BAKONYI, T., & RUSVAI, M. Occurrence of acute paralysis virus of the honey bee (Apis mellifera) in a hungarian apiary infested with the parasitic mite Varroa jacobsoni. Acta Veterinaria Hungarica, v. 47, n. 3, p. 319–324, 1999. doi:10.1556/avet.47.1999.3.5
- BARBIÉRI, C.; FRANCOY, T. M. Modelo teórico para análise interdisciplinar de atividades humanas: A meliponicultura como atividade promotora da sustentabilidade. Ambiente & Sociedade, São Paulo, v. 23, p. 1-19, 2020.
- BOREHAM, M. M.; ROUBIK, D. W. Population change and control of Africanized honeybees in the Panama canal area. Bulletin of the Entomological Society of America, v. 33, p. 34-39, 1987.
- BRASIL. Ministério da Agricultura, Pecuária e Abastecimento. Programa Nacional de Sanidade Apícola (PNSAp). Brasília: MAPA/ACS, 2008.
- BRASIL. Decreto n° 9.013, de 29 de março de 2017. Regulamenta a Lei nº 1.283, de 18 de dezembro de 1950, e a Lei nº 7.889, de 23 de novembro de 1989, que dispõem sobre a inspeção industrial e sanitária de produtos de origem animal. Diário Oficial da União: seção 1, Brasília, DF, ano 129, 30 mar. 2017.
- BRASIL. Lei nº 13.680, de 14 de junho de 2018. Altera a Lei nº 1.283, de 18 de dezembro de 1950, para dispor sobre o processo de fiscalização de produtos alimentícios de origem animal produzidos de forma artesanal. Poder Executivo, Brasília, Distrito Federal,14 de junho de 2018. Disponível em: http://www.planalto.gov.br/ccivil_03/_ato2015-2018/2018/lei/L13680.htm . Acesso em: 23 de set. 2020.
- BRAND, H. Enxameação das abelhas nativas. Mensagem Doce. Apacame, mar. 2018. Disponível em: http://apacame.org.br/site/revista/mensagem-doce-n-145-marco-de-2018/artigo-3/. Acesso em: 8 set. 2020.
- BÉKÉSI, L., V. BALL, B., DOBOS-KOVÁCS, M., BAKONYI, T., & RUSVAI, M. Occurrence of acute paralysis virus of the honey bee (Apis mellifera) in a hungarian apiary infested with the parasitic mite Varroa jacobsoni. Acta Veterinaria Hungarica, v. 47, n. 3, p. 319–324, 1999. doi:10.1556/avet.47.1999.3.5
- BOTÍAS, C.; MARTÍN-HERNÁNDEZ, R.; DIAS, J.; GARCÍA-PALENCIA, P.; MATABUENA, M.; JUARRANZ, A.; BARRIOS, L.; MEANA, A.; NANETTI, A.; HIGES, M. The effect of induced queen replacement on Nosema spp. infection in honey bee (Apis mellifera iberiensis) colonies. Environmental Microbiology, 14(4), 845-859, 2012. doi:10.1111/j.1462-2920.2011.02647.x
- BROUWERS, E. V. M.; EBERT, R.; BEETSMA, J. Behavioural and physiological aspects of nurse bees in relation to the composition of larval food during caste differentiation in the honeybee. Journal of Apicultural Research, v. 26, n. 1, p. 11-23, 1987.
- BOWEN-WALKER, P. L.; MARTIN, S. J.; GUNN, A. The transmission of Deformed Wing Virus between honeybees (Apis mellifera L.) by the ectoparasitic mite Varroa jacobsoni Oud. Journal of Invertebrate Pathology, v. 73, p. 101–106, 1999. doi: 10.1006/jipa.1998.4807
- BUTLER, C. G. The choice of drinking water by the honeybee. Journal of Experimental Biology, v. 17, n. 3, p. 253-261, 1940.
- BRASIL. Ministério da Agricultura Pecuária e Abastecimento. Nota técnica Nº 9/2019/DSE/CAT/CGSA/DSAIP_2/DAS/MAPA. Infestação de colmeias pelo Aethina túmida, Brasília, 2019.
- BARKER, R.J. Poisoning by plants. London: Cornell University Press, 1990
- BELZUNCES, L.P.; TCHAMITCHAN, S.; BRUNET, J.L. Neural effects of insecticides in the honey bee. Apidologie, v. 43, p. 348-370, 2010. doi: 10.1007/s13592-012-0134-0
- BLACQUIERE, T.; SMAGGHE, G.; VAN GESTEL, C. A.; MOMMAERTS, V. Neonicotinoids in bees: a review on concentrations, side-effects and risk assessment. Ecotoxicology, v. 21, n. 4, p. 973-992, 2012.
- BOMBARDI, Larissa Mies. Geografia do uso de agrotóxicos no Brasil e conexões com a União Europeia. FFLCH-USP, 2017.
- BRITTAIN, C.; POTTS, S. G. The potential impacts of insecticides on the life-history traits of bees and the consequences for pollination. Basic and Applied Ecology, v. 12, n. 4, p. 321-331, 2011.
- CHEN, D.; GUO, R.; XIONG, C.; ZHENG, Y.; HOU, C.; FU, Z. Morphological and molecular identification of chalkbrood disease pathogen Ascosphaera apis in Apis cerana cerana. Journal of Apicultural Research, v. 57, p. 4, 2018. doi: 10.1080/00218839.2018.147594
- CHEVIN, A.; SCHURR, F.; BLANCHARD, P.; THIÉRY, R.; RIBIÈRI, M. Experimental infection of the honeybee (Apis mellifera L.) with the chronic bee paralysis virus (CBPV): infectivity of naked CBPV RNAs. Virus Research, v. 167, p. 173-178, 2012. doi: 10.1016/j.virusres.2012.04.012
- CAP- Departamento Técnico. Manual de Sanidade Apícola, Sintomas – Profilaxia – Controlo, FNAP – Federação Nacional dos Apicultores de Portugal, 2007. Disponível em < http://fnap.pt/web/wp-content/uploads/documento_cnt_projectos_127.pdf > Acesso em: 20/08/2020.
- CELLA, I; CUNHA, R. D.; SEZERINO, A. A.; SATTLER, A.; COAN, L. F. B.; SCASSO, R. E. Manejos para o controle de doenças, pragas e predadores das abelhas no sul do Brasil. Florianopolis: Epagri, 2020. 72 p. (Boletim Didatico, 151).
- CAMARGO, J.M.F. Historical Biogeography of the Meliponini (Hymenoptera, Apidae, Apinae) of the Neotropical Region. In: VIT, P.; PEDRO, S.R.M. ROUBIK, D.W. (Eds.), Pot Honey: A legacy of stingless bees. New York: Springer, 2013. p. 19-34
- DOI: 10.1007/978-1-4614-4960-7_2
- CAMARGO, J. M. F.; PEDRO, S. R. M. Meliponini Lepeletier, 1836. In: MOURE, J. S.; URBAN, D.; MELO, G. A. R. (Orgs). Catálogo das Abelhas (Hymenoptera, Apoidea) da Região Neotropical, 2013 - versão online. Disponível em: http://www.moure.cria.org.br/catalogue. Acesso em: 23 setembro 2020.
- CAMARGO, R. C. R. (Ed.). Produção de mel. Teresina: Embrapa Meio-Norte, 2002. 133 p.
- CONAMA - CONSELHO NACIONAL DO MEIO AMBIENTE. Resolução nº 496, de 19 de agosto de 2020. Disciplina o uso e o manejo sustentáveis das abelhas-nativas-sem-ferrão em meliponicultura. Diário Oficial da União, 20 de agosto de 2020. Disponível em: https://www.in.gov.br/en/web/dou/-/resolucao-n-496-de-19-de-agosto-de-2020-273217120. Acesso em: 23 set. 2020.
- CARRECK, N. L., BALL, B. V., & MARTIN, S. J. The epidemiology of cloudy wing virus infections in honey bee colonies in the UK. Journal of Apicultural Research, v. 49, n. 1, p. 66–71, 2010. doi:10.3896/ibra.1.49.1.09
- CARVALHO, A. C. P.; MESSAGE, D. A scientific note on the toxic pollen of Stryphnodendron polyphyllum (Fabaceae, Mimosoideae) wich causes sacbrood-like symptoms. Apidologie, v. 35, p. 89-90, 2004.
- CLARK, T.B. Another virus in the honey bees. American Bee Journal, v. 117, p. 340–341, 1977.
- Centro de Gestão e Estudos Estratégicos (CGEE). Importância dos polinizadores na produção de alimentos e na segurança alimentar global, DF: 2017. 124 p.
- CORTOPASSI-LAURINO, M.; NOGUEIRA NETO, P. Abelhas sem ferrão do Brasil. Editora da Universidade de São Paulo: São Paulo, 2016. 124 p.
- COSTA, R. O.; BEZERRA, A. H. A.; FERREIRA, A. C.; AFONSO, J. P. S. D.; ALVES, A. S.; JUNIOR, L. S. P.; GOMES, A.T. Problemas na cadeia produtiva de mel do Estado da Paraíba. Revista Brasileira de Gestão Ambiental, Pombal, v. 11, n. 2, p. 05-09, 2017.
- CRANE, E. Bees and beekeeping: science, practice and world resources. Oxford: Heinemann Newnes, 1990. 640 p.
- CALLIGARIS, I. B. Toxicidade do néctar e do pólen de Spathodea campanulata (Bignoneaceae) sobre operárias de Apis mellifera (Hymenoptera: Apidae) e Scaptotrigona postica (Hymenoptera: Apidae). 2001. Dissertação, Universidade Estadual Paulista Júlio de Mesquita Filho, São Paulo, 2001.
- CARVALHO, A. C. P. Pólen de Stryphnodendron polyphillum como agente causador da cria ensacada brasileira em Apis mellifera L. 1998. 60 f. Dissertação (Mestrado em Entomologia), Universidade Federal de Viçosa, Viçosa, 1998.
- CARVALHO, A. C. P.; MESSAGE, D. A scientific note on the toxic pollen of Stryphnodendron polyphyllum (Fabaceae, Mimosoidae) wich causes sacbrood-like symptoms. Apidologie, v.35, p.89-90, 2004.
- CHAMBÓ, E.D.; GARCIA, R.C.; OLIVEIRA, N.T.E.; DUARTE-JÚNIOR J.B. Aplicação de inseticida e seus impactos sobre a visitação de abelhas (Apis mellifera L.) no girassol (Helianthus annuus L.). Revista Brasileira de Agroecologia. v. 5, n. 1, p. 37-42, 2010.
- CINTRA P.; MALASPINA, O.; PETACCI, F.; FERNANDES, J.B.; BUENO, O.C.; VIEIRA, P.C.; SILVA, M.F.G.F. Toxicity of Dimorphandra mollis to workers of Apis mellifera. Journal of Brazilian Chemical Society, v.13, n.1, p.115-118, 2002.
- CINTRA, P.; MALASPINA, O.; BUENO O.C. Toxicity of Barbatimão to Apis mellifera and Scaptotrigona postica, under laboratory conditions. Journal of Apicultural Research, v.42, n.1/2, p.9-12, 2003.
- DA CRUZ LANDIM, C. Abelhas: morfologia e função de sistemas. São Paulo: UNESP, 2009.
- DE MIRANDA, J. R.; CORDONI, G.; BUDGE, G. The acute bee paralysis vírus-Kashimir bee vírus-Israeli acute paralysis virus complex. Journal of Invertebrate Pathology, v. 103, p. S30-S47, 2010. doi: 10.1016/j.jip.2009.06.014
- DE MIRANDA, J. R.; GENERSH, E. Deformed wing vírus. Journal of Invertebrate Pathology, v. 103, p. S48-S61, 2010. doi: 10.1016/j.jip.2009.06.012
- Disponível em: <https://ainfo.cnptia.embrapa.br/digital/bitstream/item/31359/1/comunicado-178.pdf> Acesso em: 12/08/2020.
- DE JONG D. Africanized honey bees in Brazil, forty years of adaptation and success. Bee World, v.77, 2 edição, p.67-70, 1996.
- DE SOUZA, D. A.; GRAMACHO, K. P.; CASTAGNINO, G. L. B. Produtividade de mel e comportamento defensivo como índices de melhoramento genético de abelhas africanizadas (Apis mellifera L.). Revista Brasileira de Saúde e Produção Animal, Salvador, v. 13, n. 2, p. 550-557, 2012.
- DELAPLANE, K. S.; MAYER, D. F. Crop pollination by bees. Oxon: CABI Publishing, 2005. 344 p.
- DEL LAMA, M. A.; SOUZA, R. O.; DURAN, X. A. A.; SOARES, A. E. E. Clinal variation and selection on MDH allozymes in honeybees in Chile. Hereditas, v. 140, p. 149-153, 2004.
- DIETZ, A.; HAYDAK, M. H. Caste determination in honeybees. I. The significance of moisture in larval food. Journal of Experimental Zoology, v. 177, n. 3, p. 353-357, 1971.
- DAINAT, B.; KEN, T.; BERTHOUD, H.; NEUMANN, P. The ectoparasite mite Tropilaelaps mercedasae (Acari, Laelapidae) as a vector of honey bee viroses. Insectes Sociaux, v. 56, p. 40-43, 2009. doi: 10.1007/s00040-008-1030-s
- DISCOVERY LIFE. Guide Apoidea Species. 2020. Disponível em: https://www.discoverlife.org/mp/20q?guide=Apoidea_species&frags=HAS. Acesso em: 24 nov. 2020.
- DECOURTYE, A.; ARMENGAUD, C.; RENOU, M.; DEVILLERS, J.; CLUZEAU, S.; GAUTHIER, M.; PHAM-DELÈGUE, M. H. Imidacloprid impairs memory and brain metabolism in the honeybee (Apis mellifera L.). Pesticide Biochemistry and Physiology, v. 78, n. 2, p. 83-92, 2004.
- DE QUEIROZ, A. C. M.; VENTURIERI, G. C.; CONTRERA, FAL. Tulipeira-africana (Spathodea campanulata): mocinha ou vilã para as abelhas? Mensagem Doce, n. 143, 2017.
- DESNEUX, N.; DECOURTYE, A.; DELPUECH, J. The sublethal effects of pesticides on beneficial arthropods. Annual Review of Entomology, v. 52, p. 81-106, 2007.doi: 10.1146/annurev.ento.52.110405.091440.
- DI PRISCO, G.; CAVALIERE, V.; ANNOSCIA, D.; VARRICCHIO, P.; CAPRIO, E.; NAZZI, F.; PENNACCHIO, F. Neonicotinoid clothianidin adversely affects insect immunity and promotes replication of a viral pathogen in honey bees. Proceedings of the National Academy of Sciences, v. 110, n. 46, p. 18466-18471, 2013
- EBELING, J.; KNISPEL, H.; HERTLEIN, G.; FUNFHAUS, A.; GENERSH, E. Biology of Paenibacillus larvae, a deadly pathogen of honey bee larvae. Applied Microbiology and Biotechnology, v. 100, p. 7387-7395, 2016. doi: 10.1007/s00253-016-7716-0
- EUROPEAN FOOD SAFETY AUTHORITY. Conclusion on the peer review of the pesticide risk assessment for bees for the active substance imidacloprid. EFSA Journal, v. 11, n. 1, p. 3068, 2013.
- FAO - FOOD AND AGRICULTURE ORGANIZATION. Pollinators vital to our food supply under threat 2016. Disponível em: http://www.fao.org/news/story/pt/item/384726/icode/. Acesso em: 23 set. 2020.
- FAO - FOOD AND AGRICULTURE ORGANIZATION. Faostat. 2019. Disponível em: http://www.fao.org/faostat/en/#data. Acesso em: 23 set. 2020.
- FERNANDES JÚNIOR, J, V. M.; ARAÚJO SILVA, N. G. Cadeia Produtiva do Mel: um estudo no município de Pau dos Ferros/RN. Revista Eletrônica em Gestão, Educação e Tecnologia Ambiental, Santa Maria, v. 20, n. 1, p. 115-124, 2016.
- FREITAS, B. M.; RIBEIRO, M. D. F.; GUIMARÃES, M. D. O.; PACHECO, W. F.; MILFONT, M. D. O.; NEPOMUCENO, R. C. Atividade externa e coleta de recursos em ninhos naturais por campeiras da abelha canudo Scaptotrigona bipunctata (Hymenoptera, Apidae, Meliponini). In: REUNIÃO ANUAL DA SOCIEDADE BRASILEIRA DE ZOOTECNIA, 44., 2007, Jaboticabal. Anais [...] Jaboticabal: Unesp: SBZ, 2007.
- FLORES, J. M.; RUIZ, J. A.; RUZ, J. M.; PUERTA, F.; BUSTOS, M.; PADILLA, F.; CAMPANO, F. Effect of temperature and humidity of sealed brood on chalkbrood development under controlled conditions. Apidologie, v. 27, p. 185–192, 1996. doi: 10.1051/apido:19960401
- FLORES, J. M.; SPIVAK, M.; GUTIÉRREZ, I. Spores of Ascosphaera apis contained in wax foundation can infect honeybee brood. Veterinary Biology, v. 108, p. 141-144, 2005. doi: 10.1016/j.vetmic.2005.03.005
- FNAP – Federação Nacional dos Apicultores de Portugal, 2007. Disponível em < http://fnap.pt/web/wp-content/uploads/documento_cnt_projectos_127.pdf > Acesso em: 20/08/2020.
- FRANCIS, R. M.; NIELSEN, S. L.; KRYGER, P. Varroa-virus interaction in collapsing honey bee colonies. PLoS ONE, v. 8, p. e57540, 2013. doi: 10.1371/journal.pone.0057540
- FRIES, I. Nosema apis - a parasite in the honey bee colony. Bee World, v. 74, n 1, p. 5–19, 1993. doi: 10.1080/0005772X.1993.11099149
- FRIES, I. Nosema ceranae in European honey bees (Apis mellifera). Journal of Invertebrate Pathology, v. 103, p. s73-s79, 2010. doi: 10.1016/j.jip.2009.06.017
- FRIES, I.; CHAUZAT, M-P.; CHEN, Y-P.; DOUBLET, V.; GENERSH, E.; GISDER, S.; HIGES, M.; MCMAHON, D. P.; MARTÍN-HERNANDÉZ, R.; NATSOPOULOU, M.; PAXTON, R. J.; TANNER, G.; WEBSTER, T. C.; WILLIAMS, G. R. Standard methods for Nosema research. Journal of Apicultural Research, v. 52, n. 1, 2013. doi: 10.3896/IBRA.1.52.1.14
- FRIES, I.; SLEMENDA, S. B.; DA SILVA, A.; PIENIAZEK, N. J. African honey bees (Apis mellifera scutellata) and nosema (Nosema apis) infections. Journal of Apicultural Research, v. 42, p. 13–15, 2003. doi: 10.3896/IBRA.1.52.1.14
- FUJIYUKI, T.; TAKEUCHI, H.; ONO, M.; OHKA, S.; SASAKI, T.; NOMOTO, A.; KUBO, T. Kakugo virus from brains of aggressive worker honeybees. Advances in Virus Research, v. 65, p. 1-27, 2005. doi: 10.1016/s0065-3527(05)65001-4
- FUJIYUKI, T.; TAKEUCHI, H.; ONO, M.; OHKA, S.; SASAKI, T.; NOMOTO, A.; KUBO, T. Novel insect picorna-like virus identified in the brains of aggressive worker honeybees. Journal of Virology, v. 78, n. 3, p. 1093-1100, 2004. doi: 10.1128/JVI.78.3.1093-1100.2004
- FRANSOZO, A; FRANSOZO, N. M. L. Zoologia dos invertebrados. São Paulo: GEN Roca, 2017. 716p
- FREITAS, P. V. D. X.; RIBEIRO, F. M.; ALMEIDA, E. M.; ZANATA, R. A.; ALVES, J. J. L.; OLIVEIRA, V. F.; FAQUINELLO, P. Declínio populacional das abelhas polinizadoras: Revisão. PUBVET, v. 11, n. 1, p. 1-10, 2017.
- FRANCOY, Tiago Maurício. Variabilidade genético – morfológica em populações Neotropicais de Apis mellifera. 2007. Tese (Doutorado em Ciências) – Faculdade de Medicina, Ribeirão Preto, São Paulo, 2007.
- FAIRBROTHER, A.; PURDY, J.; ANDERSON, T.; FELL, R. Risks of neonicotinoid insecticides to honeybees. Environmental Toxicology and Chemistry, v. 33, n. 4, p. 719-731, 2014.
- FATE, ENVIRONMENTAL; EFFECTS DIVISION (EFED); PEST MANAGEMENT REGULATORY AGENCY (PMRA); CALIFORNIA DEPARTMENT OF PESTICIDES REGULATION (CDPR). White Paper in Support of the Proposed Risk. Assessment Process for Bees, v. 275, 2012.
- FAUSER‐MISSLIN, A.; SADD, B. M.; NEUMANN, P.; SANDROCK, C. Influence of combined pesticide and parasite exposure on bumblebee colony traits in the laboratory. Journal of Applied Ecology, v. 51, n. 2, p. 450-459, 2014.
- FREITAS, B. M.; IMPERATRIZ-FONSECA, V. L.; MEDINA, L. M.; KLEINERT, A. M. P.; GALETTO, L.; NATES-PARRA, G.; QUEZADA-EUÁN, J. J. G. Diversity, threats and conservation of native bees in the Neotropics. Apidologie, v. 40, p. 332-346, 2009.
- FREITAS, B.M.; PINHEIRO, J.N. Efeitos sub-letais dos pesticidas agrícolas e seus impactos no manejo de polinizadores dos agroecossistemas brasileiros. Oecologia Brasiliensis (Online), v. 14, p. 282 - 298, 2010.
- GENERSH, E. American foulbrood in honeybees and its causative agent, Paenibacillus larvae. Journal of Invertebrate Pathology, v. 103, n. 1, p. 10-19, 2010. doi: 10.1016/j.jip.2009.06.015
- GILLARD, M.; CHARRIERE, J. D.; BELLOY, L. Distribution of Paenibacillus larvae espores inside honey bee colonies and its relevance for diagnosis. Journal of Invertebrate Pathology, v. 99, p. 92-95, 2008. doi: 10.1016/j.jip.2008.05.010
- GOVAN, V. A.; LEAT, N.; ALLSOP, M.; DAVISON, S. Analysis of the complete genome sequence of acute bee paralysis virus shows that it belongs to the novel group of insect-infecting RNA viruses. Virology, v. 277, p. 457–463, 2000.
- GIANNINI, T. C., CORDEIRO, G. D., FREITAS, B. M., SARAIVA, A. M., & IMPERATRIZ-FONSECA, V. L. (2015). The dependence of crops for pollinators and the economic value of pollination in Brazil. Journal of economic entomology, 108(3), 849-857.
- GONÇALVES, L. S. A. influência do comportamento das abelhas africanizadas na produção, capacidade de defesa e resistência à doenças. In: I ENCONTRO SOBRE ABELHAS DE RIBEIRÃO PRETO, 1994, São Paulo. Anais [...]. São Paulo: USP, 1994. p. 69-79.
- GONÇALVES, L. S. Impactos biológicos causados pela africanização das abelhas Apis mellifera e pela competição das abelhas africanas Apis mellifera scutellata com seu parasita obrigatório, o pseudoclone de Apis mellifera capensis. In: V ENCONTRO SOBRE ABELHAS DE RIBEIRÃO PRETO, 2001, São Paulo. Anais [...]. São Paulo: USP, 2001. p. 72-77.
- GONÇALVES, L. S. Desenvolvimento e expansão da apicultura no Brasil com abelhas africanizadas. Revista SEBRAE, v. 3, p. 14-16, 2006.
- GONCALVES, L. S.; DE JONG, D.; GRAMACHO, K. P. A expansão da apicultura e da tecnologia apícola no Nordeste Brasileiro, com especial destaque para o Rio Grande do Norte. Mensagem doce, v. 3, p. 7-15, 2010.
- GONÇALVES, L. S. Como as abelhas se comunicam? Mensagem Doce. Apacame, 2003. Disponível em: https://www.apacame.org.br/mensagemdoce/71/artigo2.htm. Acesso em: 10 set. 2020.
- GUERRA-JÚNIOR, J. C.; GONÇALVES, L. S.; DE JONG, D. Africanized honey bees (Apis mellifera L.) are more efficient at removing worker brood artificially infested with the parasitic mite Varroa jacobsoni Oudemans than are Italian bees or Italian/Africanized hybrids. Genetics and Molecular Biology, v, 23, n. 1, p. 89-92, 2000.7
- GALLO, D.; NAKANO, O.; SILVEIRA NETO, S.; CARVALHO, R. P. L.; BAPTISTA, G. C. de; BERTI FILHO, E.; PARRA, J. R. P.; ZUCCHI, R. A.; ALVES, S. B.; VENDRAMIM, J. D.; MARCHINI, L. C.; LOPES, J. R. S.; OMOTO, C. Entomologia Agrícola. Piracicaba: Fealq, 2002.
- GODFRAY, H. C. J.; BLACQUIERE, T.; FIELD, L. M.; HAILS, R. S.; PETROKOFSKY, G.; POTTS, S. G.; MCLEAN, A. R. A restatement of the natural science evidence base concerning neonicotinoid insecticides and insect pollinators. Proceedings of the Royal Society B: Biological Sciences, v. 281, n. 1786, p. 20140558, 2014.
- GOULSON, D.; NICHOLLS, E.; BOTÍAS, C.; ROTHERAY, E. L. Bee declines driven by combined stress from parasites, pesticides, and lack of flowers. Science, v. 347, n. 6229, p. 1435, 2015.
- GUNASEKARA, A. S.; TRUONG, T.; GOH, K. S.; SPURLOCK, F.; TJEERDEMA, R. S. Environmental fate and toxicology of fipronil. Journal of Pesticide Science, p. 0706180001-0706180001, 2007.
- HARTFELDER, K.; ENGELS, W. The composition of larval food in stingless bees: evaluating nutritional balance by chemosystematic methods. Insectes Sociaux, v. 36, n. 1, p. 1-14, 1989.
- HARTFELDER, K.; MARKET, G. R.; JUDICE, C. C.; PEREIRA, G. A.; SANTANA, W. C.; DALLACQUA, R.; BITONDI, M. M. Physiological and genetic mechanisms underlying caste development, reproduction and division of labor in stingless bees. Apidologie, v. 37, n. 2, p. 144-163, 2006.
- HAYDAK, M. H. Honeybee nutrition. Annual Review of Entomology, v. 15, n. 1, p. 143-156, 1970.
- HARTMANN, U., FORSGREN, E., CHARRIÈRE, J. D., NEUMANN, P., & GAUTHIER, L. Dynamics of Apis mellifera filamentous virus (amfv) infections in honey bees and relationships with other parasites. Viruses, v. 7, n. 5, p. 2654–2667, 2015. doi:10.3390/v7052654
- HASEMANN, L. How long can spores of American foulbrood live? American Bee Journal, v. 101, p. 298-299, 1961.
- HEATH, L. A. F. Development of chalkbrood in a honeybee colony: a review. Bee World, v. 63, p. 119-130, 1982. doi: 10.1080/0005772X.1982.11097877
- HIGES, M.; MARTÍN, R.; MEANA, A. Nosema ceranae, a new microsporidian parasite in honeybees in Europe. Journal of Invertebrate Pathology, v. 92, p. 81–83, 2006. doi: 10.1016/j.jip.2006.02.005
- HIGES, M.; MARTIN-HERNANDEZ, R.; BOTIAS, C.; BAILON, E. G.; GONZALES-PORTO, A. V.; BARRIOS, L.; DEL NOZAL, M. J.; BERNAL, J. L.; JIMENEZ, J. J.; PALENCIA, P. G.; MEANA, A. How natural infection by Nosema ceranae causes honey bee colony collapse. Environmental Microbiology, v. 10, v. 10, p. 2659–2669, 2008. doi: 10.1111/j.1462-2920.2008.01687.x
- ICTV. International Committee on Taxonomy of Viruses. 2020. Disponível em: < https://talk.ictvonline.org/taxonomy/p/taxonomy-history?taxnode_id=201901944 > Acesso em: 28/12/2020.
- HOLDER, P. J.; JONES, A.; TYLER, C. R.; CRESSWELL, J. E. Fipronil pesticide as a suspect in historical mass mortalities of honey bees. Proceedings of the National Academy of Sciences, v. 115, 2018.
- JIN, L.; MEHMOOD, S.; ZHANG, G.; SONG, Y.; SU, S.; HUANG, W.F.; HUANG, H.; ZHANG, Y.; GENG, H.; HUANG, W-F. Visualizing sacbrood virus of honey bees via transformation and coupling with enhanced green fluorescent protein. Viruses, v. 12, n. 2, p. 224, 2020. doi:10.3390/v12020224.
- KHONGPHINITBUNJONG, K.; DE GUZMÁN, L. L.; TARVER, M.R.; RINDERER, T. E.; CHANTAWANNAKUL, P. Interactions of Tropilaelaps mercedesae, honey bee viruses and immune response in Apis mellifera. Journal of Apicultural Research, v. 54, n. 1, p. 40-47, 2015. doi: 10.1080/00218839.2015.1041311
- IMPERATRIZ-FONSECA, V. L.; CONTRERA, F. A. L.; KLEINERT, A. M. P. A meliponicultura e a iniciativa brasileira dos polinizadores. In: XV CONGRESSO BRASILEIRO DE APICULTURA, 2004, Natal. Anais […]. Natal, 2004. P. 1-7.
- Instituto Brasileiro De Geografia e Estatística – IBGE. Pesquisa pecuária municipal. IBGE (2017). Disponível em: https://sidra.ibge.gov.br/Itabela/6622#resultado. Acesso em: 02 set. 2020
- Instituto Brasileiro De Geografia e Estatística – IBGE. Pesquisa pecuária municipal. IBGE (2018). Disponível em: < https://sidra.ibge.gov.br/tabela/74#resultado>. Acesso em: 02 set. 2020.
- Integrated Taxonomic Information System (ITIS), 2018. Apoidea. Disponível em: https://www.itis.gov/servlet/SingleRpt/SingleRpt?search_topic=TSN&search_value=1543 44#null. Acesso em: 23 set. de 2010.
- KERR, W. E. The history of introduction of African bees to Brazil. South African Bee Journal, v. 39, p. 3-5, 1967.
- KERR, W. E. História parcial da ciência apícola no Brasil. In: V CONGRESSO BRASILEIRO DE APICULTURA, 1980, Viçosa. Anais [...]. Minas Gerais: Confederação Brasileira de Apicultura, 1980.
- KERR, W. E.; DEL RIO, S. L.; BARRIONUEVO, M. D. The southern limits of the distribution of the Africanized honey bees in South America. American Bee Journal, v. 122, p. 196 -198, 1982.
- KERR, W. E. Abejas africanas, su introduccion y expansion en el continente Americano. Subespécies e ecotipos africanos. Industria Apícola, n. 13, p. 12-21, 1992.
- KOSER, J. R.; BARBIÉRI, C.; FRANCOY, T. M. Legislação sobre meliponicultura no Brasil: demanda social e ambiental. Sustainability in Debate, Brasília, v. 11, n. 1, p. 179-194, 2020.
- KRUPKE, C. H.; HUNT, G. J.; EITZER, B. D.; ANDINO, G.; GIVEN, K. Multiple routes of pesticide exposure for honeybees living near agricultural fields. Plos One, v. 7, 2012.
- LENGLER, L.; RATHMANN, R. Assimetria de relacionamentos na cadeia apícola do Rio Grande do Sul. Revista FAE, Curitiba, v. 9, n. 2, p. 51-62, 2006.
- LEAT, N.; BALL, B.; GOVAN, V.; DAVISON, S. Analysis of the complete genome sequence of black queen cell virus, a picorna-like virus of honey bees. Journal of General Virology, v. 81, p. 2111–2119, 2000. doi: 10.1099/0022-1317-81-8-2111
- LINDSTROM, A.; KORPELA, S.; FRIES, I. The distribution of Paenibacillus larva espores in adult bees and honey and larval mortality, following the addition of American foulbrood disease brood or spore-contaminated honey in honey bee (Apis mellifera) colonies. Journal of Invertebrate Pathology, v. 99, n. 1, p. 82-86, 2008. doi: 10.1016/j.jip.2008.06.010
- LUNDIN, O.; RUNDLÖF, M.; SMITH, H. G.; FRIES, I.; BOMMARCO, R. Neonicotinoid insecticides and their impacts on bees: a systematic review of research approaches and identification of knowledge gaps. PloS One, v. 10, 2015.
- MAORI, E.; TANNE, E.; SELA, I. Reciprocal sequence exchange between non‐retro viruses and hosts leading to the appearance of new host phenotypes. Virology, p. 362, 342–349, 2007. doi: 10.1016/j.virol.2006.11.038
- MARTIN, S. J.; ALLSOPP, M. H. Honey bee diseases and parasites. In: Starr, C.K. (ed.). Encyclopedia of Social Insects. Manchester: Springer, 2020. doi: 10.1007/978-3-319-90306-4_59-1
- MEDINA, L. M.; MARTIN, S. J., A comparative study of Varroa jacobsoni reproduction in worker cells of honey bees (Apis mellifera) in England and Africanized bees in Yucatan, Mexico. Experimental and Applied Acarology, v.23, p.659-667, 1999.
- MESSAGE, D.; GUIDUGLI-LAZZARINIK. R.; FREITAS, N. H. A.; SIMÕESZ. L. P.; DE JONG, D.; SILVAI. C.; TEIXEIRA, E. W. Colapso de colônias de abelhas africanizadas Apis mellifera L. (Hymenoptera, Apidae) no Brasil. Revista de Educação Continuada em Medicina Veterinária e Zootecnia do CRMV-SP, v. 9, n. 3, p. 59-59, 2011.
- MORGENTHALER, O. Das jahreszeitliche auftreten der bienenseuchen. Beih. Schweiz. Bienenztg, v. 1, p. 285-336, 1944.
- MORISON, G. D. Acarine disease and the muscles of honey bee. Nature, v. 120, p. 259-260, 1927.
- MUELLER, C. M.; JACK, C. J.; MORTENSEN, A. N.; ELLIS, J. Identification and treatment of European foulbrood in honey bee colonies. Entomology and Nematology Department, UF/IFAS, ENY174, 2019. doi: 10.32473/edis-in1272-2019
- MARTINEZ, O. A.; SOARES, A. E. E. Melhoramento genético na apicultura comercial para produção da própolis. Revista Brasileira de Saúde e Produção Animal, v. 13, n. 4, p. 982-990, 2012.
- MOURE CRIA. Catálogo de Abelhas Moure, 2020. Disponível em: <http://moure.cria.org.br/>. Acessado em: 9 de set. De 2020.
- MAIA-SILVA, C.; HRNCIR, M.; DA SILVA, C. I.; IMPERATRIZ-FONSECA, V. L. Survival strategies of stingless bees (Melipona subnitida) in an unpredictable environment, the Brazilian tropical dry forest. Apidologie, v. 46, n. 5, p. 631-643, 2015.
- MENEZES, C.; VOLLET-NETO, A.; IMPERATRIZ-FONSECA, V. L. An advance in the in vitro rearing of stingless bee queens. Apidologie, v. 44, n. 5, p. 491-500, 2013.
- MICHENER, C. D. Comparative social behavior of bees. Annual review of entomology, v. 14, n. 1, p. 299-342, 1969.
- MICHENER, C. D. The social behavior of the bees: a comparative study. Cambridge: Harvard University Press, 1974.
- MICHENER, C. D. Comparative social behavior of bees. Annual review of entomology, v. 14, n. 1, p. 299-342, 1969.
- MICHENER, C. D. The meliponini. In: VIT, P.; PEDRO, S. R. M.; ROUBIK, D. Pot-honey. New York: Springer, 2013. cap. 1, p. 3-17.
- MOURE, J. S.; URBAN, D.; MELO, G. A. R. Catalogue of bees (Hymenoptera, Apoidea) in the Neotropical region. Curitiba: Sociedade Brasileira de Entomologia, 2007. 1058 p.
- MALASPINA, O.; SOUZA, T. F.; ZACARIN, E. C. M. S.; CRUZ, A. S.; JESUS, D. Efeitos provocados por agrotóxicos em abelhas no Brasil. In: ANAIS DO ENCONTRO SOBRE ABELHAS, 8., Ribeirão Preto, 2008, Anais [...]. São Paulo, 2008, p. 41-48.
- MALASPINA, O. E SILVA-ZACARIN, E.C.M. Cell markers for ecotoxicological studies in target organs of bees. Brazilian Journal of Morphological Sciences, v. 23, p. 303-309, 2006.
- MAPA - MINISTÉRIO DA AGRICULTURA, PECUÁRIA E ABASTECIMENTO. Sistemas de Agrotóxicos Fitossanitários, 2019. Disponível em: <http://extranet.agricultura.gov.br/agrofit_cons/principal_agrofit_cons>.
- Acesso em: 20 de ago. de 2020.
- MELATHOPOULOS, A.P.; WINSTON, M.L.; WHITTINGTON, R.; HIGO, H. & LEDOUX, M. Field evaluation of neem and canola oil for the selective control of the honey bee mite parasites Varroa jacobsoni and Acarapsis woodi. Journal of Economic Entomology, v. 93, p. 559-567, 2000. doi: 10.1603/0022-0493-93.3.559
- MESSAGE, D., BALL, B. V., SILVA, I. C. A serious brood disease affecting africanized honeybees (Apis mellifera). In: PROCEEDING OF APIMONDIA CONGRESS, 34, Lausane, 1995, Proceedings [...]. Lausane, 1995, p. 203
- MESSAGE, D. Management and disease problems of africanized bees in Brazil. Londres: The Central Association Of Bee-Keepers, 1997.
- NASCIMENTO, C. B.; MELLO, R. P.; SANTOS, M. W.; NASCIMENTO, R. V.; SOUZA, D. J. Ocorrência de acariose em Apis mellifera L. no Brasil. Pesquisa Agropecuária Brasileira, v. 6, p. 57–60, 1971.
- NIE, H.; WANG, X.; XU, S.; GAO, Y.; LIN, Y.; ZHU, Y.; YANG, D.; LI, Z.; SU, S. Changes in the gene expression of chalkbrood resistance in Apis mellifera larvae infected by Ascophaera apis. Apidologie, v. 51, p. 35-47, 2020. doi: 10.1007/s13592-019-00702-y
- NASCIMENTO, H. M.; DELGADO, B.; BARBARIC, I. F. Avaliação da aplicação de agentes sanitizantes como controladores do crescimento microbiano na indústria alimentícia. Revista Ceciliana, v. 2, n. 1, p. 11-13, 2010.
- NOGUEIRA-COUTO, R. H.; COUTO, L. A. (2006). Apicultura: manejo e produtos, 3e ed., FUNEP, Jaboticabal.
- OIE. Terrestrial Animal Health Code. 2019. Disponível em: < https://www.oie.int/standard-setting/terrestrial-code/access-online/ > Acesso em: 17/08/2020.
- NOGUEIRA-NETO, P. A Criação de abelhas indígenas sem ferrão. São Paulo: Chácaras e Quintais, 1953. 280 p.
- NOGUEIRA-NETO, P. Vida e criação de abelhas indígenas sem ferrão. São Paulo: Editora Nogueirapis, 1997. 446 p.
- NAGGAR, Y.; CODLING, G.; VOGT, A.; NAIEM, E.; MONA, M.; SEIF, A.; GIESY, J. P. Organophosphorus insecticides in honey, pollen and bees (Apis mellifera L.) and their potential hazard to bee colonies in Egypt. Ecotoxicology and Environmental Safety, v. 114, p. 1-8, 2015.
- NOCELLI, R. C. F.; ROAT, T. C.; ZACARIN, E. C. M. S.; MALASPINA, O. Riscos de pesticidas sobre as abelhas. IN: Semana dos Polinizadores, 2012, Petrolina. Anais [...]. Petrolina: Embrapa Semi-Árido, 2012.
- NOGUEIRA-NETO, P. Vida e criação das abelhas indígenas sem ferrão. São Paulo: Nogueirapis, 1997.
- OIE (Office International des Epizooties – World Organisation for Animal Health, 2019.
- OIE (Office International des Epizooties – World Organisation for Animal Health) – Terrestrial Manual 2018.
- OIE (Office International des Epizooties) - Nosemosis of honey bees, 2008. Disponível em: http://www.oie.int/eng/ normes/mmanual/2008/pdf/2.02.04_NOSEMOSIS.pdf
- OIE. Terrestrial Animal Health Code. 2019. Disponível em: < https://www.oie.int/standard-setting/terrestrial-code/access-online/ > Acesso em: 17/08/2020.
- OLIVEIRA M. L.; CUNHA J. A. Abelhas africanizadas Apis mellifera scutellata Lepeletier, 1836 (Hymenoptera: Apidae: Apinae) exploram recursos na floresta amazonica?. Acta Amazonica, v. 35, p. 389 - 394, 2005.
- OLIVEIRA, R. C.; MENEZES, C.; SOARES, A. E. E.; FONSECA, V. L. I. Ninhos-armadilha para abelhas sem ferrão (Hymenoptera, Meliponini). Apidologie, v. 44, n. 1, p. 29-37, 2012.
- PARANÁ. Lei N° 19152 de 02 de out. de 2017. Dispõe sobre a criação, o manejo, o comércio e o transporte de abelhas sociais nativas (meliponíneos). Diário Oficial do Estado, Curitiba, PR, 02 de outubro de 2017.
- PARPINELLI, R. S. Qualidade microbiológica e caracterização físico-química de amostras de mel de abelhas sem ferrão de seis regiões do estado do Paraná. 2016. (Tese Doutorado em Zootecnia) Universidade Estadual de Maringá, Maringá, 2016.
- PEREIRA, D. S.; MENEZES, P. R.; BELCHIOR, V.; FILHO DE SOUSA, A. H.; MARACAJÁ, P. B. Abelhas indígenas criadas no Rio Grande do Norte. Acta Veterinaria Brasilica, v. 5, n. 1, p. 81-91, 2011.
- PEREIRA, F. D. M.; SOUZA, B. D. A.; LOPES, M. D. R.; VIEIRA NETO, J. M. Manejo de colônias de abelhas sem ferrão. Teresina: Embrapa Meio-Norte-Documentos (INFOTECA-E), 2012. 31 p.
- PEREIRA, D. S.; HOLANDA-NETO, J. P.; SOUSA, L. C. F. S.; COELHO, D. C.; SILVEIRA, D. C.; HERNANDEZ, M. L. Mitigação do comportamento de abandono de abelhas Apis mellifera L. em apiários no Semiárido Brasileiro. ACTA Apicola Brasilica, v. 2, n. 2, p. 01-10, 2014.
- PEIXOTO, C. M.; CORREIA-OLIVEIRA, M. E.; CARVALHO, C. A. L. Current status of Acarapis woodi mite infestation in Africanized honey bee Apis mellifera in Brazil. Florida Entomologist, v. 102, n. 4, p. 775-777, 2020. doi: 10.1653/024.102.0416
- PATEL, N.G.; HAYDAK, M.H.; GOCHNAUER, T.A. Electrophoretic components of the proteins in honeybee larval food. Nature, v. 186, p. 633-634, 1960. doi: 10.1038/186633a0
- PENA, M. F.; AMARAL, E. H.; SPERLING, E. V.; CRUZ, I. Método para determinação de resíduos de clorpirifós em alface por cromatografia a líquido de alta eficiência. Pesticides, v. 13, n 1, p. 37-44, 2003.
- PETTIS, J. S.; LICHTENBERG, E. M.; ANDREE, M.; STITZINGER, J.; ROSE, R. Crop pollination exposes honeybees to pesticides which alters their susceptibility to the gut pathogen Nosema ceranae. PloS one, v. 8, n. 7, p. e70182, 2013.
- PORTUGAL-ARAÚJO, V. O perigo da dispersão da Tulipeira do Gabão (Spathodea campanulata Beauv.). Chácaras e Quintaes, v.107, p.562, 1963.
- ROSA, A.; TEIXEIRA, J. S. G.; VOLLET-NETO, A.; QUEIROZ, E. P.; BLOCHTEIN, B.; PIRES, C. S. S.; IMPERATRIZ-FONSECA, V. L. Consumption of the neonicotinoid thiamethoxam during the larval stage affects the survival and development of the stingless bee, Scaptotrigona aff. depilis. Apidologie, v. 47, n. 6, p. 729-738, 2016
- RAMSEY, SD., OCHOA, R., BAUCHAN, G. et al. (2019). Varroa destructor feeds primarily on honey bee fat body tissue and not hemolymph. Proc Natl Acad Sci USA 116:1792–1801. https://doi.org/10.1073/pnas.1818371116.
- RENNIE, J. Isle of Wight disease in hive bees. Acarine disease: the organism associated with the disease, Tarsonemus woodi, n. sp. Earth and Environmental Science Transactions of the Royal Society of Edinburgh, v. 52, p. 768–779, 1921.
- RIBIÈRE, M.; TRIBOULOT, C.; MATHIEU, L.; AURIÈRES, C.; FAUCON, J. P.; PÉPIN, M. Molecular diagnosis of chronic bee paralysis virus infection. Apidologie, v. 33, p. 339–351, 2002. doi: 10.1051/apido:2002020
- ROCHA, H. C.; BAGAGLE, E.; FUNARI, S. R. C. Identificação do fungo Ascophaera apis em colônias de abelhas Apis mellifera L. no Estado de São Paulo-SP. In: XII Congresso Brasileiro de Apicultura, Salvador. Anais. 1998.
- ROSENKRANZ, P., AUMEIER, P., & ZIEGELMANN, B. (2010). Biology and control of Varroa destructor. Journal of Invertebrate Pathology, 103, S96–S119. doi:10.1016/j.jip.2009.07.016
- RANGEL. J.; KELLER, J. J.; TARPY, D. R. The effects of honey bee (Apis mellifera L.) queen reproductive potential on colony growth. Insectes Sociaux, v. 60, p. 65-73, 2013.
- REIS, V. D. A.; PINHEIRO, R. S. Fundamentos para o desenvolvimento seguro da apicultura com abelhas africanizadas. Empresa Brasileira de Pesquisa Agropecuária: Centro de Pesquisa Agropecuária do Pantanal. Ministério da Agricultura, Pecuária e Abastecimento, Documentos 118, 2011. 32 p.
- RINDERER T. E.; OLDROYD, B. P.; SHEPPARD, W. S. Africanized bees in the U.S. Scientific American, v. 269, p. 52-58, 1993.
- ROUBIK, D. W. Seasonality in colony food storage, brood production and adult survivorship: studies of Melipona in tropical forest (Hymenoptera: Apidae). Journal of the Kansas Entomological Society, v. 55, n. 4, p. 789-800, 1982.
- ROUBIK, D. W. Stingless bee nesting biology. Apidologie, v. 37, n. 2, p. 124-143, 2006.
- RUTTNER F.; TASSENCOURT L.; LOUVEAUX, J. Biometrical statistical analysis of the geographic variability of Apis mellifera L. Apidologie, v. 9, p. 363-381, 1978.
- SANTOS, A. B. Abelhas nativas: polinizadores em declínio. Natureza online, v. 8, p. 103-106, 2010.
- SANTOS, M. L. A., MESSAGE. D. Taninos causando sintomas da Cria Ensacada Brasileira. In: CONGRESSO BRASILEIRO DE APICULTURA, 12., Bahia, 1998, Anais [...]. Bahia, 1998, p. p. 251.
- SILVA, I. C. Efeito tóxico de Stryphnodendron polyphyllum (Fabaceae) para as abelhas Apis mellifera, Tetragonisca angustula, Scaptotrigona aff. depilis e Nannotrigona testaceicornis (Apidae). 2009. Tese de Doutorado. Faculdade de Filosofia Ciências e Letras, Universidade de São Paulo, Ribeirão Preto, 2012.
- SMODIS SKERL, M.I. E GREGORC, A. Heat shock proteins and cell death in situ localization in hypopharyngeal glands of honeybee (Apis mellifera carnica) workers after imidacloprid or coumaphos treatment. Apidologie, v. 41, p. 73-86, 2010. doi: 10.1051/apido/2009051
- SOARES, H. M. Avaliação dos efeitos do inseticida imidacloprido para abelhas sem ferrão Scaptotrigona postica Latreille, 1807 (Hymenoptera, Apidae, Meliponini). 2012. Dissertação de Mestrado. Universidade Estadual Paulista Júlio de Mesquita Filho, Rio Claro, 2012.
- SGOLASTRA, F.; MEDRZYCKI, P.; BORTOLOTTI, L.; MAINI, S.; PORRINI, C.; SIMON-DELSO, N.; BOSCH, J. Bees and pesticide regulation: Lessons from the neonicotinoid experience. Biological Conservation, v. 241, p. 108356, 2020.
- STANLEY, J.; SAH, K.; JAIN, S. K.; BHATT, J. C.; SUSHIL, S. N. Evaluation of pesticide toxicity at their field recommended doses to honeybees, Apis cerana and A. mellifera through laboratory, semi-field and field studies. Chemosphere, v. 119, p. 668-674, 2015.
- STEVENSON, J.H.; WALTER, J.H.H. Evaluation of pesticides for use with biological control. Agriculture Ecosystems Environmental, v. 1001, p. 29-39, 1983. doi: 10.1016/0167-8809(83)90062-2
- SAKAGAMI, S. F. Stingless bees. In: HERMANN, H. R. (Eds.), Social Insects, New York: Academic Press, 1982. p. 362-421.
- SEELEY, Thomas D. Honeybee Ecology: A Study of Adaption in Social Life. Princeton University Press, 1992.
- SEELEY, T. D. Ecologia da abelha: um estudo de adaptação na vida social. Paixão, 2006.
- SILVA, Alexandre Coletto da. Implantação da meliponicultura e etnobiologia de abelhas sem ferrão (Melipona) em comunidades indígenas no Estado do Amazonas. 2006. Tese (Doutorado em Entomologia) - Universidade Federal do Amazonas, Manaus, 2006.
- SILVA, W. P.; PAZ, J. R. L. Abelhas sem ferrão: muito mais do que uma importância econômica. Natureza online, v. 10, p. 146-152, 2012.
- SAKAMOTO, Y.; MAEDA, T.; YOSHIYAMA, M.; KONNO, F.; PETTIS, J.S. Differential autogrooming response to the tracheal mite Acarapis woodi by the honey bees Apis cerana and Apis mellifera. Insectes Sociaux, v. 67, p. 95-102, 2020. doi: 10.1007/s00040-019-00732-w
- SALDAÑA, L. M., LARA, L. G., & ANTONIO, D. J. Manual, Nuevos manejos en la apicultura para el control del pequeño escarabajo de la colmena Aethina tumida Murray. México DF. 2014.
- SAMMATARO, D.; GERSON, U.; NEEDHAM, G. Parasitic mites of honey bees: life history, implications, and impact. Annual Review of Entomology, v. 45, p. 519–548, 2000.
- SAMMATARO, D.; DE GUZMÁN, L.; GEORGE, S.; OCHOA, R.; OTIS, R. Standard methods for tracheal mite research. Journal of Apicultural Research, v. 52, p. 1–20, 2013. doi: 10.3896/IBRA.1.52.4.20
- SATTLER, A.; DISCONZI, M. S.; DUARTE, V.; SILVEIRA, J. R. P. Ocorrência de cria giz Ascosphaera apis em abelhas Apis mellifera L. de apiários no Rio Grande do Sul. In: XII Congresso Brasileiro de Apicultura, Salvador. Anais. 1998.
- SCHNEIDER, H. Untersuchugen uber due Acarapis: milben der honigbiene. Die flugel und hinterleibsmilbe. Mitteilungen der Schweizerischen Entomologischen Gesellschaft, v. 18, p. 318-327, 1941.
- SHEN, M.; YANG, X.; COX-FOXTER, D.; CUI, L. The role of varroa mites in infections of Kashmir bee virus (KBV) and deformed wing virus (DWV) in honey bees. Virology, v. 342, n. 1, p. 141-149, 2005. doi: 10.1016/j.virol.2005.07.012
- SHIMANUKI, H. BACTERIA. IN: MORSE, R.A.; FLOTTUM, K. (eds.). Honey bee pests, predators, and diseases. Medina: AI Root Co., 1997.
- SITAROPOULOU, N.; NEOPHYTOU, E. P.; THOMOPOULOS, G. N. Structure of the Nucleocapsid of A Filamentous Virus of the Honey Bee (Apis mellifera). Journal of Invertebrate Pathology. v. 53, p. 354–357, 1989. doi: 10.1016/0022-2011(89)90099-2
- SMART, M. D.; SHEPPARD, W. S. Nosema ceranae in age cohorts of the western honey bee (Apis mellifera). Journal of Invertebrate Pathology, v. 109, n. 1, p. 148-151, 2011. doi:10.1016/j.jip.2011.09.009
- SPIVAK, M.; REUTER, G. S. Resistance to American foulbrood disease by honey bee colonies Apis mellifera bred for hygienic behavior. Apidologie, v. 32, p. 555-565, 2001.doi: 10.1051/apido:2001103
- SPIVAK, M.; VAN ENGELDORP, D.; WILKINS, S.; GENERSH, E. Standard methods for American foulbrood research. Journal of Apicultural Research, v. 52, n. 1, p. 1-28, 2013.
- STEPHAN, J. G.; DE MIRANDA, J. R.; FORSGREN, E. American foulbrood in a honeybee colony: spore-symptom relationship and feedbacks between disease and colony development. BMC Ecology, v. 20, n. 15, 2020. doi: 10.1186/s12898-020-00283-w
- STRAPAZZON, R., CARNEIRO, F. E., GUERRA JCVJ, MORETTO, G. (2009). Genetic characterization of the mite Varroa destructor (Acari: Varroidae) collected from honey bees Apis mellifera (Hymenoptera, Apidae) in the state of Santa Catarina, Brazil. Genet Mol Res 8:990–997. https://doi.org/10.4238/vol8-3gmr567.
- SOMMEIJER, M. J.; BEUVENS, F. T.; VERBEEK, H. J. Distribution of labour among workers of Melipona favosa F: Construction and provisioning of brood cells. Insectes Sociaux, v. 29, n. 2, p. 222-237, 1982.
- SOARES, A. E. E. Captura de enxames com caixas iscas e sua importância no melhoramento de abelhas africanizadas. In: CONGRESSO BRASILEIRO DE APICULTURA, 2004, Natal. Anais [...]. Natal, CBA: 2004. 1 CDROM.
- SOARES, A. E. E. Abelhas africanizadas no Brasil. In: 64ª REUNIÃO ANUAL DA SBPC, 2012, São Luís. Anais [...]. Maranhão, 2012.
- SHEPPARD, W. S.; RINDERER, T. E.; GARNERY, L.; SHIMANUKI, H. Analysis of Africanized honey bee mitochondrial DNA reveals further diversity of origin. Genetics and Molecular Biology, v. 22 p. 73-75, 1999.
- TANTILLO, G.; BOTTARO, M.; DI PINTO, A.; MARTELLA, V.; DI PINTO, P.; TERIO, V. Virus infections of honeybees Apis mellifera. Italian Journal of Food Safety, v. 4, n. 3, p. 5364, 2015. doi: 10.4081/ijfs.2015.5364
- TEIXEIRA, É. W.; DE JONG, D.; SATTLER, A.; MESSAGE, D. Aethina tumida Murray (Coleoptera, nitidulidae), o pequeno besouro das colmeias, chega ao Brasil. Mensagem Doce, São Paulo, v. maio, n. 136, p. 2-10, 2016. Disponível em: < http://apacame.org.br/site/revista/mensagem-doce-n-136-maio-de-2016/nota-tecnica/ >. Acesso em: 15/08/2020.
- TEIXEIRA, E. W.; FERREIRA, E. A.; LUZ, C. F. P.; MARTINS, M. F.; RAMOS, T. A.; LOURENÇO, A. P. European Foulbrood in stingless bees (Apidae: Meliponini) in Brazil: Old disease, renewed threat. Journal of Invertebrate Pathology, v. 172, p. 107357, 2020. doi: 10.1016/j.jip.2020.107357
- TOMKIES, V.; FLINT, J.; JOHNSON, G.; WAITE, R.; WILKINS, S.; DANKS, C.; WATKINS, M.; CUTHBERTSON, A. G. S.; CARPANA, E.; MARRIS, G.; BUDGE, G.; BROWN, M. A. Development and validation of a novel field test kit for European foulbrood. Apidologie, v. 40, 2009. doi: 10.1051/apido:2008060
- TORRES, R. N. S.; BARRETO, M. R. Incidência de Varroa destructor (Anderson e Trueman) em criação de abelhas com ferrão na região de Sinop, MT. EntomoBrasilis, v.6, n.1, 2013.
- TASSINARI, W.; LORENZON, M.; PEIXOTO, E. Spatial regression methods to evaluate bee keeping production in the state of Rio de Janeiro. Arquivo Brasileiro de Medicina Veterinária e Zootecnia, v. 65, p. 553-558, 2013.
- TOLEDO, Vagner de Alencar Arnaut. Estudo comparativo de parâmetros biológicos e de produção de cera e geléia real em colônias de abelhas Apis mellifera africanizadas, cárnicas, italianas e seus híbridos. Tese (Doutorado em Zootecnia) - Faculdade de Ciências Agrárias e Veterinárias, Universidade Estadual Paulista, São Paulo, 1997.
- USDA – UNITED STATES DEPARTMENT OF AGRICULTURE. U.S. Cost of pollination. 2017. Disponível em: https://usda.library.cornell.edu/concern/publications/d504rk335?locale=en. Acesso em: 23 set. 2020.
- USDA Agricultural Projections to 2029. Office of the Chief Economist, World Agricultural Outlook Board, U.S. Department of Agriculture. Prepared by the Interagency Agricultural Projections Committee. Long-term Projections Report OCE-2020-1, 114 pp.
- THOMPSON, H. M. Esterases as markers of exposure to organophosphates and carbamates. Ecotoxicology, v. 8, n. 5, p. 369-384, 1999.
- THOMPSON, H. M. Risk assessment for honeybees and pesticides—recent developments and ‘new issues’. Pest Management Science, v. 66, n. 11, p. 1157-1162, 2010.
- TOLEDO, Vagner de Alencar Arnaut. Estudo comparativo de parâmetros biológicos e de produção de cera e geléia real em colônias de abelhas Apis mellifera africanizadas, cárnicas, italianas e seus híbridos. Tese (Doutorado em Zootecnia) - Faculdade de Ciências Agrárias e Veterinárias, Universidade Estadual Paulista, São Paulo, 1997.
- TRIGO, J. R.; SANTOS, W. Insect mortality in Spathodea campanulata Beauv. (Bignoniaceae) flowers. Revista Brasileira de Biologia, v.60, n.3, p.537-538, 2000.
- VAN DER SLUIJS, J. P.; SIMON-DELSO, N.; GOULSON, D.; MAXIM, L.; BONMATIN, J. M.; BELZUNCES, L. P. Neonicotinoids, bee disorders and the sustainability of pollinator services. Current Opinion in Environmental Sustainability, v. 5, n. 3-4, p. 293-305, 2013.
- VÁSQUEZ, A; OLOFSSON, T. C. The lactic acid bacteria involved in the production of bee pollen and bee bread. Journal of apicultural research, v. 48, n. 3, p. 189-195, 2009.
- VILLAS-BÔAS, J. Manual Tecnológico: Mel de abelhas sem ferrão. Brasília: Instituto Sociedade, população e Natureza (ISPN), 2012. 96 p.
- VIT, P.; PEDRO, S. R. M.; ROUBIK, D. Pot honey - a legacy of stingless bees. New York: Springer, 2013. 654 p.
- VOLLET-NETO, A.; MAIA-SILVA, C.; MENEZES, C.; IMPERATRIZ-FONSECA, V. L. Newly emerged workers of the stingless bee Scaptotrigona aff. depilis prefer stored pollen to fresh pollen. Apidologie, v. 48, n. 2, p. 204-210, 2017.
- WIESE, H. Apicultura – Novos Tempos. Guaíba: Agrolivros, 2005. 378 p.
- WHITE, G. F. Sacbrood. US Washington: Department of Agriculture, 1917. doi:10.5962/bhl.title.54400
- WHITEHORN, P.R.; O’CONNOR, S.; WACKERS, F.L.; GOULSON, D. Neonicotinoid pesticide reduces bumble bee colony growth and queen production. Science, v.336, p.351-352,
- 2012. DOI: 10.1126/science.1215025.
- WOLOWSKI, M., AGOSTINI, K., RECH, A. R., VARASSIN, I. G., MAUÉS, M., FREITAS, L., ... & SARAIVA, A. M. (2019). Relatório temático sobre polinização, polinizadores e produção de alimentos no Brasil. Espiríto Santo: REBIPP.
- WU, J. Y.; ANELLI, C. M.; SHEPPARD, W. S. Sub-lethal effects of pesticides residues in brood comb on worker honey bee (Apis mellifera) development and longevity. PloS one, v. 6, n. 2, p. e14720, 2011.
- WIESE, H. Nova apicultura. 6ª ed. Porto Alegre: Agropecuária, 1995.
- WOLFF, L. F. & NAVA, D. E. Ocorrência da mosca dos favos Pseudohypocera kerteszi (Diptera: Phoridae) em colmeias de abelhas melíferas africanizadas no Rio Grande do Sul. Pelotas, RS. Comunicado Técnico Embrapa Clima Temperado, 2007.
- WOYKE, J. Mating behaviour of the parasitic honey bee mite Tropilaelaps clareae. Experimental and Applied Acarology, v. 18, p. 723 –733, 1994. doi: 10.1007/BF00051539
- WOYKE, J. Survival and prophylactic control of Tropilaelaps clareae infesting Apis mellifera colonies in Afghanistan. Apidologie, v. 15, p. 421–434, 1984. doi: 10.1051/apido:19840405
- WINSTON, Mark L. The Biology of the Honey Bee. Harvard University Press, 1991.
- WINSTON, M. L. A biologia da abelha. Porto Alegre: Magister, 2003.
- WOLOWSKI, M.; AGOSTINI, K.; RECH, A. R.; VARASSIN, I. G.; MAUÉS, M.; FREITAS, L.; SILVA, C. I. Relatório temático sobre polinização, polinizadores e produção de alimentos no Brasil (BPBES). 2019. Disponível em: https://www.bpbes.net.br/producto/polinizacao-producao-de-alimentos/ Acesso em: 23 setembro 2020.
- WOLFF, L. F. Abelhas melíferas: bioindicadores e qualidade ambiental e de sustentabilidade da agricultura familiar de base ecológica. Pelotas: Embrapa Clima Temperado, 2008. 38 p. (Documento 244).
- WU, J. Y.; ANELLI, C. M.; SHEPPARD, W. S. Sub-lethal effects of pesticides residues in brood comb on worker honey bee (Apis mellifera) development and longevity. PloS one, v. 6, n. 2, p. e14720, 2011
- YONHSAWAS, R.; CHAINMANEE, V.; PETTIS, J. S.; BONCRISTIANI JR, H. F.; LOPEZ, D.; IN-ON, A.; CHANTAWANNAKUL, P.; DISAYATHANOOWAT, T. Impact of sacbrood virus on larval microbiome of Apis mellifera and Apis cerana. Insects, v.11, v. 7, p. 439, 2020. doi: 10.3390/insects11070439
- YUE, D.; NORDHOFF, M.; WIELER, L. H.; GENERSH, E. Fluorescence in situ hybridization (FISH) analysis of the interactions between honeybee larvae and Paenibacillus larvae, the causative agent of American foulbrood of honeybees (Apis mellifera). Environmental Microbiology, v. 10, n. 6, p. 1612-1620, 2008. doi: 10.1111/j.1462-2920.2008.01579.x
- ZORZENON, F. J. Noções sobre as principais pragas urbanas. Biológico, v.64, n.2, p.231-234, 2002.
¶ Disposições Gerais
As sugestões para aprimoramento ou possíveis correções deste documento devem ser direcionadas ao Departamento responsável, para alinhamento das melhores práticas de mercado, legislação vigente e/ou regulamentações, que não tenham sido contempladas na versão vigente.
¶ Histórico de revisões
| Versão | Conteúdo alterado | Data | Motivo |
|---|---|---|---|
| 1.0 | Inclusão dos tópicos: Folha de rosto, Folha resumo, Disposições gerais e Histórico de revisão. | 24/10/2022 | Transcrição do manual para o modelo de manualização validado pela SDA no Projeto de elaboração do modelo de manualização da SDA. |
¶ Anexos
¶ Checklist – Materiais de uso do SVO em atendimento às ocorrências de vigilância oficial (Loque americana, Loque europeia, Aethina tumida e Tropilaelaps sp.)*
| Itens do material permanente | Descrição/Observação | √ |
| Macacão completo | Com máscara destacável, conferir integridade do mesmo que não deve ter rasgos ou furos que permitam a entrada de abelhas | |
| Luvas | Luva de apicultor que proteja de ferroadas de abelhas | |
| Botas | Cano alto e rígido (caso contrário utilizar perneiras por dentro da calça do macacão, evitando incidentes com cobras peçonhentas), bom fechamento com o macacão para que não entre abelhas | |
| Fumigador | Conferir integridade e funcionamento do fole | |
| Formão | Deve estar limpo e desinfectado | |
| Faca | Deve estar limpa e desinfectada, preferencialmente toda de inox | |
| GPS | Conferir carga de baterias | |
| Itens de consumo ou que haja reposição frequente | Descrição/Observação | √ |
| Luvas de procedimento de látex | Considerar tamanho das luvas de apicultor utilizadas | |
| Material para combustão do fumigador | Deve ser usado material seco sem cheiro forte e livre de contaminantes (maravalha/cepilho de madeira sem tratamento, folhas de eucalipto, etc.) | |
| Caixa de fósforos e/ou isqueiro | Conferir integridade e funcionamento destes itens | |
| Álcool 70% | Para desinfecção de materiais e conservação de amostras, no mínimo 1 L, observar data de validade | |
| Sabão | Para limpeza de faca e formão | |
| Balde pequeno | Para limpeza de faca e formão | |
| Galão com água | Para limpeza de faca, formão e mãos | |
| Toalhas de papel | Para limpeza de faca e formão auxiliando remoção de resíduos de cera e própolis e secar as mãos | |
| Palha de aço ou bucha | Para limpeza de faca e formão auxiliando remoção de resíduos de cera e própolis | |
| Pinça | Remoção de material dentro dos alvéolos | |
| Palito de fósforo ou de dentes | Para direcionar suspeita de loque americana ou loque europeia | |
| Potes de amostras (500 mL) | Pote plástico de boca larga para amostras de favos de mel | |
| Tubos tipo Eppendorf | Coleta de larvas ou pupas suspeitas | |
| Etiqueta ou esparadrapo | Para identificação das amostras nos recipientes de coleta | |
| Caneta do tipo marcador permanente | Identificar as amostras | |
| Termo de coleta | Documentos impressos a partir do e-Sisbravet | |
| Lápis e caneta esferográfica | Preferencialmente lápis para identificação de amostras | |
| Envelope | Para envio de formulários | |
| Saco plástico | Para material de descarte (incinerar se caso de loque americana) | |
| Caixa isotérmica com gelo reciclável | Material extra para amostras em suspeitas de intoxicação por agrotóxicos (conforme descrito no capítulo 7) | |
| Caixa de papelão | Para acondicionar amostras maior que 25x18x15 cm | |
| Fita adesiva transparente larga ou crepe | Para fechar os punhos com as luvas e uso geral |
* Se investigação de interesse do programa estadual adicionar os materiais específicos