¶ Folha de rosto
© 2023 Ministério da Agricultura e Pecuária.
Todos os direitos reservados. Permitida a reprodução parcial ou total desde que citada a fonte e que não seja para venda ou qualquer fim comercial. A responsabilidade pelos direitos autorais de textos e imagens desta obra é do autor.
2ª edição. Ano 2023
Elaboração, distribuição, informações:
Ministério da Agricultura e Pecuária - MAPA
Secretaria de Defesa Agropecuária - SDA
Departamento de Saúde Animal - DSA
Coordenação-Geral de Prevenção e Vigilância em Saúde Animal - CGVSA
Coordenação de Prevenção e Vigilância de Doenças Animais - CDVIG
Divisão de Prevenção e Vigilância Animal V - DIVIG
Esplanada dos Ministérios - Bloco D - Anexo A - Sala 326
Brasília-DF CEP: 70.043 900
Tel.: +55 (61) 3218-2473
e-mail: pnss@agro.gov.br https://www.gov.br/agricultura/pt-br/
Coordenação Editorial: Assessoria Especial de Comunicação Social - AECS
Créditos das imagens: MAPA/iStock; DejaVu Designs/Freepik; Mark Stebnicki;
Catalogação na Fonte
Biblioteca Nacional de Agricultura – BINAGRI
Dados Internacionais de catalogação na Publicação (CIP) Biblioteca Nacional de Agricultura – BINAGRI
|
Brasil. Ministério da Agricultura e Pecuária. Plano integrado de vigilância de doenças dos suínos / Ministério da Agricultura e Pecuária. Secretaria de Defesa Agropecuária. Departamento de Saúde Animal. – 2ª. ed. – Brasília : MAPA/SDA, 2023. 68 p. : il. Recurso: Digital Formato: PDF ISBN:978-85-7991-209-2 1. Suinocultura. 2. Sanidade Animal. 3. Peste Suína Clássica . 4. Peste Suína Africana. 5. Síndrome Reprodutiva e Respiratória dos Suínos. 6. Sistema de vigilância. I. Secretaria de Defesa Agropecuária. II. Título. AGRIS L73 5300 |
Layla Alexandrina Barboza dos Santos CRB1 - 3447
¶ Definições e conceitos
CC: Ciclo completo
DSA: Departamento de Saúde Animal
ELISA: Ensaio imunoenzimático
e-Sisbravet: Ferramenta eletrônica específica para gestão dos dados obtidos da vigilância passiva em saúde animal, desenvolvida para o registro e acompanhamento das notificações imediatas de suspeitas de doenças e das investigações realizadas pelo Serviço Veterinário Oficial.
GRSC: Granja de Reprodutores Suínos Certificada
MAPA: Ministério da Agricultura, Pecuária e Abastecimento
OESA: Órgão Estadual de Sanidade Agropecuária
OMSA: Organização Mundial de Saúde Animal
PCR: Reação em cadeia da polimerase
PSA: Peste Suína Africana
PSC: Peste Suína Clássica
PRRS: Síndrome Reprodutiva e Respiratória dos Suínos
PNSS: Programa Nacional de Sanidade Suídea
SEI: Sistema Eletrônico de Informações
SDA: Secretaria de Defesa Agropecuária
SVO: Serviço Veterinário Oficial
UPL: Unidade Produtora de Leitões
VN: Neutralização Viral
ZL de PSC: Zona Livre do vírus da peste suína clássica
ZnL de PSC: Zona não Livre do vírus da peste suína clássica
¶ Responsabilidades
O presente manual possui vigência e prazo indeterminado e será revisado sempre que necessário, ou a cada três anos, pelo setor responsável do Departamento de Saúde Animal (DSA) e aprovada pela Secretaria de Defesa Agropecuária (SDA).
A gestão deste manual está sob a responsabilidade do DSA, que prestará auxílio ao público-alvo leitor. Dúvidas e/ou sugestões quanto à aplicação deste manual devem ser submetidas ao e-mail pnss@agro.gov.br.
A publicação e atualização das versões na plataforma oficial da SDA para acesso pelo público-alvo será de responsabilidade da Secretaria representada pelo DSA.
¶ Procedimentos
¶ 1. INTRODUÇÃO
O Brasil é o quarto maior produtor mundial de carne suína, com um rebanho de mais de 40 milhões de animais, abastece o mercado nacional com cerca de 80% dessa produção e exporta o restante, sendo o quarto maior exportador mundial desta proteína. A suinocultura brasileira possui condição sanitária bastante favorável por ser considerada livre de doenças economicamente muito importantes que ocorrem em várias partes do mundo, notadamente a Peste Suína Africana (PSA) e a Síndrome Reprodutiva e Respiratória dos Suínos (PRRS) e por possuir uma vasta zona livre de Peste Suína Clássica (PSC). A manutenção desta condição sanitária no Brasil garante menores custos de produção e vantagem competitiva no acesso a mercados internacionais.
Entretanto, o crescente trânsito internacional de pessoas, o comércio internacional de animais e produtos, a intensificação da produção pecuária e outros fatores contribuem para um aumento dos riscos de introdução e disseminação de doenças cujos impactos sociais, econômicos e ambientais podem ser extremamente altos. Além disso, diante dos crescentes riscos sanitários, os parceiros comerciais exigem evidências cada vez mais robustas para a certificação dos animais e produtos comercializados. Ademais, as condições para certificações de zonas livres de doenças estabelecidas pela Organização Mundial de Saúde Animal (OMSA) baseiam-se em princípios técnicos e científicos, que estão em contínuo avanço.
Nesse sentido, a vigilância representa a principal atividade em saúde animal que permite a detecção precoce de doenças animais emergentes e reemergentes, viabilizando o controle e a erradicação eficiente, bem como a certificação de zonas livres de doenças, sustentando o acesso dos sistemas produtivos ao comércio nacional e internacional.
Este Plano integrado de vigilância revisa a primeira versão, publicada em 2021 e executada 2021 e 2022, pelo Departamento de Saúde Animal (DSA), vinculado à Secretaria de Defesa Agropecuária (SDA) do Ministério da Agricultura, Pecuária e Abastecimento (MAPA), para a vigilância de PSC, PSA e PRRS. O Plano foi delineado inicialmente para as três doenças, mas pode ser aplicado e adaptado para outras, considerando alterações na situação epidemiológica, demandas relacionadas ao comércio, interesses dos setores público e privado e disponibilidade de recursos. Os resultados satisfatórios e os aprendizados obtidos no 1º ciclo do plano de vigilância permitem promover adequações e melhorias para o 2º ciclo.
O Plano integrado de vigilância de doenças de suínos foi desenvolvido pelo Serviço Veterinário Oficial (SVO) em colaboração com os setores da iniciativa privada, representando o compromisso em manter e melhorar a vigilância animal implantada no Brasil
¶ 2. CONTEXTO ATUAL DAS DOENÇAS NO BRASIL (PSC, PSA e PRRS)
¶ 2.1 Peste Suína Clássica (PSC)
O processo de reconhecimento internacional de zonas livres (ZL) do vírus da PSC priorizou as regiões de maior relevância para produção e exportação de suínos e seus produtos. Atualmente, cerca de 83% do rebanho suíno brasileiro encontra-se em ZL do vírus da PSC, envolvendo, aproximadamente, 50% do território nacional. A condição zoossanitária da doença no Brasil, reconhecida pela OMSA, está constituída da seguinte forma:
- três zonas Livres: uma constituída pelos estados do Rio Grande do Sul e de Santa Catarina; outra pelos estados do Acre, Bahia, Distrito Federal, Espírito Santo, Goiás, Mato Grosso, Mato Grosso do Sul, Minas Gerais, Rio de Janeiro, Rondônia, São Paulo, Sergipe, Tocantins e os municípios de Guajará, Boca do Acre, sul do município de Canutama e sudoeste do município de Lábrea, pertencentes ao estado do Amazonas; e outra formada pelo estado do Paraná.
- uma zona não Livre (ZnL): formada pelos estados de Alagoas, Amapá, Amazonas (exceto região pertencente à ZL), Ceará, Maranhão, Pará, Paraíba, Pernambuco, Piauí, Rio Grande do Norte e Roraima.
O PNSS trabalha em duas linhas: manter a condição zoossanitária nas ZL e evoluir no processo de erradicação do vírus da PSC na ZnL, buscando o reconhecimento de todo o país como livre. Os objetivos são associados, uma vez que a erradicação do vírus da PSC na ZnL contribui para garantir a condição sanitária na ZL.
¶ 2.2 Peste Suína Africana (PSA)
A PSA foi introduzida no Brasil em 1978, no município de Paracambi no estado do Rio de Janeiro. As investigações realizadas à época revelaram que os suínos do estabelecimento caracterizado como foco índice se infectaram pela ingestão de sobras de comida servida a bordo de aviões procedentes de Portugal e da Espanha, países onde grassava a doença.
A última ocorrência de PSA no Brasil foi registrada no município de Moreno, estado de Pernambuco, em novembro de 1981. As medidas aplicadas pelo SVO brasileiro permitiram a erradicação da doença em todo seu território e a declaração de país livre de PSA em 1984, porém com alto custo para o país.
A partir de 2018, a PSA ingressou e se dispersou amplamente nos continentes asiático e europeu, chegando ao continente americano em 2021. O MAPA, os Órgãos Estaduais de Sanidade Agropecuária (OESA) e os setores privados da suinocultura têm desenvolvido e reforçado ações que evitem o ingresso da PSA no Brasil e que possam mitigar os impactos econômicos e sociais no caso de introdução da doença.
A realização da vigilância direcionada à PSA é uma das formas de cumprir os objetivos do “Plano de Ação para Prevenção da PSA – versão 2.0 de fevereiro de 2020” (SEI 21000022137/2020-47) que busca elencar, organizar e orientar as ações prioritárias, definir responsabilidades, identificar os principais obstáculos e os recursos necessários para fortalecer a prevenção e a vigilância da doença para manutenção da condição sanitária do Brasil como país livre de PSA
¶ 2.3 Síndrome Reprodutiva e Respiratória dos Suínos (PRRS)
A PRRS foi descrita inicialmente nos Estados Unidos em 1987, na Europa em 1990 e logo após na Ásia. A PRRS causa alta mortalidade em suínos recém-nascidos e desmamados, baixa taxa de concepção em rebanhos de reprodutores, aumento na taxa de aborto, natimortos e nascimento de leitões fracos, acarretando enormes perdas econômicas aos produtores.
Pela experiência de países com suinocultura altamente especializada nas quais houve entrada da doença, foram notadas características muito preocupantes da PRRS, como alta taxa de difusão, falta de vacinas eficientes e incapacidade de medidas estritas de biosseguridade em evitar a infecção de granjas livres. O vírus da PRRS já foi identificado em importantes países produtores de suínos, sendo endêmico em vários deles.
No Brasil, a PRRS nunca foi registrada e trabalhos científicos publicados, analisando diversos estratos da cadeia produtiva de suínos no Brasil, sempre demonstram a ausência de anticorpos ou RNA para o vírus da PRRS. Neste sentido, o Brasil adota rigorosos controles de importação de suínos para reprodução e material genético, com vistas a mitigar o risco de introdução desta doença em território nacional.
Dada a importância dos impactos econômicos e sociais no caso de introdução da PRRS no Brasil, se faz necessário fortalecer o sistema de prevenção, vigilância e resposta a uma possível detecção da doença.
¶ 3. DESCRIÇÃO DAS DOENÇAS E DEFINIÇÕES DE CASOS
Para mais informações e detalhes referentes às doenças e respectivas definições de caso, consultar: Ficha técnica da PSC, Ficha Técnica da PSA e Ficha Técnica da PRRS (https://sistemasweb.agricultura. gov.br/pages/fichas_tecnicas/ficha_tecnica.html).
¶ 3.1. Peste Suína Clássica
¶ 3.1.1. Caso Suspeito de PSC
- Suíno (doméstico ou asselvajado) com sinais clínicos ou lesões compatíveis com PSC, associados ou não ao aumento das taxas de mortalidade.
¶ 3.1.2. Caso Provável de PSC
- Suíno com sinais clínicos ou lesões compatíveis com PSC constatados pelo SVO; ou
- Resultado positivo em teste de RT-PCR em amostra de vigilância ativa para PSC.
- A constatação de caso provável de PSC exige a adoção imediata de medidas de biosseguridade e de providências para o diagnóstico laboratorial para a exclusão ou a confirmação da doença.
¶ 3.1.3. Caso Confirmado de PSC
- Isolamento e identificação do vírus da PSC em amostras procedentes de um ou mais suínos com ou sem sinais clínicos da doença; ou
- Identificação de antígeno viral, excluindo cepas vacinais, ou ácido nucleico específico do vírus da PSC em amostras procedentes de um ou mais suínos com sinais clínicos ou lesões compatíveis com PSC; ou epidemiologicamente vinculados a um caso confirmado de PSC; ou com indícios de exposição ao vírus da PSC; ou
- Detecção de anticorpos específicos do vírus da PSC, que não sejam consequência da vacinação ou de infecção por outro Pestivirus, em amostras de um ou mais suínos com sinais clínicos ou lesões compatíveis com PSC; ou epidemiologicamente vinculados a um caso confirmado de PSC; ou com indícios de exposição ao vírus da PSC.
OBS 1: o primeiro caso/foco em zona livre de PSC deverá ser confirmado com isolamento e identificação do vírus.
OBS 2: em um foco de PSC já confirmado, todos os suínos com sinais clínicos compatíveis com PSC serão considerados casos confirmados
¶ 3.2. Peste Suína Africana
¶ 3.2.1. Caso Suspeito de PSA
- Suíno (doméstico, silvestre ou asselvajado) com sinais clínicos ou lesões compatíveis com PSA associados ou não ao aumento das taxas de mortalidade.
¶ 3.2.2. Caso Provável de PSA
- Suíno com sinais clínicos ou lesões compatíveis com PSA constatados pelo SVO; ou
- Resultado positivo em teste de PCR em amostra de vigilância ativa para PSA.
A constatação de caso provável de PSA exige a adoção imediata de medidas de biosseguridade e de providências para o diagnóstico laboratorial para a exclusão ou a confirmação da doença.
¶ 3.2.3. Caso Confirmado de PSA
- Isolamento e identificação do vírus da PSA em amostras procedentes de um ou mais suínos com ou sem sinais clínicos da doença; ou
- Identificação de antígeno viral ou ácido nucleico específico do vírus da PSA em amostras procedentes de um ou mais suínos com sinais clínicos ou lesões compatíveis com PSA; ou epidemiologicamente vinculados a um caso confirmado da PSA; ou com indícios de exposição ao vírus da PSA.
OBS 1: o primeiro caso/foco de PSA no Brasil deve ser confirmado com isolamento e identificação do vírus seguido de sequenciamento genético.
OBS 2: em um foco de PSA já confirmado, todos os suínos com sinais clínicos compatíveis com PSA serão considerados casos confirmados.
¶ 3.3. Síndrome Respiratória e Reprodutiva dos Suínos - PRRS
¶ 3.3.1. Caso Suspeito de PRRS
- Suíno (doméstico ou asselvajado) com sinais clínicos ou lesões compatíveis com PRRS, associados ou não ao aumento das taxas de mortalidade.
¶ 3.3.2. Caso Provável de PRRS
- Suíno com sinais clínicos ou lesões compatíveis com PRRS constatados pelo SVO; ou
- Resultado positivo em teste de PCR em amostra de vigilância ativa para PRRS. A constatação de caso provável de PRRS exige adoção imediata de medidas de biosseguridade e de providências para o diagnóstico laboratorial para a exclusão ou a confirmação da doença.
¶ 3.3.3. Caso Confirmado de PRRS
- Isolamento e identificação do vírus da PRRS em amostras procedentes de um ou mais suínos com ou sem sinais clínicos da doença; OU
- Identificação de antígeno viral ou ácido nucleico específico do vírus da PRRS em amostras procedentes de um ou mais suínos com sinais clínicos ou lesões compatíveis com PRRS; ou epidemiologicamente vinculados a um caso confirmado de PRRS.
OBS 1: o primeiro caso/foco de PRRS no Brasil deve ser confirmado com isolamento seguido de sequenciamento genético.
OBS 2: em um foco de PRRS já confirmado, todos os suínos com sinais clínicos compatíveis com PRRS serão considerados casos confirmados.
¶
4. PROPÓSITOS E JUSTIFICATIVAS
A situação da PSC na ZnL do País, a ocorrência da PRRS nos principais países produtores de suínos e o aumento da disseminação da PSA na Ásia, Europa e outras partes do mundo aumentam a preocupação com a possível introdução e disseminação dessas doenças no Brasil ou na zona livre, no caso da PSC.
A rápida detecção de uma eventual introdução dessas doenças é essencial para o sucesso das ações de resposta a emergências, o controle e erradicação do foco, com objetivo de recuperação rápida da condição sanitária. Essa detecção precoce pode ser dificultada pelas semelhanças dos quadros clínicos com outras doenças presentes nos sistemas de produção. Faz-se necessário atualizar os conhecimentos dos produtores, tratadores e técnicos do setor privado sobre as doenças, bem como fortalecer a interação com o SVO para assegurar uma detecção rápida e precisa de doenças.
Os componentes de vigilância ativa de PSC, PSA e PRRS, na atual zona livre de PSC, têm grande relevância para demonstrar a ausência das doenças, visando a certificação para comércio de suínos e seus produtos do Brasil aos mais diversos mercados. Sua realização de forma continuada e com níveis adequados de sensibilidade também permite identificar surgimento ou mudanças em fatores de risco e a adoção de medidas de gestão que promovam a mitigação, além do direcionamento eficiente de recursos para áreas e setores estratégicos.
Os dados padronizados e auditáveis do sistema de vigilância devem ser capazes de suportar processos de análises de risco e avaliações do próprio Plano integrado de vigilância, de forma a auxiliar a definição de políticas sanitárias e estratégias de curto, médio e longo prazo do PNSS.
Assim, o DSA, após revisão dos procedimentos em vigor, propõe um Plano integrado de vigilância para PSC, PSA e PRRS visando fortalecer a vigilância e a resposta às emergências para estas doenças, além de otimizar o uso de recursos empenhados, com o propósito principal de proteger a suinocultura e a economia nacional da ocorrência das doenças mencionadas e de seus impactos econômicos e sociais, além de garantir a certificação para acesso a mercados.
¶ 5. OBJETIVOS
Este documento descreve um Plano integrado de vigilância que se baseia nas metodologias de diagnóstico atualmente disponíveis e visa atingir os seguintes objetivos:
¶ Objetivo 1: fortalecer a capacidade de detecção precoce de casos de PSC, PSA e PRRS
A detecção precoce de casos suspeitos de PSC, PSA e PRRS, seguido do atendimento imediato e preciso às notificações, constitui a base da vigilância passiva e da preparação e resposta a emergências zoossanitárias.
Ademais, as notificações e investigações de casos suspeitos, realizados de forma precoce e consistente, oferecem uma sólida base de dados de ausência das doenças que contribui para a avaliação situacional no início de um eventual surto e para evidenciar a ausência das doenças investigadas. Este Plano integrado de vigilância amplia o escopo da vigilância de casos suspeitos, buscando detectar não somente a síndrome hemorrágica dos suínos, tendo como alvo a PSC e a PSA, mas também quadros compatíveis com a PRRS.
Outro aspecto importante é que essas investigações, aliadas aos demais componentes de vigilância, mantêm em atividade as ações e a capacidade dos sistemas de informação zoossanitária, de colheita e envio de amostras, de laboratórios e de gestão de emergências, condições essenciais para uma adequada resposta em caso de ocorrências de algum caso confirmado, quando a demanda é súbita e volumosamente aumentada.
¶ Objetivo 2: demonstrar a ausência de PSC, PSA e PRRS nas populações de suínos domésticos
Os dados gerados pelo sistema de vigilância para PSC, PSA e PRRS, em suínos domésticos e asselvajados, devem ser capazes de certificar a condição de zonas livres fornecendo suporte contínuo às confirmações de condição sanitária junto à OIE e aos parceiros comerciais. Esse suporte poderá ser obtido a partir dos dados provenientes da execução das atividades previstas neste Plano, sem necessidade de estudos e amostragens adicionais.
A contínua busca ativa (clínica e laboratorial) das doenças alvo, em setores de maior risco da cadeia produtiva, também contribui para aumentar as chances de detecção precoce de casos ou de reações sorológicas compatíveis com ocorrência de transmissão viral.
A princípio, considerando a ausência de casos na região das Américas e as características da PSA, o componente de vigilância sorológica para demonstração da condição de livre da doença não será executado. Havendo qualquer alteração relevante na situação epidemiológica da PSA na região, a amostragem da vigilância sorológica para PSC e PRRS passa a ser testada também para PSA.
¶ 6. RESULTADOS ESPERADOS
O desenvolvimento das ações previstas nesse Plano está relacionado com o atendimento dos objetivos descritos no item 5.
Todos os dados coletados deverão ser registrados nos sistemas específicos para vigilância passiva (e-SISBRAVET) e ativa definidos pelo MAPA.
Os resultados serão apresentados na forma de:
- Registros e bases de dados dos respectivos sistemas de informação utilizados para gestão da vigilância;
- Relatório anual do sistema de vigilância; e
- Análises de desempenho dos componentes do sistema e avaliação de indicadores de vigilância.
As informações resultantes serão usadas pelos gestores do sistema para a tomada de decisões e ações específicas como:
- Atendimento imediato e investigação no prazo máximo de 12 horas de suspeitas de Síndromes Hemorrágicas notificadas ao serviço oficial de saúde animal, para descartar ou confirmar as doenças alvo;
- Avaliação do desempenho na execução da vigilância passiva para orientar os procedimentos durante as investigações;
- Ativação do sistema de resposta rápida em caso de confirmação de foco das doenças;
- Adequação das capacidades de detecção e resposta com base nos resultados dos indicadores da vigilância ou diante de indicação de aumento potencial de risco à população suscetível;
- Subsidiar as garantias de certificações e negociações comerciais que exijam a comprovação da condição de livre das doenças; e
- Revisão de estratégias e procedimentos quando forem detectadas as doenças-alvo.
O Plano Integrado de Vigilância deverá ser avaliado em seus parâmetros e estrutura a cada 3 anos. Atualizações poderão ser realizadas após as mudanças nas avaliações de riscos ou quando o DSA julgar necessário.
Mudanças significativas nos fatores de risco que aumentem a probabilidade de introdução das doenças na zona livre de PSC do país devem levar a uma revisão desse Plano, mesmo que fora da periodicidade estabelecida.
¶ 7. PARTES INTERESSADAS
No Brasil, o SVO é formado pelos setores das instituições governamentais que executam procedimentos relacionados à saúde animal, como o MAPA, representando a instância central e superior, e os OESAs, representando as instâncias intermediárias e locais. O SVO é um dos principais atores do sistema de vigilância para PSC, PSA e PRRS, pois é o responsável pela sua coordenação e avaliação.
Também compõem o Plano integrado de vigilância para PSC, PSA e PRRS, como partes interessadas, os atores envolvidos ou beneficiados, direta ou indiretamente.
A Tabela 1 demonstra as responsabilidades dos segmentos envolvidos ou interessados no Plano.
Tabela 1. Responsabilidades dos segmentos envolvidos ou interessados no Plano integrado de vigilância para PSC, PSA e PRRS.
| Partes interessadas | Descrição | Responsabilidade | Tipo de participação |
|---|---|---|---|
| Serviço Veterinário Oficial | Médicos veterinários e pessoal auxiliar ligados diretamente ao SVO, por vínculo institucional | Autoridade Sanitária: normatizar, gerenciar, manter o banco de dados, analisar e divulgar as informações, investigar suspeitas, inspecionar suínos, colher amostras, capacitação, educação, comunicação e financiamento | Vigilância clínica e diagnóstica |
| Produtores | Detentores de suínos | Notificação de suspeitas; adoção de boas práticas de produção, medidas de biosseguridade e registros das atividades; financiamento. | Vigilância clínica |
| Embrapa e outras Instituições de pesquisa | Médicos veterinários, zootecnistas, agrônomos e auxiliares | Pesquisas, notificação de suspeitas; difusão de informações, capacitação | Vigilância clínica e diagnóstica |
| Indústria | Segmento agroindustrial de produtos de origem animal e fornecedores de insumos pecuários | Notificação de suspeitas; difusão de informações; fornecimento de informações de vigilância indireta, financiamento, biosseguridade | Vigilância clínica |
| Laboratórios credenciados | laboratórios públicos ou privados credenciados pelo MAPA para realização dos testes de triagem | Notificação de suspeitas; difusão de informações; realização de testes sorológicos de triagem | Vigilância clínica e diagnóstica |
| Laboratórios privados | Laboratórios privados que realizam testes diagnósticos de doenças do sistema de produção | Notificação de suspeitas; difusão de informações, envio de amostras recebidas de casos clínicos compatíveis ao LFDA | Vigilância clínica e diagnóstica |
| Médicos Veterinários Habilitados | Médicos veterinários privados com delegação de competência do SVO para execução de ação específica | Notificação de suspeitas; colheita de amostras; gerar informação de interesse (relatórios de produtividade); biosseguridade; difusão de informações | Vigilância clínica |
| Prestadores de serviços | Serviços eventuais ou permanentes: consultorias, atendimento clínico, revendas agropecuárias, vacinadores, recolhimento de suínos mortos | Notificação de suspeitas; difusão de informações, biosseguridade | Vigilância clínica |
| Médicos veterinários e profissionais dos serviços de meio ambiente | médicos veterinários, biólogos, zootecnistas e outros profissionais que atuam na área de conservação ambiental e gestão de áreas de preservação | Notificação de suspeitas; colheita de amostras; difusão de informações, biosseguridade; | Vigilância clínica e colheitade amostras |
| Agentes de manejo populacional | pessoas físicas ou jurídicas autorizadas pelo órgão ambiental a realizar o manejo populacional de suínos asselvajados | Notificação de suspeitas; colheita de amostras; difusão de informações, biosseguridade | Vigilância clínica e colheita de amostras |
| CNA | Confederação da Agricultura e Pecuária do Brasil | Difusão de informações; financiamento; apoio institucional | Vigilância clínica |
| ABCS | Associação Brasileira de Criadores de Suínos e associações estaduais de criadores | Difusão de informações; financiamento; apoio institucional | Vigilância clínica |
| ABPA | Associação Brasileira de Proteína Animal | Difusão de informações; financiamento; apoio institucional | Vigilância clínica |
| ABEGS | Associação Brasileira das Empresas de Genética Suína | Difusão de informações; financiamento; apoio institucional | Vigilância clínica |
| Fundos de defesa sanitária animal | associações instituídas com a finalidade de arrecadar fundos para indenizações de apoio às ações de defesa agropecuária | Difusão de informações; financiamento | Vigilância clínica |
| Extensão rural | Médicos veterinários e auxiliares | Notificação de suspeitas; difusão de informações, biosseguridade | Vigilância clínica |
| Transportadores de suínos | Profissionais que realizam transporte de suínos entre as propriedades e para o abate | Notificação de suspeitas; difusão de informações, biosseguridade | Vigilância clínica |
| Vigilância agropecuária internacional | médicos veterinários e pessoal auxiliar ligados à vigilância do trânsito internacional de animais e mercadorias | Notificação de suspeitas; difusão de informações, biosseguridade | Vigilância clínica |
¶ 8. DESCRIÇÃO DA POPULAÇÃO-ALVO
O presente Plano integrado de vigilância para PSC, PSA e PRRS deverá, inicialmente, ser aplicado em toda área geográfica da zona livre de PSC do Brasil (RS, SC, AC, BA, DF, ES, GO, MT, MS, MG, PR, RJ, RO, SP, SE, TO e os municípios de Guajará, Boca do Acre, sul do município de Canutama e sudoeste do município de Lábrea, pertencentes ao estado do AM).
_(pdf.io).jpg)
Este Plano fundamenta-se na caracterização da população de suínos do Brasil, separada em três distintas partes assim denominadas: Suinocultura Tecnificada, Suinocultura Não Tecnificada e População de Suínos Asselvajados, tal divisão encontra-se ilustrada abaixo:
SUINOCULTURA TECNIFICADA: representa o conjunto de criações feitas por produtores tecnificados, ou seja, que incorporam os avanços tecnológicos em genética, nutrição, sanidade, biosseguridade e que fazem o acompanhamento dos índices zootécnicos de sua produção. Nesse grupo encontram-se empresas de genética, grandes e médias agroindústrias, suinocultores integrados, cooperados e independentes que acessam os principais canais de processamento e distribuição da cadeia produtiva.
Nesse grupo encontram-se estabelecimentos das categorias:
• Granja de Reprodutores Suínos Certificada (GRSC): estabelecimento que cumpre integralmente os requisitos estabelecidos para certificação de atendimento a padrões diferenciados de biosseguridade e certificados como livre das doenças especificadas;
• Unidade Produtora de Leitões (UPL): estabelecimento comum em sistemas de integração ou em cooperativas. Envolvendo as fases de cobertura, gestação, maternidade, creche e central de inseminação de uso exclusivo;
• Creche: estabelecimento que recebe os leitões desmamados da UPL para criá-los apenas na fase de creche;
• Terminação: estabelecimento que recebe suínos da creche com a finalidade de engorda para posterior envio ao abate;
• Ciclo Completo (CC): estabelecimento predominante entre as suinoculturas independentes. Esse modelo engloba todas as fases da produção, ou seja, o mesmo estabelecimento contempla desde a chegada de leitoas destinadas à reprodução até o fim da terminação.
SUINOCULTURA NÃO TECNIFICADA: o conjunto de criações de produtores não tecnificados, que não incorporam os avanços tecnológicos (sobretudo em genética, nutrição, sanidade e biosseguridade) e para os quais a produção de suínos é destinada ao consumo próprio (subsistência) ou ao comércio local ou microrregional (comercial), acessando de forma limitada alguns canais de processamento e distribuição da cadeia produtiva.
Constituem essa população:
• Suinocultura Não Tecnificada de Subsistência: estabelecimentos em que a produção de suínos é destinada ao consumo próprio;
• Suinocultura Não Tecnificada de Comércio Local: estabelecimentos que, em regra, são de pequeno porte e destinados ao comércio local, acessando de forma limitada alguns canais de processamento e distribuição da cadeia produtiva.
As características para identificação desse tipo de criação estão descritas no Anexo I.
POPULAÇÃO DE SUÍNOS ASSELVAJADOS: animais da espécie Sus scrofa, que inclui o porco doméstico (Sus scrofa domesticus), suas diferentes formas, raças e linhagens, o javali-europeu (Sus scrofa scrofa) e todos os diferentes graus de cruzamento entre estas subespécies em vida livre, ou seja, vivendo em condição selvagem.
Nota: As espécies Tayassu tajacu e o Tayassu pecari conhecidos popularmente como cateto e queixada, respectivamente, pertencem à família Tayassuidae, que apesar de serem conhecidas popularmente como porcos-do-mato, não pertencem à família Suidae e, portanto, não são alvo deste Plano.
Apesar de não haver dados quantitativos da população de suínos asselvajados no Brasil, sua distribuição pelo território nacional pode ser acessada pelo Sistema de Informação de Manejo de Fauna – SIMAF, gerido pelo IBAMA e por mapas de percepção da presença de suínos asselvajados no Brasil, realizado pelo MAPA. A Figura 2 ilustra essa distribuição no País.
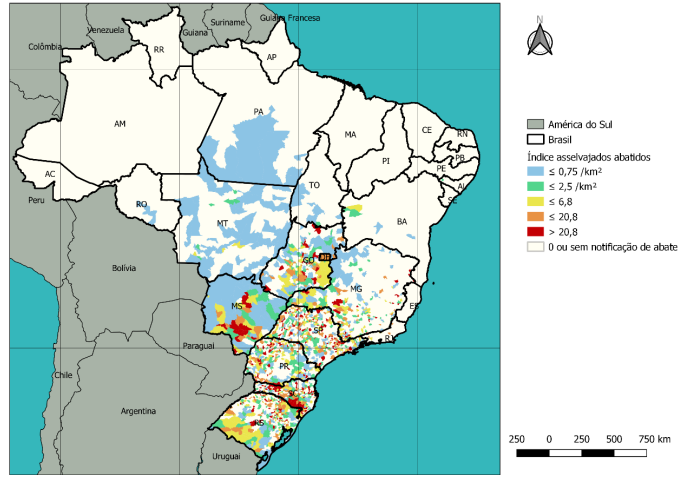
¶ 9. FONTES E USO DE DADOS
Tabela 2. Principais fontes de dados do PNSS.
| Tipo de dados | Fonte do dado | Local de registro e acesso | Descrição |
|---|---|---|---|
| Registros de notificações e investigações das suspeitas de doenças de notificação obrigatória em suínos | MAPA e OESA | e-Sisbravet | Inseridos sob responsabilidade do OESA e gerenciados pelo OESA e MAPA. O PNSS utiliza esses dados para acompanhar os atendimentos às ocorrências de casos prováveis de PSC, PSA e PRRS e avaliar a vigilância a partir da notificação de suspeitas. |
| Cadastros de estabelecimentos e rebanhos com sua geolocalização | OESA | Sistema informatizado do OESA | Registrados em bancos de dados pelos OESA, atualizados pelos produtores rurais e utilizados no delineamento da vigilância. |
| Registros da movimentação animal pela emissão da Guia de Trânsito Animal(GTA) | OESA | Sistema informatizado do OESA | Realizados pelos produtores e médicos veterinários habilitados e OESA e utilizados pelo PNSS para estruturar ações de gestão zoossanitária, como fiscalização de trânsito animal, identificação de estabelecimentos de maior concentração da movimentação e interrelações entre as áreas do país. |
| Cadastros de estabelecimentos de abate e informações de suínos abatidos e inspeção oficial | MAPA e OESA | PGA-SIGSIF e Sistema informatizado do OESA |
Dados consolidados tanto pelo MAPA (estabelecimentos sob fiscalização federal) como pelos OESA (estabelecimentos de abate estadual e municipal). São utilizados pelo PNSS para analisar a vigilância em abatedouros. |
| Registro dos dados da vigilância de inspeção de estabelecimentos e gestão das atividades do PNSS | MAPA e OESA | SIGEP |
Consolidados pelos OESA e encaminhados ao MAPA, servindo de base para a realização das análises para avaliação do sistema de vigilância para as doenças de notificação obrigatória em suínos no País. |
| Registro de dados de recursos humanos, financeiros e estruturais dos OESA, dos fundos de emergência e do MAPA | MAPA e OESA | Planilhas de relatórios anuais | Atualizados e consolidados anualmente pelos OESA e SFA servem de complemento para a realização das análises do PNSS. |
| Registro dos dados da vigilância internacional | MAPA/VIGIAGRO | SIGVIG e planilhas | Obtidos do VIGIAGRO nos pontos de ingresso de pessoas, animais e mercadorias diversas |
| Registro dos dados dos laboratórios oficiais e credenciados | LFDA e laboratórios credenciados | SIGEP | Utilizados pelo PNSS para análises relacionadas à vigilância a partir de notificações e vigilância sorológica. |
| Registros de dados da vigilância sorológica ativa | MAPA | SIGEP | Registrados pelo OESA no SIGEP e gerenciados pelo DSA. |
| Informações sobre suínos asselvajados | IBAMA | SIMAF | Registrados pelo IBAMA e agentes de manejo populacional |
| Dados de estudos e pesquisas | Instituições de pesquisa | Artigos científicos e resultados de estudos | Produzidos por instituições de pesquisa e avaliados pelo DSA |
| Dados de ocorrências de eventos epidemiológicos relevantes e presença ou ausência de doenças | OIE e organismos internacionais | Sistema OIE-WAHIS e outros | Dados utilizados pelo PNSS, quando necessário, para análises específicas |
¶ 10. COMPONENTES DO SISTEMA DE VIGILÂNCIA
Cada componente do sistema de vigilância compreende uma atividade utilizada para investigar um ou mais perigos na população-alvo. O conjunto dos componentes ou atividades de vigilância capazes de produzir dados sobre a condição da doença em particular, ou sobre a condição de uma população específica, constitui um sistema de vigilância.
Este Plano fundamenta-se nas diretrizes propostas pela OIE e pela Organização das Nações Unidas para a Alimentação e Agricultura (FAO) em vários de seus documentos, notadamente o “Código Sanitário dos Animais Terrestres e o “Manual de Provas de Diagnóstico e Vacinas” da OIE , e o “Manual para Vigilância de Doenças Baseada em Risco”, da FAO.
Levando em consideração as diversidades regionais, o Plano integrado de vigilância para PSC, PSA e PRRS buscou estabelecer um programa com melhor eficácia e custo-benefício, em especial no que diz respeito à existência de riscos diferenciados de ocorrência da doença nas diferentes regiões e nos diversos tipos de produção e regiões do País.
O Plano integrado de vigilância é composto por cinco componentes abaixo listados e ilustrados na Figura 4:
1. vigilância sorológica baseada em risco
2. inspeções em estabelecimentos de criação
3. investigações de casos suspeitos
4. inspeção em abatedouros
5. vigilância sorológica em suínos asselvajados
Tendo em vista a disponibilidade de material científico para fundamentação e a alta previsibilidade e controle do SVO sobre as ações do Plano, foi possível estabelecer o nível esperado de sensibilidade e a probabilidade de ausência das doenças alvo em relação ao componente “Vigilância sorológica baseada em risco”. Para os demais componentes, há carência de elementos que viabilizem uma análise quantitativa prévia e completa de suas contribuições. Apesar disso, é importante ressaltar que a execução satisfatória de todos os componentes, de acordo com o preconizado neste Plano, é essencial para que o sistema de vigilância atinja a sensibilidade esperada e a abrangência mais completa possível da população de suínos.
De acordo com o Código Terrestre “as estratégias de vigilância empregadas para determinar a condição da PSA devem ser adaptadas à situação (...) a abordagem utilizada deve levar em conta a presença de suínos selvagens ou asselvajados, a presença de carrapatos do gênero Ornithodoros, e a presença de PSA em países ou zonas adjacentes”.
Uma vez que a PSA não se encontra presente nas Américas há mais de 30 anos, os componentes “Vigilância sorológica baseada em risco” e “Vigilância sorológica em suínos asselvajados” não incluirão testes direcionados a essa doença na rotina. No entanto, a vigilância de casos suspeitos de síndrome hemorrágica, oriundas de quaisquer componentes, serão testadas tanto para PSC como para PSA, no intuito de promover a detecção precoce de eventual ocorrência de PSA.
A realização de testes para PSA, ou mudanças na estratégia de amostragem, fica na dependência de avaliações quanto às possíveis alterações dos riscos da ocorrência da PSA no Brasil ou região.
¶ 10.1 COMPONENTE 1 – VIGILÂNCIA SOROLÓGICA BASEADA EM RISCO
O desenho amostral deste componente é calculado e otimizado em função do risco para a PSC e as informações abaixo explicam esse processo. Apesar de não ser o objetivo primário do componente, testes sorológicos serão concomitantemente realizados para a PRRS e interpretados à luz dos mesmos métodos de avaliação, fornecendo resultados que alcancem uma sensibilidade satisfatória.
Para fins de caracterização e delineamento do plano amostral, a zona livre de PSC foi dividida em três áreas geográficas (Figura 3). Para cada uma dessas áreas foi elaborado um plano de amostragem em que foram consideradas diferentes probabilidades de ausência prévia de PSC, de acordo com o histórico e avaliações do sistema de vigilância aplicado anteriormente e proximidade com áreas não livres de PSC.
De maneira a calcular as sensibilidades do componente em cada área, foram selecionados grupos de maior risco com base na categoria “tipo de estabelecimento”. Em sequência, foram definidos, para cada área geográfica, os números de estabelecimentos e suínos a serem amostrados, de modo que a sensibilidade do componente da vigilância se mantivesse acima de 95% e que a probabilidade de ausência de PSC na área, caso todas as amostras resultem negativas aos testes diagnósticos, se mantivesse acima de 99%.
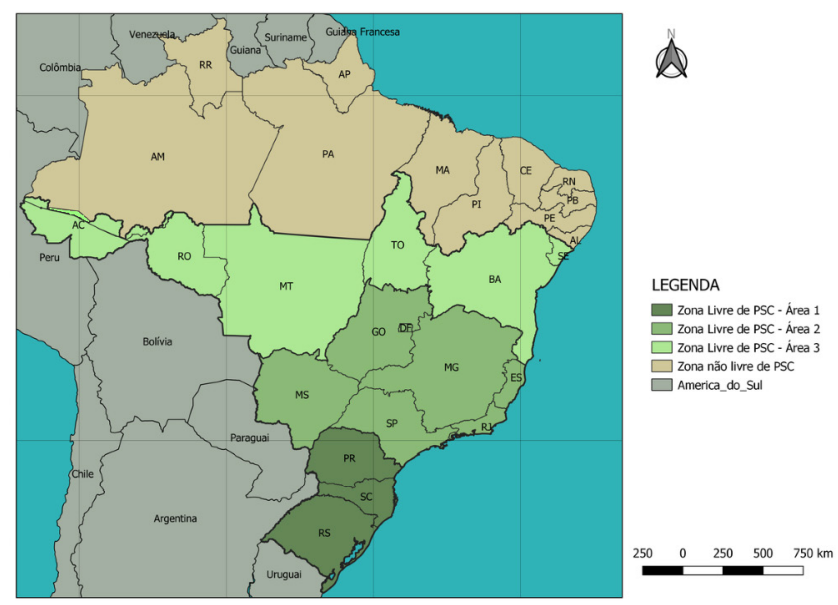
¶ 10.1.1 Probabilidade de ausência das doenças (Áreas 1, 2 e 3)
Áreas Geográficas: diante da ampla diversidade de ecossistemas, sistemas produtivos, realidades sociais e particularidades geográficas que influenciam a aplicação do sistema de vigilância, a área correspondente às zonas livres de PSC foi dividida em três áreas, conforme apresentado na Figura 5, visando adequação às realidades e desafios epidemiológicos.
Para cada uma das três áreas geográficas, o componente de vigilância foi delineado separadamente, aplicando-se diferentes níveis de “Prior”, ou seja, as probabilidades de ausência prévia da doença. Estes diferentes níveis foram estabelecidos de acordo com o histórico e avaliações do sistema de vigilância anteriormente praticado. Quanto mais intensivo e validado o sistema de vigilância anterior, com resultados satisfatórios na população, maior é essa probabilidade considerada.
• Área 1: composta pelos estados da Região Sul (PR, SC e RS), que concentram a maior parte da suinocultura industrial do País, com 50,6% da população suína. Nesta Região predomina a produção tecnificada em sistema de integração. As últimas ocorrências de PSC foram em 1997.
Nesta área, o sistema de vigilância foi primeiramente estruturado e alcançou resultados bastante robustos na avaliação de demonstração de ausência da infecção nos rebanhos suínos (MOTA, A.L.A.A, 2016). Tal condição permite que, de maneira ainda conservadora, seja utilizado o valor de 90% para probabilidade de ausência da PSC.
• Área 2: formada pelas unidades federativas da Região Sudeste e parte da Região Centro-Oeste (SP, MG, ES, RJ, GO, DF e MS), com cerca de 23% da população suína. Nesta região há significativa produção de suínos em sistemas tecnificados de forma integrada, mas predomina a presença de produtores independentes. A proporção de sistemas de produção não tecnificados é maior que na Região I. Nesta Área 2, as últimas ocorrências de PSC foram em 1998. A Área 2 também tem longo histórico de vigilância para PSC com resultados satisfatórios, porém menos robustos e consistentes que os da Área I. Logo, para esta área foi estimada uma probabilidade de ausência de 70%.
• Área 3: formada pelos estados limítrofes com a ZnL de PSC (AC, RO, MT, TO, BA e SE, além dos municípios de Guajará, Boca do Acre, sul do município de Canutama e sudoeste do município de Lábrea, pertencentes ao estado do AM), com 11% da população suína. Nesta Área 3, há presença de sistemas de produção tecnificados, integrados e independentes, assim como maior proporção de sistemas de produção não tecnificados, sejam eles comerciais ou não. As últimas ocorrências de PSC foram em 1995. Nesta Área também há um sistema de vigilância para PSC com muitos anos de atividades e resultados favoráveis, porém com fragilidades em algumas UF.
Para a Área 3 foi estabelecida uma probabilidade de ausência da PSC de 50%, valor utilizado quando se desconhece a situação epidemiológica, essa decisão foi tomada em vista das divisas com as ZnL e à maior proporção de sistemas de produção não tecnificados.
Cabe destacar que estas probabilidades prévias serão reajustadas para valores superiores, de acordo com os resultados da execução dos componentes deste Plano integrado de vigilância. Alcançando-se as metas para os indicadores estabelecidos e não se detectando casos das doenças, estes ajustes serão realizados e implicarão em reduções nos planos amostrais das referidas áreas.
¶ 10.1.2 Risco Atribuído aos Tipos de Estabelecimentos
Os estabelecimentos de criação de suínos tiveram seus riscos categorizados conforme suas características e estão representados na árvore de cenários da Figura 6. Tal categorização considerou a heterogeneidade dos estabelecimentos de criação de suínos e do consequente impacto que as práticas de manejo, sanidade e biosseguridade exercem no risco de introdução ou disseminação de doenças como a PSC.
O risco atribuído a cada tipo de estabelecimento da suinocultura tecnificada foi embasado na “Estimativa de Riscos Relativos para Introdução de PSC” (MOTA, A.L.A.A, 2016), que também seguiu as diretrizes propostas pelo “Manual para Vigilância de Doenças Baseada em Risco”, da FAO. Entre os tipos principais de estabelecimentos, foram selecionados quatro para comporem o sistema de vigilância sorológica.
• Granjas de Reprodutores Suínos Certificada (GRSC): Esse tipo de estabelecimento, apesar de ser a categoria de estabelecimentos com a maior biosseguridade e menor risco de ocorrência de PSC, foi introduzido no componente uma vez que o teste para PSC é um requisito para certificação de qualquer GRSC. Esses estabelecimentos possuem vinculação, direta ou indireta, com toda cadeia de produção e, assim, a garantia da ausência de PSC e PRRS nesse tipo de estabelecimento é de grande relevância para o setor. Dessa forma, o Risco atribuído às GRSC é 1.
• Unidades Produtoras de Leitões (UPL): Este tipo de estabelecimento representa o setor integrado da cadeia de produção e que apresenta a maior concentração de suínos adultos. O Risco atribuído a este tipo de estabelecimento é 3,4.
• Estabelecimentos de ciclo completo (CC): Os estabelecimentos de ciclo completo são identificados como aqueles com maior risco entre as suinoculturas tecnificadas (MOTA, A.L.A.A., 2016). Isso se deve, entre outros fatores, a uma menor adesão às medidas sanitárias e de biosseguridade. O Risco atribuído a este tipo de estabelecimento é 4,5.
Os estabelecimentos dos tipos “Creche” e “Terminação” não foram incluídos na amostragem devido ao menor risco atribuído a essas categorias e, principalmente, à expectativa de se encontrar somente animais jovens. Esses animais possuem menor tempo de possível exposição aos agentes patogênicos, caso estes estejam presentes, e, portanto, menores chances de apresentarem reações imunológicas ou presença dos agentes investigados. Além disso, creches e terminações são alojadas e esvaziadas aproximadamente a cada 45 dias (creches) e 90 dias (terminações), e após cada retirada de animais são realizados manejo de limpeza , desinfecção e vazio sanitário.
Os estabelecimentos de suinocultura não tecnificada de subsistência não foram priorizados para colheita de amostras por serem considerados de menor risco em relação aos de suinocultura não tecnificada de comércio local.
¶ 10.1.3 Amostragem
A vigilância soroepidemiológica tem o objetivo de apoiar a certificação de ausência de transmissão do vírus da PSC e da PRRS. Uma amostragem baseada em risco, cujo alvo são rebanhos e indivíduos com maior probabilidade de serem infectados, é mais apropriada, pois fornece um nível melhor de probabilidade da ausência da doença, ao ser comparada com uma amostra representativa do mesmo tamanho.
O desenho amostral foi definido no intuito de maximizar a probabilidade de detecção de PSC. Por esse motivo, seleciona estabelecimentos dentre os 4 tipos escolhidos, refletindo a distribuição nas 3 áreas e estados. Conforme descrito anteriormente, apesar do modelo ser baseado nas características da PSC, as amostragens também serão satisfatórias para a comprovação da ausência de PRRS e, caso seja necessário, também para a PSA.
Foram considerados, como parâmetros epidemiológicos, a prevalência mínima de estabelecimentos infectados de 1%, a prevalência em animais dentro de um rebanho infectado de 15%, a sensibilidade dos testes sorológicos (ELISA) de 94,4% e para a PCR de 99,0%. A especificidade do sistema diagnóstico é tratada como 100%, considerando as investigações complementares clínica, laboratorial e epidemiológica visando a confirmação de casos pelo SVO. O número de amostras foi calculado de modo a satisfazer uma sensibilidade mínima para o sistema de vigilância de 99% e probabilidade de ausência de PSC de 95%.
As GRSC seguirão a legislação vigente para certificação com definição da amostragem a ser procedida. Quanto à temporalidade do Plano Integrado de Vigilância, as amostragens em suinocultura tecnificada e não tecnificada de comércio local devem ser distribuídas em todos os meses do ano, podendo sofrer variações, conforme indicadores da Tabela 9 (Componentes para avaliação representatividade Temporal), mas não se concentrando em poucos meses, de forma a garantir a representatividade temporal dos componentes.
¶ 10.1.4 Caracterização dos estabelecimentos amostrados
A relação dos municípios e estabelecimentos a serem amostrados será elaborada anualmente pelo DSA, em conjunto com o OESA de cada UF. No entanto, ao avaliar o estabelecimento selecionado, o técnico do OESA responsável pela colheita deverá certificar que este possui as características necessárias para se enquadrar na categoria “tipo de produção” que lhe foi atribuída, conforme descrito no Item 8 deste Plano e na Tabela 1 do Anexo I.
As UF que desenvolverem estudos para identificação de áreas ou de propriedades de maior risco poderão agregar estas informações para subsidiar a seleção das propriedades a serem amostradas.
¶ 10.2 COMPONENTE 2 – INSPEÇÕES EM ESTABELECIMENTOS DE CRIAÇÃO
Neste componente, as inspeções clínica e de índices zootécnicos devem ser direcionadas a outros estabelecimentos em que não houver sido realizada a vigilância sorológica, com presença de fatores de risco para a introdução, manutenção ou disseminação do vírus da PSC, PSA e PRRS. O protocolo de atividades e informações a serem checadas nas inspeções em estabelecimentos e a lista de fatores de risco a serem considerados estão disponíveis no Anexo II.
A vigilância de inspeções em estabelecimentos de criação de maior risco é de grande importância, pois propicia a atualização de informações do estabelecimento e dos rebanhos suínos, além da interação do SVO com os responsáveis pelo manejo dos suínos para o desenvolvimento de ações de educação em saúde animal.
Complementarmente, e de forma não dirigida, outras inspeções e fiscalizações do SVO em estabelecimentos com suínos, com distintos propósitos, podem ser consideradas na produção de dados e informações sobre a vigilância da doença. Novamente, as UF que desenvolverem estudos para identificação de áreas ou de propriedades de maior risco poderão agregar estas informações para subsidiar a seleção das propriedades a serem inspecionadas. Esses estudos poderão ser realizados por cada UF em parceria com instituições de ensino e pesquisa e validados pelo DSA.
Quanto à temporalidade, as inspeções devem ser distribuídas em todos os meses do ano, podendo sofrer variações, conforme indicadores da Tabela 6 (Indicadores para avaliação da representatividade Temporal), mas não se concentrando em poucos meses, de forma a garantir a representatividade temporal dos componentes.
¶ 10.2.1. Amostragem
Para fins de caracterização e delineamento do plano amostral, a zona livre de PSC foi dividida em três áreas geográficas (áreas 1, 2 e 3), de acordo com os critérios adotados no componente 1, de probabilidades de ausência da infecção pelo vírus da PSC.
A amostragem para detecção de PSC foi calculada objetivando-se ter confiança superior a 95% de que a PSC não estaria presente nas granjas e uma prevalência entre rebanhos superior a 1% e intra-rebanhos superior a 15%, tomando-se que 1% dos animais estariam apresentando sintomas no momento da inspeção, e que a “sensibilidade diagnóstica” – no caso a capacidade do veterinário detectar os sinais clínicos ao realizar uma inspeção de rebanho – seria de 15%. Da mesma forma que no “Componente 1 - Vigilância Sorológica Baseada em Risco”, foram incorporados no desenho amostral os riscos relativos para PSC por tipo de suinocultura ( UPL - 3,4; Ciclo completo - 4,5; Não Tecnificada - 7,0), e as probabilidades de ausência de PSC prévias (Área 1 - 90%; Área 2 - 70%; Área 3 - 50%). Esses parâmetros foram descritos mais extensivamente no componente 1.
O desenho amostral baseado em risco foi definido no intuito de maximizar a probabilidade de detecção de sinais clínicos de PSC, na zona livre de PSC, e selecionar estabelecimentos pertencentes aos tipos UPL, ciclo completo e suinoculturas não tecnificadas, refletindo a distribuição nas três áreas de amostragem e unidades federativas.
Os médicos veterinários ou agentes de fiscalização do serviço oficial devem executar a inspeção do rebanho como um todo (inspeção visual), procedendo ao exame individual (inspeção clínica) de animais que julguem se destacar clinicamente dos demais, registrando o total de inspecionados visualmente e inspecionados clinicamente no formulário eletrônico.
A relação dos municípios com os estabelecimentos, tecnificados e não tecnificados, a serem amostrados será indicada pelo DSA, com base em dados de cadastros enviados por cada OESA. No entanto, ao selecionar o estabelecimento, o técnico do OESA deve se certificar de que este possui as características necessárias para se enquadrar na categoria “tipo de estabelecimento” que foi indicada pelo DSA, conforme descrito no Item 8 deste Plano e na Tabela 1 do Anexo I, e que possui pelo menos um dos fatores de risco listados no Anexo II deste Plano Integrado.
¶ 10.3 COMPONENTE 3 – INVESTIGAÇÕES DE CASOS SUSPEITOS
A investigação de casos suspeitos, em suínos domésticos ou asselvajados, é a forma mais comum e a mais importante do sistema de vigilância. A notificação por parte dos criadores, demais profissionais da cadeia suinícola e agentes de manejo populacional de suínos asselvajados devidamente instruídos e sensibilizados acerca dos sinais das doenças é fundamental para detecção precoce de focos.
Os procedimentos padronizados pelo DSA, tanto o fluxo de notificações e registros de informações zoossanitárias, quanto procedimentos técnicos para os atendimentos de casos suspeitos e diagnósticos laboratoriais de PSC, PSA e PRRS estão disponíveis no “Manual do Sistema Nacional de Informações Zoossanitárias – SIZ” e no “Manual de investigação de doenças dos suínos”.
No caso de a notificação de suspeita ser considerada caso provável de PSC, PSA ou PRRS por um médico veterinário oficial (MVO), deve-se proceder à interdição imediata do estabelecimento e registro no e-Sisbravet. A investigação clínica e epidemiológica de casos prováveis deve ser complementada com testes laboratoriais executados pelo LFDA para a confirmação ou descarte dos casos, conforme apresentado nas fichas técnicas das doenças. Quando da ocorrência de casos prováveis ou confirmados em suínos asselvajados, não haverá interdição do estabelecimento.
Em situações em que ocorra a confirmação de casos de PSC, PSA ou PRRS, as ações deverão seguir o estabelecido nos respectivos planos de contingência.
¶ 10.3.1 O papel das instituições de ensino ou pesquisa e laboratórios privados de diagnóstico
Assume especial importância para a detecção precoce de focos, a inserção das instituições de ensino ou pesquisa e dos laboratórios de diagnóstico privados, no sistema de notificação ao SVO. Estes laboratórios, profissionais da área e professores de universidades são rotineiramente acionados pelos produtores e veterinários responsáveis pelos estabelecimentos de criação para produção de vacinas autógenas e diagnósticos de outros problemas sanitários, que não as doenças de controle oficial.
Em caso de ocorrência de uma das doenças deste Plano em estabelecimentos tecnificados pode ocorrer que, equivocadamente, estes laboratórios recebam amostras não oficiais de casos prováveis, antes mesmo da notificação ao SVO. Uma vez que as amostras provêm de suínos que apresentam sinais clínicos, podendo incluir casos de PSC, PSA ou PRRS, estas representam um alto valor de vigilância para a detecção precoce. Portanto, em condições que caracterizem casos suspeitos dessas doenças, estes laboratórios devem notificar imediatamente ao serviço oficial de saúde animal para investigações e diagnósticos diferenciais.
O SVO de cada unidade federativa deve manter atualizados os contatos dos laboratórios de diagnóstico, privados e de universidades, e realizar visitas periódicas para intercâmbio de informações, sensibilização, esclarecimentos quanto às obrigações em relação à notificação de doenças e disponibilização dos contatos para a imediata notificação de casos suspeitos.
¶ 10.4 COMPONENTE 4 – INSPEÇÃO EM ABATEDOUROS
Os objetivos da inspeção em estabelecimentos de abate são direcionados principalmente para a saúde pública, como garantir a segurança, a inocuidade e a qualidade higiênico-sanitária dos produtos de origem animal, além de mitigar os riscos de transmissão de doenças ou contaminação por resíduos. A representatividade dos dados de abate possui limitações e tem grande viés de amostragem, o que limita a interpretação dos dados produzidos para ações em saúde animal, destacando que:
- Os suínos enviados para abate em estabelecimentos sob inspeção oficial são considerados uma amostragem tendenciosa por diversos motivos, desde comerciais e geográficos, até epidemiológicos, sanitários e sazonais, não sendo representativa da população geral.
- Os suínos enviados para abate tendem a ser mais jovens e mais saudáveis que o resto da população, exclui ou sub-representa animais muito jovens, mal desenvolvidos ou com alguma doença.
- As doenças que causam alta mortalidade são subestimadas nos abatedouros, já que os animais nem chegam a ser abatidos.
- Ocorre no final da cadeia, portanto, é uma detecção tardia dentro do sistema de vigilância.
Assim, os dados de abates têm limitada validade para avaliação de doenças que apresentem lesões de difícil detecção ou cuja ocorrência reduza a probabilidade de envio de animais para o abate, mas os grandes volumes de animais envolvidos e a padronização dos procedimentos de inspeção animal ante e post mortem para a detecção precoce de casos suspeitos das doenças alvo oferecem uma contrapartida, tornando este componente relevante para o sistema de vigilância.
As inspeções realizadas na rotina podem detectar a presença de sinais clínicos e lesões patológicas e direcionar ações de vigilância nos estabelecimentos de origem dos suínos.
A vigilância em estabelecimentos de abate é comumente interpretada como uma forma de vigilância ativa. As principais vantagens são: a) baixo custo, haja vista que os suínos já são inspecionados para outras finalidades; b) grande número de suínos inspecionados; c) fornecimento constante de dados; d) permite a coleta de dados e materiais, em poucos abatedouros, de um grande número de estabelecimentos rurais de origem dos suínos e com método padronizado para detectar sinais clínicos e patológicos, sendo em geral mais específica que as observações dos proprietários; e e) é uma forma de monitorar os demais componentes do sistema de vigilância, pois caso existam falhas de detecção em nível de campo, nessa última fase é possível fazer a detecção de casos prováveis da doença.
Em caso de detecção de lesões compatíveis com PSC, PSA e PRRS o serviço de inspeção oficial deve comunicar o serviço de saúde animal para realizar a investigação clínica e epidemiológica.
¶ 10.5 COMPONENTE 5 – VIGILÂNCIA SOROLÓGICA EM SUÍNOS ASSELVAJADOS
São considerados neste componente do sistema de vigilância o porco doméstico ou o javali (Sus scrofa) em todas as suas formas, linhagens, raças e seus diferentes graus de cruzamento, vivendo em vida livre na condição selvagem, sem supervisão e controle humano.
O SVO deverá dispor de dados atualizados das populações e habitat dos suínos asselvajados que podem ser obtidos de fontes oficiais, como o Sistema de Informação de Manejo de Fauna (SIMAF/IBAMA), mapas de percepção do SVO, eventualmente complementados com outras fontes governamentais e não governamentais ligadas ao meio ambiente e vida selvagem, institutos de pesquisa da vida selvagem, clubes de caça e afins. A vigilância sorológica em suínos asselvajados tem função complementar para a validação da condição de ausência das doenças que constam neste Plano na população suína.
A coleta de dados sobre os suínos asselvajados e sua correlação com as populações domésticas é de suma importância para que se possam tomar ações do SVO no sentido de evitar o ingresso da PSC, PSA e PRRS e a resposta rápida em caso de introdução. Os suínos asselvajados têm importância epidemiológica na manutenção da PSC, PSA e PRRS como reservatório para o vírus e possíveis fontes de infecção para os suínos de criação doméstica.
A vigilância sorológica na população de suínos asselvajados será realizada mediante parceria entre Agentes de Manejo Populacional autorizados e o SVO, conforme procedimentos descritos no Anexo III.
¶ 11 DIAGNÓSTICO LABORATORIAL
¶ 11.1 DIAGNÓSTICOS DAS INVESTIGAÇÕES DE CASOS PROVÁVEIS
Para os casos prováveis de PSC, PSA e PRRS, deve-se proceder conforme o preconizado em suas respectivas fichas técnicas.
A realização de testes diagnósticos em amostras oriundas de casos prováveis de PSC, PSA e PRRS é autorizada somente em laboratórios oficiais do MAPA - os Laboratórios Federais de Defesa Agropecuária (LFDAs).
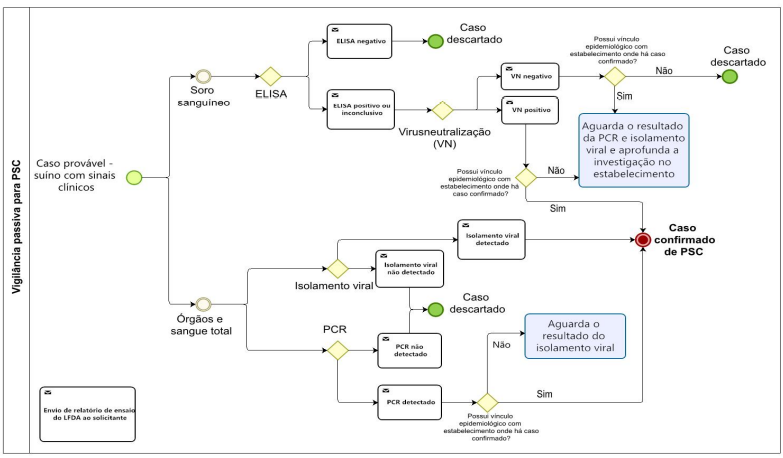
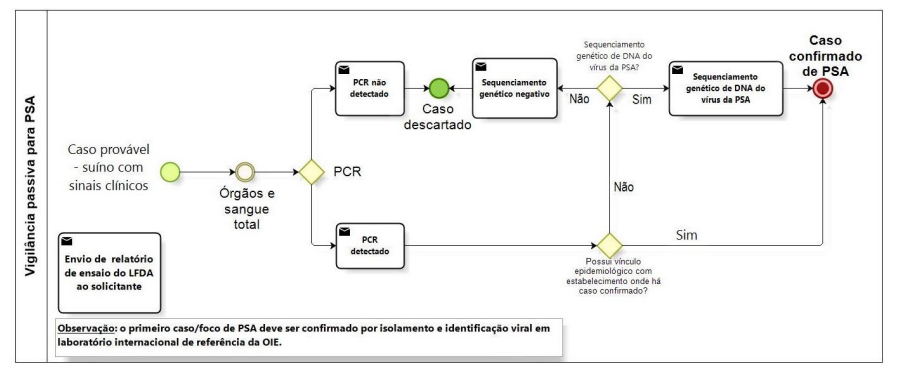
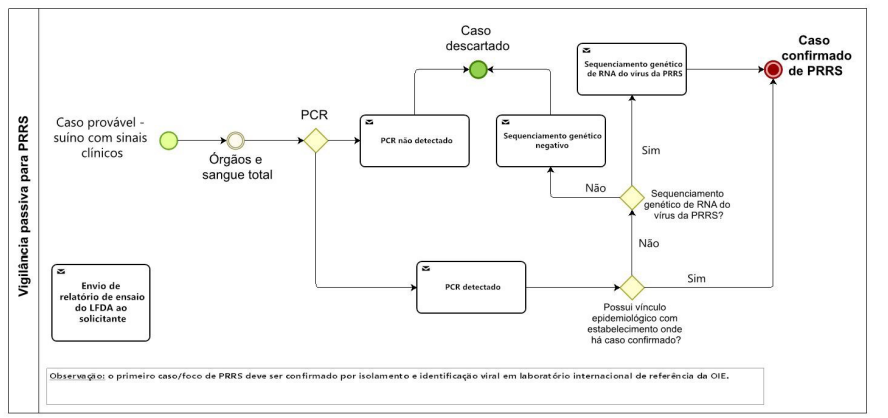
¶ 11.2 DIAGNÓSTICOS DA VIGILÂNCIA SOROLÓGICA
Para realização dos testes da vigilância sorológica para PSC, PSA e PRRS é utilizada a rede de Laboratórios Públicos e credenciados pelo MAPA, com seu credenciamento ativo para o escopo e nos demais laboratórios que vierem a ser credenciados para esta finalidade:
• Centro de Diagnóstico de Sanidade Animal - CEDISA, Santa Catarina;
• Centro de Diagnóstico Marcos Enrietti - CDME, Paraná;
• Instituto Biológico - IB, São Paulo;
• Instituto Mineiro de Agropecuária - IMA, Minas Gerais;
• Instituto de Pesquisas Veterinárias Desidério Finamor - IPVDF, Rio Grande do Sul; e
• Laboratório de Análise e Diagnóstico Veterinário – LABVET, Goiás.
Caso haja alguma amostra inconclusiva ou positiva nos testes de triagem, as investigações complementares continuam e os testes confirmatórios são realizados nos LFDAs de referência.
O fluxo simplificado e os testes laboratoriais da vigilância ativa podem ser visualizados nas figuras abaixo.
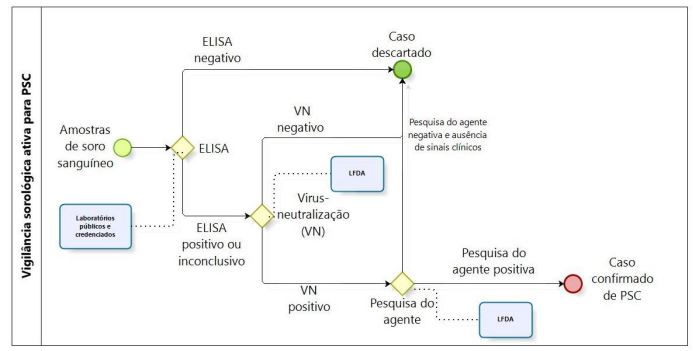
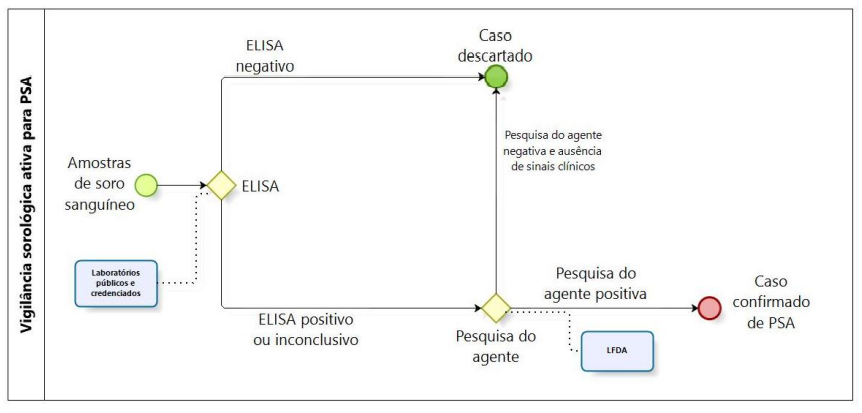
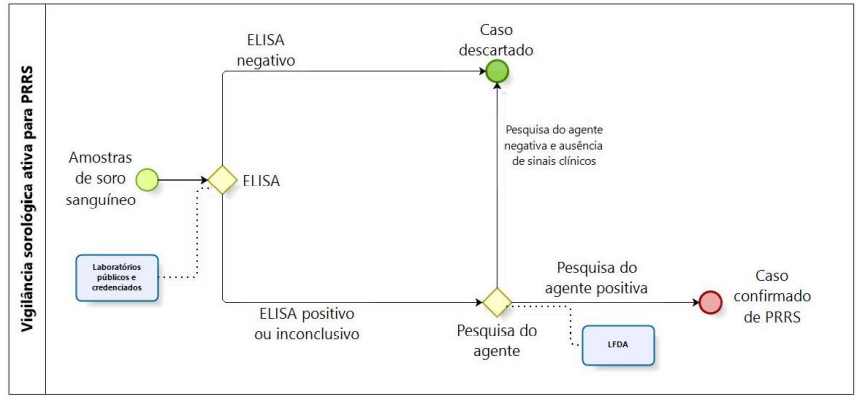
Tabela 3. Responsáveis, tipos de amostras, laboratórios, sistemas de registro das atividades de vigilância e periodicidade de inserção dos dados.
| Tipo de Amostragem | Responsável pela colheita | Tipo de amostra | Laboratório | Sistema de colheita de dados | Inserção de dados |
|---|---|---|---|---|---|
| Investigações de casos suspeitos/ prováveis | OESA | Sangue total, soro e órgãos de eleição | LFDA/MG LFDA/PE | e-Sisbravet | Imediato e contínuo |
| Vig. sorológica em estabelecimentos tecnificados e não tecnificados | OESA | Soro sanguíneo | IMA/MG IB/SP CDME/PRCEDISA/SC IPVDF/RS LABVET/GO | SIGEP (estudo sui_doméstico) | Contínuo, conforme andamento das atividades |
| Vig. sorológica em suínos asselvajados | Manejadores | Soro sanguíneo | IMA/MG IB/SP CDME/PRCEDISA/SC IPVDF/RS LABVET/GO | SIGEP (estudo sui_asselvajado) | Contínuo, conforme andamento das atividades |
¶ 12 DESEMPENHO DO SISTEMA DE VIGILÂNCIA: PLANEJAMENTO DA ANÁLISE E AVALIAÇÃO
O Plano integrado de vigilância de doenças de suínos deve incluir indicadores e metas objetivas que permitam a avaliação do desempenho do sistema, visando adequado monitoramento e correções de desvios e deficiências.
As avaliações dos indicadores de desempenho do Plano de vigilância deverão fazer parte da compilação e análise dos resultados obtidos em cada um dos componentes e será efetuado pela coordenação do PNSS, com o apoio dos pontos focais nas SFAs e OESAs em cada unidade federativa. Deverão ser inseridos nos Relatórios Semestrais para cada unidade federativa envolvida, visando avaliar o cumprimento das metas de vigilância, os quais devem ser encaminhados ao Departamento de Saúde Animal. Esses dados serão compilados pelo DSA e subsidiarão a formulação do relatório anual, conforme descrito no item 15.
Para o presente plano foram propostos indicadores para avaliação dos seguintes aspectos de performance, descritos nas tabelas a seguir:
• representatividade geográfica;
• representatividade dos tipos de produção/faixa etária;
• representatividade temporal;
• consistência dos resultados com as definições de caso;
• oportunidade da vigilância.
Tabela 4. Indicadores para avaliação da representatividade geográfica
| Componente | Características avaliadas | Indicador | Meta |
|---|---|---|---|
| Investigações de casos suspeitos | A distribuição geográfica das notificações de suspeitas e dos atendimentos a casos prováveis deve refletir a distribuição da população de suínos | NA | NA |
| Vig. sorológica em Suinocultura Tecnificada | A distribuição geográfica da amostragem deve aproximar da distribuição das unidades de produção tecnificadas de suínos. | % de estabelecimentos selecionados com realização de colheita | 95% |
| Vig. sorológica em Suinocultura Não Tecnificada | A distribuição geográfica da amostragem na Suinocultura Não Tecnificada deve ser em toda zona livre de PSC, priorizando os municípios em áreas de maior risco. | % de municípios selecionados que cumpriram a amostragem | 95% |
| Vig. sorológica em GRSC | A amostragem envolverá todas as GRSC | % de GRSC com realização de colheita | 100% |
| Vig. sorológica em suínosasselvajados | A distribuição geográfica das amostras de suínos asselvajados deve refletir a população estimada de suínos asselvajados e em compatibilidade com o quantitativo de Agentes de manejo populacional capacitados e ativos pelo SVO para colaboração na vigilância. Os dados de municípios com atividade de manejo populacional devem ser obtidos no SIMAF. | municípios com colheita de amostras / municípios com manejo populacional de suínos asselvajados | 70% |
| Inspeções em estabelecimentos de criação (tecnificada e não tecnificada) | A distribuição geográfica das inspeções deve aproximar da distribuição dos municípios com suínos não tecnificados ou áreas classificadas como de maior risco. | % de municípios selecionados que cumpriram a amostragem | 95% |
| Inspeção em abatedouros |
A distribuição geográfica dos municípios, com estabelecimentos de criação de suínos, que enviaram animais para abatedurante o ano. |
% dos municípios com suinocultura tecnificada que enviaram suínos para abate | 80% |
Tabela 5. Indicadores para avaliação da representatividade por tipos de produção/faixa etária
| Componente | Características avaliadas | Indicador | Meta |
|---|---|---|---|
| Investigações de casos suspeitos | A distribuição das notificações de suspeitas e dos atendimentos a casos prováveis deve refletir os tipos de produção existentes na respectiva Área devigilância. | NA | NA |
| Vig. sorológica em Suinocultura Tecnificada | O número de estabelecimentos amostrados em cadaUF deve refletir a proporção de estabelecimentos por tipo de produção na respectiva Área de vigilância. A distribuição das amostras colhidas deve aproximar da distribuição dos diferentes tipos de estabelecimentos tecnificados, priorizando aqueles considerados de maior risco. |
Nº de estab. amostrados / Nº de estab. selecionados % de amostras colhidas de suínos adultos |
95%
100% |
| Vig. sorológica em Suinocultura Não Tecnificada | A amostragem deve ser feita em suínos adultos, com maior probabilidade de apresentar anticorpos contra as doenças. | % de amostras colhidas de suínos adultos | 100% |
| Vig. sorológica em GRSC | Todas as GRSC devemser amostradas, priorizando a amostragem em suínos adultos.Naquelas tipo sítioII e sítio III devem ser contempladas, ainda que não possuam suínos acima de 8 meses. | % de GRSC amostradas | 100% |
| Vig. sorológica em suínosasselvajados | Espera-se que a amostragem seja prioritariamente de suínos adultos, com maior probabilidade de apresentar anticorpos contra as doenças. O tipo de produção não se aplica a este componente. | % de amostras colhidas de suínos adultos | 90% |
| Inspeções em estabelecimentos de criação (tecnificada e não tecnificada) | Os estabelecimentos amostrados em cadamunicípio devem possuirpelo menos um dos critérios de risco elencados no Anexo II. | % de estabelecimentos inspecionados que possuem critérios de risco | 80% |
| Inspeção em abatedouros | O número de estabelecimentos com suínos inspecionados em cada UF deve aproximar do total de estabelecimentos tecnificados existentes. | NA | NA |
Tabela 6. Indicadores para avaliação representatividade Temporal
| Componente | Características avaliadas | Indicador | Meta |
|---|---|---|---|
| Investigações de casos suspeitos | A distribuição das notificações de suspeitas e dos atendimentos a casos prováveis deve refletir os tipos de produção existentes na respectiva Área de vigilância. | NA | NA |
| Vig. sorológica em Suinocultura Tecnificada | O número de estabelecimentos amostrados em cadaUF deve refletir a proporção de estabelecimentos por tipo de produção na respectiva Área de vigilância. A distribuição das amostras colhidas deve aproximar da distribuição dos diferentes tipos de estabelecimentos tecnificados, priorizando aqueles considerados de maior risco. |
Nº de estab. amostrados / Nº de estab. selecionados % de amostras colhidasde suínos adultos |
95%
100% |
| Vig. sorológica em Suinocultura Não Tecnificada | A amostragem deve ser feita em suínos adultos, com maior probabilidade de apresentar anticorpos contra as doenças. | % de amostras colhidas de suínos adultos | 100% |
| Vig. sorológica em GRSC | Todas as GRSC devemser amostradas, priorizando a amostragem em suínos adultos.Naquelas tipo sítioII e sítio III devem ser contempladas, ainda que não possuam suínos acima de 8 meses. | % de GRSC amostradas | 100% |
| Vig. sorológica em suínos asselvajados | Espera-se que a amostragem seja prioritariamente de suínos adultos, com maior probabilidade de apresentar anticorpos contra as doenças. O tipo de produção não se aplica a este componente. | % de amostras colhidasde suínos adultos | 90% |
| Inspeções em estabelecimentos de criação (tecnificada e não tecnificada) | Os estabelecimentos amostrados em cadamunicípio devem possuirpelo menos um dos critérios de risco elencados no Anexo II. | % de estabelecimentos inspecionados que possuem critérios de risco | 80% |
| Inspeção em abatedouros | O número de estabelecimentos com suínos inspecionados em cada UF deve aproximar do total de estabelecimentos tecnificados existentes. | NA | NA |
Tabela 7. Indicadores para avaliação da oportunidade do plano de vigilância
| Componente | Característica | Indicador | Meta |
|---|---|---|---|
| Investigações de casos suspeitos |
Os atendimentos às notificações de suspeitas devem ser realizados em até 12 horas após o recebimento. As amostras colhidas de casos prováveis devem chegar o mais rápido possível ao LFDA, não ultrapassando as 48 horas após a colheita. Ao chegar ao laboratório, as amostras devem ser processadas com urgência e os resultados dos testes laboratoriais devem ser disponibilizados em até 24hapós o recebimento. |
1.Tempo de reação; 2.Tempoentre a colheita e a chegada ao LFDA; 3.Tempo entre o recebimento da amostra e o resultado 4. Tempo para registro de atendimentos no e-Sisbravet |
1. 12h 2. 48h 3. 24h 4. 24h |
| Vig. sorológica em Suinocultura Tecnificada |
As amostras colhidas da vigilância sorológica devem ser enviadaso mais rápido possível ao laboratório oficial credenciado, não ultrapassando os 15 (quinze) diasapós a colheita. Ao chegar ao laboratório, as amostras devem ser processadas com brevidade, dentro de 7 (sete) dias após o recebimento e os resultados dos testes laboratoriais devem ser disponibilizados rapidamente após obtidos. Amostras positivas nos testesde triagem devemser enviadas ao LFDA em até 72h após os resultados no lab. Credenciado |
1. Tempo entre a colheita e o envio das amostras; 2. Tempo entre o recebimento no lab. e o resultado 3. Tempo entre o resultado positivo do teste de triagem e o envio da amostra ao LFDA |
1. 15 dias 2. 7 dias 3. 3 dias |
| Vig. sorológica em Suinocultura Não Tecnificada |
As amostras colhidas da vigilância sorológica devem ser enviadaso mais rápido possível ao laboratório oficial credenciado, não ultrapassando os 10 (dez) diasapós a colheita. Ao chegar ao laboratório, as amostras devem ser processadas com brevidade, dentro de 7 (sete) dias após o recebimento e os resultados dos testes laboratoriais devem ser disponibilizados rapidamente após obtidos. Amostras positivas nos testesde triagem devemser enviadas ao LFDA em até 72h após os resultados no lab. credenciado |
1. Tempo entre a colheita e o envio das amostras; 2. Tempo entre o recebimento no lab. e o resultado 3. Tempo entre o resultado positivo do teste de triagem e o Tempo entre o resultado positivo do teste de triagem e o envio da amostra ao LFDA |
1. 15 dias 2. 7 dias 3. 3 dias |
| Vig. sorológica em GRSC |
As amostras colhidas da vigilância sorológica devem ser enviadas o mais rápido possível ao laboratório oficial credenciado, não ultrapassando as 15 (quinze) dias após a colheita. Ao chegar ao laboratório, as amostras devem ser processadas com brevidade, dentro de 7 (sete) dias após o recebimento e os resultados dos testes laboratoriais devem ser disponibilizados rapidamente após obtidos. Amostras positivas nos testes de triagem devem ser enviadas ao LFDA em até 72h após os resultados no lab. credenciado |
1. Tempo entre a colheita e o envio das amostras; 2. Tempo entre o recebimento no lab. e o resultado 3. Tempo entre o resultado positivo do teste de triagem e o envio da amostra ao LFDA |
1. 15 dias 2. 7 dias 3. 3 dias |
| Inspeções em estabelecimentos (tecnificada e não tecnificada) |
Os procedimentos de levantamento de informações sobre os estabelecimentos e os critérios para identificação de casos prováveis devem seguir ao disposto no protocolo de inspeção e nas fichas técnicas. As atividades de inspeção em estabelecimentos deverãoser registradas no SIGEP em até 7 (sete) dias após a realização. Quando da detecção de casos prováveis de doenças, os registros relacionados à investigação devem se registrados no e-Sisbravet |
1. % de inspeções dentro dos padrões estabelecidos 2. Registros de inspeções lançados no SIGEP em até 7 dias após a realização da atividade 3. Registros de casos prováveis lançados no e-Sisbravet em até 24h |
1. 80% 2. 100% 3. 100% |
| Vig. sorológica em suínosasselvajados |
As amostras colhidas da vigilância em suínos asselvajados devem ser entregues pelos Agentes de manejo populacional com urgência ao OESA e enviadas o mais rápido possível ao laboratório oficial credenciado, não ultrapassando as 15 (quinze) dias após o recebimento. Ao chegar ao laboratório, as amostras devem ser processadas com brevidade, dentro de 7 (sete) dias após o recebimento e os resultados dos testes laboratoriais devem ser disponibilizados rapidamente após obtidos. Amostras positivas nos testes de triagem devem ser enviadas ao LFDA em até 72h após os resultados no lab. credenciado |
1. Tempo entre a colheita de amostra e a entrega ao OESA; 2. Tempo entre o recebimento das amostras pelo OESA e o envio ao lab. 3. Tempo entre o recebimento no lab. e o resultado 4. Tempo entre o resultado positivo do teste de triagem e o envio da amostra ao LFDA |
1. 10 dias 2. 15 dias 3. 7 dias 4. 3 dias |
¶ 13 SENSIBILIDADE ALCANÇADA PELOS COMPONENTES DO SISTEMA DE VIGILÂNCIA
A sensibilidade de cada componente do sistema de vigilância será calculada ao final do período de 12 meses desde a instituição do plano. A realização das atividades preconizadas como a investigação de casos suspeitos e o cumprimento das amostragens planejadas são os fatores determinantes para que a sensibilidade atinja os níveis satisfatórios. Os cálculos serão realizados de maneira independente para cada uma das três áreas definidas, e a contribuição relativa de cada estado será avaliada.
¶ 14 SISTEMAS DE NOTIFICAÇÃO E REGISTROS
Todos os atendimentos realizados dentro do “componente 3 – Investigações de casos suspeitos” deverão ser registrados no e-Sisbravet, que tem por objetivo registrar, consolidar e compartilhar os dados de atendimentos às notificações e ocorrências zoossanitárias realizados pelas instâncias local, intermediária e superior.
Para o registro de notificação pela internet, por qualquer tipo de usuário, foi criado o endereço web de acesso ao e-Sisbravet www.gov.br/agricultura/pt-br/notificacao. Todas as notificações registradas serão direcionadas à UVL responsável pelo município onde esteja localizada a propriedade com caso suspeito.
Todas as atividades realizadas para o cumprimento do “componente 1 - Vigilância sorológica baseada em risco”, do “componente 2 – Inspeções em estabelecimentos de criação” e do componente 5 - Vigilância sorológica em suínos asselvajados deverão ser registradas no Sistema informatizado do DSA, do MAPA, que tem por objetivo registrar, consolidar e compartilhar os dados de estudos epidemiológicos e outras atividades da vigilância ativa.
Para o componente 4 - Inspeção em abatedouros, os registros de inspeção federal serão colhidos do SIGSIF. Quanto aos estabelecimentos sob inspeção estadual e municipal, os OESAs devem buscar integração para obtenção das informações. Quando houver notificação e atendimento a casos suspeitos, as informações devem ser registradas no e-Sisbravet
¶ 15 COMUNICAÇÃO DE RESULTADOS: TRANSPARÊNCIA DO PROCESSO
A compilação e análise dos resultados obtidos em cada um dos componentes deste Plano será efetuado pela coordenação do PNSS, com o apoio dos pontos focais nas SFAs e OESAs em cada unidade federativa. Deverão ser elaborados Relatórios Semestrais para cada unidade federativa envolvida, visando avaliar o cumprimento das metas de vigilância, os quais devem ser encaminhados ao Departamento de Saúde Animal. Esses dados serão compilados pelo DSA e subsidiarão a formulação do relatório anual das ações de vigilância integrada para PSC, PSA e PRRS.
As partes interessadas deverão receber relatórios ou informes com análises e ações executadas a partir dos dados inseridos no Plano integrado de vigilância, sendo de suma importância que cheguem até o nível local, permeando por todos os elos deste sistema. O DSA/MAPA disponibilizará os relatórios no Sistema Eletrônico de Informações (SEI) às SFA e aos OESA, além de disponibilizar na página eletrônica.
A retroalimentação da informação demonstra a transparência do sistema e mantém a cadeia de comunicação ativa entre as partes interessadas, informando adequadamente e estimulando a cooperação, pela percepção da importância de sua contribuição ao sistema. Dessa forma, garante a sua inserção efetiva e a qualidade dos dados obtidos.
¶ 16 RECURSOS E FINANCIAMENTO DO PLANO
O Plano integrado de vigilância de doenças dos suínos deve ser financiado de forma compartilhada por diferentes atores envolvidos e interessados na promoção da saúde animal e nos benefícios do desenvolvimento do sistema de produção de suínos.
Há que se estabelecer um acordo de cooperação entre as partes envolvidas na cadeia da suinocultura das atuais zonas livres de PSC do País de forma que o financiamento seja garantido, com complementação dos setores privados ou pelo MAPA, para sustentar os custos de cada componente do sistema de vigilância em todas as UF envolvidas.
Os custos envolvem os recursos humanos, físicos e financeiros, públicos e privados, essenciais para o sucesso de cada um dos componentes do Plano.
Em cada UF, os atores envolvidos devem organizar reuniões para definição da distribuição dos custos do sistema de vigilância e avaliações da aplicação dos recursos e da execução das atividades previstas.
A tabela 8 ilustra um exemplo de distribuição dos custos entre os principais atores envolvidos, porém, conforme expressado anteriormente, o arranjo a ser estabelecido entre os atores públicos e privados, deve ser construído observando a organização da cadeia produtiva em cada UF.
É importante destacar que o sistema de vigilância apresentado visa a detecção precoce das doenças, mitigando os impactos econômicos e sociais de eventuais ocorrências, e gerar segurança à manutenção e abertura de novos mercados aos suínos e produtos suinícolas do Brasil.
Dessa forma, percebe-se que os custos do sistema de vigilância são muito inferiores aos benefícios gerados à cadeia produtiva, sendo, portanto, essencial o financiamento compartilhado entre os setores público e privado na aplicação de recursos humanos, físicos e financeiros. Ainda assim, futuras análises de custo- benefício do Plano de vigilância integrada de doenças de suínos devem ser realizadas visando prestar contas à sociedade interessada e aperfeiçoar o uso de recursos na sua execução.
Tabela 8. Proposta de modelo de distribuição dos custos em recursos humanos, físicos e financeiros do Plano integrado de vigilância de doenças de suínos, entre os atores envolvidos.
| Componente | Atividade de campo e colheita de amostras | Envio de amostras | Realização de testes laboratoriais | Sistemas, análises e relatórios | ||||
|---|---|---|---|---|---|---|---|---|
| Humanos | Materiais | Financeiros | Humanos | Materiais | Financeiros | |||
| Investigações de casos prováveis1 | OESA | OESA | OESA | Fundos/ associações | LFDA/MAPA | LFDA/MAPA | LFDA/MAPA | DSA/ MAPA |
| Vig. sorológica em Suinocultura Tecnificada | OESA | OESA | OESA | Fundos/ associações |
Lab. credenciado
LFDA/MAPA2 |
Lab. credenciado
LFDA/MAPA2 |
Lab. credenciado
LFDA/MAPA2 |
DSA/ MAPA |
| Vig. soro- lógica em Suinocultura Não Tecnificada | OESA | OESA | OESA | Fundos/ associações |
Lab. credenciado
LFDA/MAPA2 |
Lab. credenciado
LFDA/MAPA2 |
Lab. credenciado
LFDA/MAPA2 |
DSA/ MAPA |
| Vig. sorológica em GRSC | OESA | GRSC | GRSC | GRSC | Lab. credenciado | Lab. credenciado | GRSC | DSA/ MAPA |
| Vig. sorológica em suínos asselvajados | Agentes de manejo populacional | OESA | --- | Fundos/ associações |
Lab. credenciado
LFDA/MAPA2 |
Lab. credenciado
LFDA/MAPA2 |
Lab. credenciado
LFDA/MAPA2 |
DSA/ MAPA |
| Inspeções em estabelecimentos de criação | OESA | OESA | OESA | --- | --- | --- | --- | DSA/ MAPA |
| Inspeção em abatedouros | SIF, SIE,SIM | --- | ---- | --- | --- | --- | --- | DSA/ MAPA |
Observações: 1O envio de amostras e realização de testes somente em casos prováveis. 2O LFDA/MAPA realizará os testes confirmatórios.
¶ Base legal e documentos de referência
1. Best practices for risk-based and cost-effective animal health surveillance in the European Union, Risksur.
2. BRASIL. Decreto nº 24.548, de 31 de julho de 1934. Diário Oficial da União, Poder Legislativo, Rio de Janeiro, RJ, 14 jul. 1934. Seção 1, p. 14250.
3. BRASIL. Ministério da Agricultura, Pecuária e Abastecimento. Secretaria de Defesa Agropecuária. Departamento de Saúde Animal. Norma Interna DSA n° 05 de 2009. Ementa: Aprova o manual de procedimentos do sistema de vigilância sanitária na zona livre de peste suína clássica.
4. BRASIL. Ministério da Agricultura, Pecuária e Abastecimento. Secretaria de Defesa Agropecuária. Departamento de Saúde Animal. Norma Interna DSA n° 03 de 2014. Ementa: Aprova o Plano de Vigilância em Suídeos Asselvajados na zona livre de PSC do Brasil.
5. FAO. 2014. Risk-based disease surveillance – A manual for veterinarian son the design and analysis of surveillance for demonstration of freedom from disease. FAO Animal Production and Health Manual No. 17. Rome, Italy.
6. Guidelines for Developing an Animal Health Surveillance Plan, USDA – APHIS – VS – Centers for Epidemiology and Animal Health - National Surveillance Unit.
7. Manual of Basic Animal Disease Surveillance, Dr. Angus Cameron, AFRICAN UNION INTERAFRICAN BUREAU FOR ANIMAL RESOURCES, 2012.
8. MINISTERIO DE AGRICULTURA, PESCA Y ALIMENTACIÓN - ESPAÑA - Programa nacional de vigilância sanitária porcina adaptado al incremento de riesgo de incursión de peste porcina africana em la EU, Año 2020.
9. MOTA, A.L.A.A. Avaliação do Sistema de Vigilância da Peste Suína Clássica nos estados de Santa Catarina e Rio Grande do Sul. Brasília: Faculdade de Agronomia e Medicina Veterinária, Universidade de Brasília, 2016, 79 p. Tese de Doutorado.
10. Produção de suínos: teoria e prática / Coordenação editorial, Associação Brasileira de Criadores de Suínos; Coordenação Técnica da Integrall Soluções em Produção Animal - Brasília, DF, 2014.
11. Sobestiansky, Juriji. Doenças dos Suínos/editores, Juriji Sobestiansky, David Barcellos. – Goiânia: Canone Editorial, 2007. 960p.
12. Swine Hemorrhagic Fevers: African and Classical Swine Fever Integrated Surveillance Plan. United States Department of Agriculture - Animal and Plant Health Inspection Service Veterinary Services May 2019.
13. World Organisation for Animal Health – OIE. Animal health surveillance. Terrestrial Animal Health Code, CHAPTER 1.4. 2019.
14. World Organisation for Animal Health – OIE. Infection with african swine fever virus. Terrestrial Animal Health Code, CHAPTER 15.1. 2019.
15. World Organisation for Animal Health – OIE. Infection with classical swine fever virus. Terrestrial Animal Health Code, CHAPTER 15.2. 2019.
16. World Organisation for Animal Health – OIE. Infection with porcine reproductive and respiratory syndrome virus. Terrestrial Animal Health Code, CHAPTER 15.2. 2019.
17. World Organisation for Animal Health – OIE. Manual of Diagnostic Tests and Vaccines for Terrestrial Animals. African swine fever, Terrestrial Manual, Chapter 3.8.1. 2019.
18. World Organisation for Animal Health – OIE. Manual of Diagnostic Tests and Vaccines for Terrestrial Animals. Classical swine fever (CSF), Terrestrial Manual, Chapter 3.8.3. 2019.
19. World Organisation for Animal Health – OIE. Manual of Diagnostic Tests and Vaccines for Terrestrial Animals. Porcine reproductive and respiratory syndrome, Terrestrial Manual, Chapter 3.8.6. 2015.
20. ZIMMERMAN, J.J; LOCKE, A. K.; RAMIREZ, A; SCHWARTZ, K.; STEVENSON, G.W. Diseases of swine, 10TH EDITION, 2012, Iowa State Pres, 968p.
¶ Disposições gerais
As sugestões para aprimoramento ou possíveis correções deste documento devem ser direcionadas ao Departamento responsável, para alinhamento das melhores práticas de mercado, legislação vigente e/ou regulamentações, que não tenham sido contempladas na versão vigente.
¶ Histórico de revisões
| Versão | Conteúdo alterado | Data | Motivo |
|---|---|---|---|
| 2.0 | Inclusão dos tópicos: Folha de rosto, Folha resumo, Disposições gerais e Histórico de revisão. | 18/04/2023 | Transcrição da nova edição do manual para o modelo validado pela SDA no Projeto de elaboração do modelo de manualização da SDA. |
¶ Anexos
¶ ANEXO I - PROCEDIMENTOS PARA VIGILÂNCIA SOROLÓGICA ATIVA EM SUÍNOS DOMÉSTICOS
¶ 1. Identificação dos estabelecimentos
Cada estabelecimento de criação a ser amostrado terá uma identificação única, que será o Código MAPA, este código será gerado de acordo com o número de estabelecimentos de criação e será disponibilizado através do SIGEP.
ATENÇÃO: OS CÓDIGOS MAPA SERÃO GERADOS PELO DSA. NÃO ATRIBUA A NUMERAÇÃO AOS ESTABELECIMENTOS DE CRIAÇÃO IDENTIFICADOS SEM CONSULTA PRÉVIA.
¶ 2. Seleção dos estabelecimentos de criação a serem amostrados
Os estabelecimentos de criação de suínos para os fins da amostragem são classificados e caracterizados segundo a tabela 1:
Tabela 1. Características da população-alvo do Plano Integrado de Vigilância para PSC, PSA e PRRS.
| POPULAÇÃO | CARACTERÍSTICAS DA PRODUÇÃO | |
|---|---|---|
| Suinocultura Tecnificada | Integrado/ Cooperado | Contrato de comodato, parceria, compra e venda, genética e nutrição |
| Controle técnico sobrea criação | ||
| Separação dos suínos de acordo com a fase de produção | ||
| Condições controladas de genética, nutrição, instalações e sanidade | ||
| Produção em escala | ||
| Independente | Sem contrato, mas inserido em programa de fomento (por meio de outras empresas, cooperativas e mini-integração) | |
| O próprio suinocultor negociao abate (por meio de outras empresasou cooperativas e mini- integração) | ||
| Controle técnico sobrea criação | ||
| Separação dos suínos de acordo com a fase de produção | ||
| Condições controladas de genética, nutrição, instalações e sanidade | ||
| Produção em escala | ||
| Suinocultura Não Tecnificada | Subsistência | Consumo próprio, não é destinado ao comércio ou comércio eventual de suínos excedentes |
| Comercial | Não há controle técnico sobre a criação | |
| Não há controle nutricional (restos de alimentos ou de culturas) | ||
| Instalações rústicas e improvisadas | ||
| Não há separação dos suínos de acordo com a fase de produção | ||
| Comércio local em pequena escalae de forma limitada | ||
| Manejos reprodutivo, nutricional e sanitário precários ou inexistentes | ||
| Suínos asselvajados | Suíno em vida livre no ambiente, de maneira selvagem | |
Os tipos de estabelecimentos que serão amostrados são os seguintes:
• Suinocultura Tecnificada:
• Granja de Reprodutores Suínos Certificada (GRSC): a amostragem envolverá todas as GRSC conforme protocolo de certificação estabelecido;
• Unidade Produtora de Leitões (UPL) e Ciclo Completo (CC): a seleção de UPL e CC a serem amostrados será realizada pelo DSA, através da base de dados cadastrais disponibilizados por cada UF.
• Suinocultura Não Tecnificada: A seleção dos municípios para amostragem será realizada pelo DSA, porém a seleção dos “Estabelecimentos de Criação de Suínos Não Tecnificados” ficará a cargo dos Médicos Veterinários responsáveis pelas Unidades Veterinárias Locais do OESA, promovendo a amostragem de estabelecimentos que se enquadrem na suinocultura não tecnificada. Os estabelecimentos selecionados necessitam possuir um rebanho com no mínimo 5 (cinco) suínos adultos. Devem ser priorizados os estabelecimentos que possuam indícios de prática de comércio local. Também devem ser priorizados aqueles que possuam um ou mais fatores de risco descritos abaixo. Além dessas características, a busca por estabelecimentos com um ou mais fatores de risco identificados abaixo é de alta valia para a detecção precoce da circulação das doenças procuradas:
- Estabelecimentos rurais com suínos contíguos ou próximos a depósitos de resíduos sólidos urbanos;
- Estabelecimentos rurais com suínos com fornecimento de resíduos alimentares (lavagem) aos suínos;
- Estabelecimentos rurais contíguos ou próximos a locais de ingresso internacional de pessoas e produtos como aeroportos, portos, ferrovias, rodoviárias e postos de fronteira internacional e divisas com zonas não livres;
- Estabelecimentos rurais localizados em fronteiras internacionais ou divisas com Estados, países ou zonas não livres de PSC, PSA e PRRS;
- Estabelecimentos rurais contíguos ou próximos a abatedouros frigoríficos ou graxarias;
- Estabelecimentos rurais pertencentes a proprietários que mantêm suínos em diferentes estabelecimentos, especialmente em outros países ou zona não livre de PSC, PSA e PRRS;
- Estabelecimentos rurais pertencentes a proprietários que comercializam suínos para zonas não livres;
- Proximidade a reservas naturais, áreas de proteção ambiental ou parques nacionais com a presença de suínos asselvajados;
- Estabelecimentos rurais em assentamentos rurais, aldeias indígenas, áreas periurbanas, comunidades carentes ou qualquer outra situação em que a biosseguridade esteja comprometida e o sistema de pecuária exija atenção veterinária especial pelo SVO;
- Estabelecimentos rurais contíguos ou próximos a laboratórios autorizados a manusear material infeccioso para PSC, PSA e PRRS;
- Estabelecimento com suínos contíguos ou próximos a paradas de ônibus com origem em zonas não livres.
Outros fatores podem ser identificados como de risco para PSC, PSA e PRRS, conforme a caracterização da área ou do município, e ser incluídos no componente de vigilância.
Caso haja mais de um estabelecimento selecionado no município, deve haver uma distância mínima de 5 Km entre os estabelecimentos amostrados.
¶ 3. Amostragem dos suínos
Para amostragem dos suínos, em cada estabelecimento de criação selecionado, deverão ser considerados apenas os suínos adultos (acima de 8 (oito) meses de idade ou que já estiverem em fase reprodutiva), visto que esses apresentam maior probabilidade de ter anticorpos contra as doenças-alvo do Plano Integrado de Vigilância, pois permaneceram mais tempo expostos ao risco de infecção, no caso de haver atividade viral no estabelecimento de criação.
Os suínos selecionados que não possuírem identificação individual, poderão receber identificação individual numérica de longa duração, a critério do OESA, que deverá ser registrada no Formulário de Colheita de Amostras de Suínos Domésticos (Formulário 1) e facilitará a investigação complementar, caso ocorra.
Os proprietários devem ser orientados a não movimentar ou consumir os animais amostrados e comunicar imediatamente ao OESA em casos de doenças, mortes ou desaparecimentos dos suínos.
O Médico Veterinário responsável pela colheita das amostras deverá realizar a inspeção geral e o exame clínico dos suínos amostrados, informando os resultados no respectivo Formulário de Colheita de Amostras de Suínos Domésticos (Formulário 1).
A amostragem dos suínos será realizada de acordo com a tabela abaixo, baseada numa prevalência intra-rebanho de suínos com anticorpos específicos para a doença igual a 15%, almejando uma sensibilidade de rebanho maior ou igual a 95%.
Tabela 2. Número de suínos a amostrar por estabelecimento de acordo com o número de suínos adultos existentes.
| Número de suínos adultos | Nº de amostras a serem colhidas * |
|---|---|
| 5 -10 | Todos |
| 11 – 15 | 11 |
| 16 – 20 | 13 |
| 21 - 30 | 15 |
| 31 -40 | 16 |
| 41 - 50 | 17 |
| 51-70 | 19 |
| ≥ 71 | 20 |
*Prevalência de animais com anticorpos específicos para a doença é igual a 15% com sensibilidade de rebanho ≥ 95%.
¶ 4. Colheita e acondicionamento de amostras
A colheita de amostra de sangue deverá ser feita de modo a evitar sua contaminação, que pode inviabilizar a realização e interpretação dos testes laboratoriais. Por essa razão, deverá ser utilizado material estéril e descartável.
Após a devida contenção do suíno, o sangue poderá ser colhido por meio de punção da veia jugular ou da cava cranial, utilizando um conjunto (agulha, seringa e tubo previamente identificados) para cada suíno.
O volume colhido deverá ser de, no mínimo, 7,0 ml e deverá preencher, no máximo, 60% da capacidade do tubo de colheita, sem a aplicação de alta pressão no momento da transferência para o tubo de modo a evitar hemólise.
Para minimizar possíveis riscos sanitários, recomenda-se que os trabalhos de fiscalização aos estabelecimentos e de vigilância por meio de colheita de amostras obedeçam aos procedimentos de biosseguridade.
A adoção de boas práticas no processo de colheita, conservação e remessa de amostras constitui um dos principais fatores para o sucesso na obtenção de material para diagnóstico laboratorial.
Para obtenção de uma amostra de soro adequada, os tubos com sangue deverão ser mantidos inclinados, ao abrigo da luz e em temperatura ambiente, até a completa coagulação e liberação do soro (geralmente de 2 a 3 horas) ou centrifugados em equipamento próprio.
Após a completa formação do coágulo sanguíneo, o soro deverá ser transferido para um microtubo tipo Eppendorf devidamente identificado. A quantidade mínima de soro a ser encaminhada ao laboratório deverá ser de 1,5 ml, observando o preenchimento máximo de 2/3 (dois terços) do microtubo, pois ao congelar, haverá aumento do volume com risco de extravasamento do conteúdo.
Os tubos contendo as amostras deverão ser congelados na vertical (em pé) e mantidos, preferencialmente a -20°C (menos vinte graus Celsius), evitando-se o descongelamento. Nunca congelar amostras de soro com a presença de coágulos, pois ocorrerá hemólise e prejuízo dos testes laboratoriais.
Caso não se disponha de meios para o congelamento das amostras, estas deverão ser mantidas sob refrigeração e chegar ao laboratório no prazo máximo de dois dias.
As amostras de soro deverão estar em condições adequadas, ou seja, límpidas, congeladas/refrigeradas, identificadas de forma legível e bem acondicionadas.
¶ 5. Identificação das amostras
As amostras de soro deverão ser identificadas com o Código MAPA do estabelecimento selecionado.
A identificação da amostra deverá constar no formulário de colheita e no microtubo.
As amostras deverão ser identificadas com etiquetas padronizadas geradas pelo sistema SIGEP. A identificação deverá constar no Formulário de Colheita de Amostras de Suínos Domésticos (Formulário 1) e no microtubo.
¶ 6. Preenchimento do Formulário
O Formulário de Colheita de Amostras de Suínos Domésticos (Formulário 1) deverá ser preenchido com letra legível e caneta esferográfica e ser assinado pelo MVO responsável pela colheita. Este formulário estará disponível no SIGEP.
Uma cópia do formulário deverá ser encaminhada junto com as amostras aos Laboratórios Públicos Credenciados que realizarão a análise das amostras.
O formulário original de colheita deverá ser digitalizado e anexado ao formulário de colheita preenchido no SIGEP, além de arquivado na UVL responsável pelo estabelecimento selecionado.
¶ 7. Embalagem e remessa das amostras ao Laboratório Público Credenciado
Antes do encaminhamento ao Laboratório Público Credenciado ou à central estadual de recepção e conferência, o MVO responsável pela colheita e pelo preenchimento do formulário de colheita deverá realizar uma última conferência para verificar se todas as informações e devidas identificações estão correlatas às amostras colhidas do respectivo estabelecimento.
¶ 8. Sistema SIGEP para gerenciamento do estudo
Para o gerenciamento das informações sobre os estabelecimentos e amostras oriundas de “Suinocultura Tecnificada” ou “Suinocultura Não Tecnificada de Comércio Local” será utilizado o SIGEP.
A inserção dos dados que constam dos formulários de colheita de amostras no SIGEP será de responsabilidade do OESA.
¶ 9. Laboratórios
As amostras oriundas dos estabelecimentos de “Suinocultura Tecnificada” ou “Suinocultura Não Tecnificada de Comércio Local” serão analisadas pelos Laboratórios Públicos Credenciados que realizarão os testes sorológicos de triagem:
• Centro de Diagnóstico de Sanidade Animal – CEDISA, Santa Catarina;
• Centro de Diagnóstico Marcos Enrietti – CDME, Paraná;
• Instituto Biológico – IB, São Paulo;
• Instituto Mineiro de Agropecuária – IMA, Minas Gerais;
• Instituto de Pesquisas Veterinárias Desidério Finamor - IPVDF, Rio Grande do Sul;
• Laboratório de Análise e Diagnóstico Veterinário – LABVET, Goiás.
¶ 10. Testes de diagnóstico
Para o Plano de vigilância integrada para PSC, PSA e PRRS, o teste de ELISA será empregado como teste de triagem.
Desta forma, ao identificar uma amostra positiva ou inconclusiva no ELISA o laboratório deve enviar esta amostra ao LFDA de referência para realização do teste confirmatório.
¶ 11. Resultado laboratorial
Todo resultado laboratorial deverá ser inserido no SIGEP assim que forem obtidos. Não haverá necessidade da emissão e envio de relatórios de ensaio. Os resultados positivos, além de inseridos no SIGEP, devem ser imediatamente enviados para a Unidade Central do OESA e para o serviço de saúde animal da Superintendência Federal de Agricultura, Pecuária e Abastecimento (SFA).
¶ 12. Investigação epidemiológica complementar
A detecção de pelo menos uma amostra positiva ou inconclusiva ao teste laboratorial de triagem (ELISA) desencadeia uma investigação epidemiológica complementar, que ainda deve ser registrada no SIGEP.
Nesse caso, deverão ser adotados os procedimentos descritos no Anexo IV deste manual “PROCEDIMENTOS PARA VIGILÂNCIA COMPLEMENTAR”.
Caso tenha ocorrido investigação complementar, todos os documentos correspondentes deverão ser arquivados Unidade Central do OESA e nas UVLs que realizaram a investigação.
¶ 13. Pagamento dos custos de remessa e análise das amostras
Os pagamentos referentes aos custos com remessas de amostras pelo SVO e testes laboratoriais da vigilância ativa do Plano integrado de vigilância para PSC, PSA e PRRS poderão ser acordados, preferencialmente, com a iniciativa privada.
¶ ANEXO II - VIGILÂNCIA CLÍNICA EM ESTABELECIMENTOS DE CRIAÇÃO
Neste componente, a vigilância é ativa e está estruturada de acordo com diferentes categorias de risco, considerando os fatores para a introdução, manutenção e disseminação do vírus da PSC, PSA e PRRS. Ao considerar os fatores de risco para uma doença específica, aumenta-se a probabilidade de detecção de um animal infectado sem necessariamente aumentar o número de animais examinados quando comparado a um sistema de vigilância que não seja baseada em risco, ou seja, essa técnica produz aumento de sensibilidade do sistema bem como a sua eficiência e eficácia.
Por essa razão, a vigilância realizada em estabelecimentos de criação e áreas de maior risco é de grande importância, pois pode detectar casos prováveis de doenças dos suínos de notificação obrigatória. Essa vigilância propicia, ainda, a colheita e registro de informações referentes aos rebanhos de suínos e a interação do SVO com os responsáveis pelo manejo dos animais para o desenvolvimento de ações de educação continuada em saúde animal.
Para este componente, deve-se aplicar o Formulário de Inspeção em Estabelecimentos de Criação (Formulário 4) buscando-se caracterizar o risco atribuído ao estabelecimento de criação, aspectos produtivos e sanitários da criação, informações sobre o trânsito de suínos, manifestações clínicas encontradas e/ou relatadas.
Caso o resultado da vigilância seja caso provável de síndrome hemorrágica ou PRRS, deve-se adotar os procedimentos descrito nas respectivas fichas técnicas.
O SVO deverá acionar o médico veterinário responsável técnico ou sanitarista da granja previamente à inspeção para que possa acompanhar a atividade e esclarecer os índices zootécnicos e sanitários. Caso não haja disponibilidade do médico veterinário, as inspeções devem seguir o cronograma proposto pelo SVO.
Fatores de risco para seleção das propriedades a serem inspecionadas:
• Estabelecimentos rurais com suínos próximos a depósitos de resíduos sólidos urbanos;
• Estabelecimentos rurais com suínos com fornecimento de resíduos alimentares (lavagem) aos suínos;
• Estabelecimentos rurais contíguos a locais de ingresso internacional de pessoas e produtos como aeroportos, portos, ferrovias, rodoviárias e postos de fronteira internacional e divisas com zonas não livres;
• Estabelecimentos rurais localizados em fronteiras internacionais ou divisas com estados, países ou zonas não livres de PSC, PSA e PRRS;
• Estabelecimentos rurais contíguos a abatedouros frigoríficos ou graxarias;
• Estabelecimentos rurais pertencentes a proprietários que mantêm suínos em diferentes estabelecimentos, especialmente em outros países ou zona não livre de PSC, PSA e PRRS;
• Estabelecimentos rurais pertencentes a proprietários que comercializam suínos para zonas não livres;
• Proximidade a reservas naturais, áreas de proteção ambiental ou parques nacionais com a presença de suínos asselvajados;
• Estabelecimentos rurais em assentamentos rurais, aldeias indígenas, áreas periurbanas, comunidades carentes ou qualquer outra situação em que a biosseguridade esteja comprometida e o sistema de pecuária exija atenção veterinária especial pelo SVO;
• Estabelecimentos rurais contíguos a laboratórios autorizados a manusear material infeccioso para PSC, PSA e PRRS;
• Estabelecimento com suínos próximos a paradas de ônibus com origem em zonas não livres.
¶ ANEXO III - PROCEDIMENTOS PARA VIGILÂNCIA SOROLÓGICA ATIVA EM SUÍNOS ASSELVAJADOS
¶ 1. Agente de Manejo Populacional
A vigilância sorológica na população de suínos asselvajados será realizada mediante parceria entre os Agentes de Manejo Populacional autorizados e o SVO.
Os OESAs deverão cadastrar e realizar treinamento para os Agentes de Manejo Populacional para colheita de amostras sorológicas e sobre as doenças de notificação obrigatória.
¶ 2. Documentação e kit para colheita de amostra
Os Agentes de Manejo Populacional deverão estar devidamente cadastrados e capacitados pelo SVO e apresentar a cópia do Certificado de Regularidade (CR) válido para a retirada do kit de colheita de amostras:
A relação do kit mínimo para colheita de amostras segue abaixo e poderá ser adequado à realidade de cada Unidade Federativa:
• Formulário de Colheita de Amostras de Suínos Asselvajados (Formulário 2);
• luvas de látex (EPI);
• tubo tipo Falcon com tampa de rosca, capacidade de 15ml;
• tubo tipo Falcon com tampa de rosca, capacidade de 50ml;
• pipeta Pasteur de 3 ml;
• saco plástico com fechamento do tipo ziploc, 23 x 17cm;
• caixa isotérmica de 10 litros;
• folheto explicativo com as instruções para a colheita do material.
¶ 3. Colheita, recepção e acondicionamento das amostras
A correta orientação sobre os procedimentos de colheita e acondicionamento de amostras oriundas de suínos asselvajados é fundamental para a qualidade da amostra e um diagnóstico preciso. A contaminação das amostras pode inviabilizar a realização e interpretação dos testes laboratoriais.
O Agente de Manejo Populacional tem até 48 horas, após a colheita, para entregar na UVL amostras de sangue total refrigeradas, que deverão ser centrifugadas na UVL e o soro congelado, e até 7 dias para amostras de soro sanguíneo congeladas. As amostras de soro sanguíneo deverão permanecer congeladas na UVL até o envio ao Laboratório Público Credenciado ou à central estadual de recepção e conferência do OESA.
As amostras deverão ser recebidas e remetidas pela UVL independente da qualidade que foram entregues pelo Agente de Manejo Populacional. Ao observar amostras de má qualidade, o MVO deve orientar o Agente de Manejo Populacional sobre as boas práticas de colheita para obtenção de uma amostra de qualidade.
Os tubos contendo as amostras deverão ser congelados na vertical (em pé) e mantidos preferencialmente a -20°C (menos vinte graus Celsius), evitando-se o descongelamento. Nunca congelar amostras de soro com a presença de coágulos, pois ocorrerá hemólise e prejuízo dos testes laboratoriais.
As amostras de soro deverão estar em condições adequadas, ou seja, congeladas/refrigeradas, identificadas de forma legível e bem acondicionadas.
¶ 4. Identificação das amostras e preenchimento do formulário
O Agente de Manejo Populacional deverá entregar as amostras, na UVL onde retirou o kit ou em outra previamente determinada, a critério do OESA, acompanhadas do Formulário de Colheita de Amostras de Suínos Asselvajados (Formulário 2) preenchido e assinado.
A UVL deverá conferir a identificação de todas as amostras juntamente com o(s) formulário(s) de colheita e as informações deverão ser inseridas no SIGEP.
Enviar uma cópia do formulário de colheita do Agente de Manejo Populacional juntamente com as amostras e arquivar o original na UVL.
¶ 5. Embalagem e remessa das amostras ao Laboratório Público Credenciado
Antes do encaminhamento ao Laboratório Público Credenciado ou à central estadual de recepção e conferência, o MVO responsável pelas amostras e pelo preenchimento do formulário de colheita deverá realizar uma última conferência para verificar se todas as informações e devidas identificações estão correlatas às amostras colhidas daquele estabelecimento.
Para encaminhamento a um dos Laboratórios Públicos Credenciados, as amostras deverão estar congeladas, embaladas em sacos plásticos, identificadas de forma legível, acompanhadas dos respectivos formulários de colheita e bem acondicionadas.
¶ 6. Sistema SIGEP para gerenciamento do estudo
Para o gerenciamento das informações sobre as amostras oriundas de suínos asselvajados será utilizado o SIGEP.
A inserção dos dados que constam dos formulários de colheita de amostras no SIGEP será de responsabilidade do OESA.
¶ 7. Laboratórios
As amostras oriundas de suínos asselvajados serão analisadas pelos Laboratórios Públicos Credenciados que realizarão os testes sorológicos de triagem:
• Centro de Diagnóstico de Sanidade Animal – CEDISA, Santa Catarina;
• Centro de Diagnóstico Marcos Enrietti – CDME, Paraná;
• Instituto Biológico – IB, São Paulo;
• Instituto Mineiro de Agropecuária – IMA, Minas Gerais;
• Instituto de Pesquisas Veterinárias Desidério Finamor – IPVDF, Rio Grande do Sul;
• Laboratório de Análise e Diagnóstico Veterinário – LABVET, Goiás.
¶ 8. Testes de diagnóstico
Para o Plano de vigilância integrada para PSC, PSA e PRRS, o teste de ELISA será empregado como teste de triagem.
Desta forma, ao identificar uma amostra positiva ou inconclusiva no ELISA o Laboratório Público Credenciado deve enviar esta amostra ao LFDA de referência para realização do teste confirmatório.
¶ 9. Resultado laboratorial
Todo resultado laboratorial deverá ser enviado para a Unidade Central do OESA e para o serviço de saúde animal da Superintendência Federal de Agricultura, Pecuária e Abastecimento (SFA).
Na Unidade Central do OESA, deverá ser mantido um arquivo organizado e auditável sobre todas as amostras colhidas e os respectivos resultados laboratoriais. Uma cópia digitalizada do resultado deverá ser inserida no SIGEP.
¶ 10. Investigação epidemiológica complementar
A detecção de pelo menos um suíno asselvajado positivo ou inconclusivo ao teste laboratorial de triagem (ELISA) desencadeia uma investigação epidemiológica complementar, que não requer registro no e-SISBRAVET.
Nesse caso, deverão ser adotados os procedimentos descritos no Anexo IV deste manual “PROCEDIMENTOS PARA VIGILÂNCIA COMPLEMENTAR”.
Caso tenha ocorrido investigação complementar, todos os documentos correspondentes deverão ser arquivados Unidade Central do OESA e nas UVLs que realizaram a investigação.
¶ 11. Pagamento dos custos de remessa e análise das amostras
O pagamento referente aos custos com a remessa e análises das amostras para o Plano integrado de vigilância para PSC, PSA e PRRS deverá ser acordado preferencialmente com a iniciativa privada.
¶ ANEXO IV - PROCEDIMENTOS PARA VIGILÂNCIA COMPLEMENTAR
Este texto tem como objetivo padronizar os procedimentos de investigação epidemiológica a serem adotados quando da detecção de resultados positivos ou inconclusivos nas vigilâncias sorológicas realizadas pelo Plano Integrado de Vigilância para PSC, PSA e PRRS.
Na vigilância sorológica, os resultados positivos/inconclusivos podem ser decorrentes dos seguintes fatores:
• Infecção natural pelo vírus da PSC, PSA e PRRS;
• Vacinação contra PSC, PSA (se disponível e autorizada pelo DSA) e PRRS;
• Anticorpos maternos decorrentes de fêmeas imunizadas;
• Reação cruzada com outros Pestivirus (Diarreia Viral Bovina - BVD e “Doença das Fronteiras” dos ovinos - BD), no caso da PSC;
• Reações não específicas do teste utilizado.
Desta forma, devemos dispor de um procedimento eficaz que indique a presença de infecção pelos vírus da PSC, PSA e PRRS por meio de testes laboratoriais (confirmatórios e diferenciais) e investigações complementares no estabelecimento de origem das amostras.
O procedimento de investigação epidemiológica complementar descrito a seguir deve ser iniciado após resultado positivo ou inconclusivo no teste de triagem ELISA e será executado pelo OESA, com acompanhamento do serviço de saúde animal da SFA. Seu objetivo é obter um diagnóstico final conclusivo sobre a presença do vírus da PSC, PSA e PRRS nas populações de suínos das UF que compõem a ZL de PSC.
¶ 1. INVESTIGAÇÃO COMPLEMENTAR PARA PSC EM SUÍNOS DOMÉSTICOS
A. Resultado laboratorial positivo e inconclusivo no teste ELISA.
As amostras com resultados laboratoriais positivos ou inconclusivos para PSC no teste ELISA devem ser encaminhadas para rede de referência do LFDA, pelos laboratórios públicos credenciados, e serão testadas no teste de neutralização viral (VN) para PSC e BVD.
Quando do resultado positivo ou inconclusivo no ELISA, o OESA deverá conduzir uma detalhada investigação no estabelecimento de origem da amostra.
Caso haja presença de suínos com sinais clínicos compatíveis com síndrome hemorrágica, o estabelecimento deverá ser interditado e deverão ser adotados os procedimentos para caso provável descritos na ficha técnica de PSC (com registros no e-Sisbravet).
Caso não haja presença de suínos com sinais clínicos compatíveis com síndrome hemorrágica, o estabelecimento deverá permanecer sob vigilância, sendo acompanhada com fiscalizações semanais, devidamente registradas no Formulário de Inspeção de Monitoramento (Formulário 3), disponível no SIGEP, até o resultado da VN.
O proprietário deverá ser instruído a não movimentar ou consumir os animais amostrados e de que, ao observar qualquer alteração do comportamento dos animais ou alta mortalidade no seu rebanho, deverá notificar o OESA imediatamente.
Nesse momento, não há necessidade de interdição do estabelecimento, visto que os animais não apresentam sinais clínicos compatíveis com síndrome hemorrágica e são esperadas reações falso-positivas ao teste de triagem ELISA.
Se os suínos permanecerem sem sinais clínicos compatíveis com síndrome hemorrágica, a investigação será encerrada quando o resultado da VN para PSC for negativo.
B. Resultado laboratorial positivo no teste de neutralização viral – VN.
Caso o resultado da VN para PSC seja positivo, a investigação em curso terá continuidade. Todas as informações da investigação ainda deverão ser registradas no SIGEP na forma do Formulário de Inspeção de Monitoramento (Formulário 3).
Novamente, deverá ser realizado um exame clínico do rebanho suíno, bem como nova investigação epidemiológica, sempre buscando indícios da ocorrência de síndrome hemorrágica dos suínos.
Se forem constatados sinais clínicos compatíveis com PSC ou PSA, deverão ser adotados os procedimentos para caso provável descritos nas fichas técnicas (com registros no e-Sisbravet).
Caso não sejam observados suínos com sinais clínicos ou lesões sugestivas de PSC, deverão ser colhidas amostras de sangue total (com EDTA) dos suínos do estabelecimento para realização do teste de PCR, com identificação individual dos suínos e preenchimento do Formulário de Colheita de Amostras Complementares (Formulário 5) no SIGEP.
Amostragem
Para a amostragem consideramos as seguintes faixas etárias:
• Adultos: reprodutores (machos e fêmeas) e castrados acima de oito meses.
• Leitões: suínos que ainda não entraram na vida reprodutiva (abaixo de oito meses).
Para o cálculo da amostra, deverá ser considerado o número total de suínos existentes no estabelecimento e o número de amostras será calculado conforme Tabela 1.
Para a escolha dos suínos a serem amostrados, priorizar a faixa etária de leitões. Não havendo suínos suficientes na faixa etária de leitões, complementar a amostragem com suínos da faixa etária superior (adultos).
Para determinação do número de suínos a ser amostrado em cada estabelecimento, foram considerados os seguintes parâmetros: sensibilidade de 95% do sistema de diagnóstico (PCR), confiança de 95% e prevalência mínima esperada em cada estabelecimento de 5% de suínos infectados.
Tabela 1. Número de suínos a serem amostrados por estabelecimento.
| Número de suínos | Nº de amostras a serem colhidas * |
|---|---|
| 5 - 10 | Todos |
| 11 - 20 | 11 |
| 21 - 30 | 15 |
| 31 - 40 | 19 |
| 41 - 50 | 21 |
| 51 - 60 | 25 |
| 61 - 70 | 27 |
| 71 - 100 | 33 |
| 101 - 200 | 44 |
| 201 - 400 | 50 |
| 401 - 600 | 55 |
| >600 | 56 |
*Prevalência de animais com anticorpos específicos para a doença é igual a 5% com sensibilidade de rebanho ≥ 95%.
Os cálculos propostos foram realizados com a ferramenta do aplicativo Epi Tools - Epidemiology Toobox App., versão 6.0, utilizando-se a opção do fator de correção para populações finitas.
Referência: Dohho I, Martin W, Stryhn H (2003). Veterinary Epidemiologic Research. AVC Inc, Charlottetown, Prince Edward Island, Cana, pp. 47 and pp 102-103.
Todos os suínos amostrados deverão estar identificados individualmente. Aqueles que não possuírem, deverão ser brincados pelo OESA no momento da colheita. A identificação presente no frasco de sangue deve permitir relacioná-lo ao animal amostrado.
As amostras deverão ser enviadas ao LFDA/MG, mediante contato prévio, acompanhadas de cópia do Formulário de Colheita de Amostras Complementares (Formulário 5).
Os estabelecimentos que apresentarem todos os resultados negativos e os suínos permanecerem sem sinais clínicos da doença terão a investigação complementar dada por encerrada. Esses estabelecimentos deverão ser incluídos na relação de estabelecimentos objeto de vigilância ativa da respectiva UVL, ou seja, estabelecimentos de maior risco.
C. Resultado laboratorial tóxico ou inconclusivo no teste de neutralização viral.
Quando o resultado da VN for tóxico ou inconclusivo, podemos ter duas situações:
a) quando o animal amostrado dispuser de identificação: deverá ser colhida nova amostra de soro deste animal com preenchimento do Formulário de Colheita de Amostras de Suínos Domésticos (Formulário 1). A amostra deverá ser enviada ao LFDA-MG para repetição do teste VN. Permanecendo o resultado tóxico ou inconclusivo, colher amostras de sangue total (com EDTA) dos suínos existentes conforme amostragem descrita na Tabela 1 do item “B. Resultado laboratorial positivo no teste de neutralização viral - VN” para realização de PCR com preenchimento do Formulário de Colheita de Amostras Complementares (Formulário 5). Os registros de vigilância deverão ser feitos no Formulário de Inspeção de Monitoramento (Formulário 3).
b) quando o animal amostrado não dispuser de identificação: deverão ser colhidas amostras de sangue total (com EDTA) dos suínos existentes, para realização de PCR, seguindo a amostragem descrita na Tabela 1 do item “B. Resultado laboratorial positivo no teste de neutralização viral - VN”, e com realização da identificação individual dos suínos amostrados. Os registros de vigilância deverão ser feitos no Formulário de Inspeção de Monitoramento (Formulário 3) e as amostras de sangue total deverão ser identificadas no Formulário de Colheita de Amostras Complementares (Formulário 5).
D. Resultado laboratorial positivo na PCR.
Nos casos de resultados positivos na PCR, o(s) suíno (s) positivo(s) deverá(ão) ser eutanasiado(s) para colheita de amostras de órgãos (20 a 50 gramas de: tonsilas, baço, linfonodos e válvula íleo-cecal) com vistas à identificação do vírus da PSC. O material colhido e o Formulário de Colheita de Amostras Complementares (Formulário 5) deverão ser encaminhados ao LFDA-MG, mediante contato prévio. Os registros de vigilância deverão ser feitos no Formulário de Inspeção de Monitoramento (Formulário 3).
O diagnóstico final e conclusivo da investigação levará em consideração todos os resultados laboratoriais e as investigações clínico-epidemiológicas realizadas no estabelecimento envolvido.
E. Procedimentos em caso de ausência de suínos no estabelecimento suspeito.
Caso, por algum motivo, não existam mais suínos no estabelecimento onde ocorreu positividade ao teste ELISA ou VN, será necessária a colheita de soro dos suínos dos estabelecimentos vizinhos ou naquelas vinculadas epidemiologicamente para a realização de testes sorológicos.
Nessa investigação estará incluída a colheita de soro dos suínos existentes nesses estabelecimentos, por amostragem, conforme a Tabela 5 do Plano Integrado de Vigilância.
Todas as informações relativas a esses estabelecimentos deverão ser registradas nos formulários Formulário de Inspeção de Monitoramento (Formulário 3) e Formulário de Colheita de Amostras de Suínos Domésticos (Formulário 1), informando no campo observações do Formulário 1 que se trata de investigação referente ao estabelecimento inicial onde não havia mais suínos.
F. Documentação e registros de dados em sistemas informatizados do MAPA.
Todas as ações executadas na investigação complementar deverão ser registradas em formulários disponíveis no SIGEP. Os registros, bem como a organização destes, devem ser realizados de forma criteriosa garantindo a comprovação das ações executadas em futuras auditorias e missões internacionais. Também é importante o registro fotográfico das inspeções clínicas e necropsias realizadas.
A investigação complementar oriunda de vigilância ativa não requer registro no e-SISBRAVET.
¶ 2. INVESTIGAÇÃO COMPLEMENTAR PARA PRRS EM SUÍNOS DOMÉSTICOS
Após ocorrência de resultado positivo ou inconclusivo para PRRS no teste de triagem (ELISA), o OESA deverá conduzir uma detalhada investigação no estabelecimento de origem da amostra. O rebanho deverá ser inspecionado em busca de sinais clínicos e/ou indicadores zootécnicos e sanitários compatíveis com a ocorrência da PRRS. Também deverão ser levantadas informações sobre possíveis vínculos epidemiológicos, visando uma ampliação da investigação, caso necessário.
Os testes diagnósticos referentes às investigações complementares serão realizados no LFDA/MG, com envio das amostras acompanhadas do Formulário de Colheita de Amostras Complementares (Formulário 5).
Colheita de amostras
Após ocorrência de resultado positivo ou inconclusivo para PRRS no teste de triagem (ELISA) a colheita de material para diagnóstico laboratorial confirmatório é obrigatória. Neste primeiro momento, a interdição dos estabelecimentos investigados dependerá da condição sanitária encontrada pelo OESA na investigação de sinais clínicos e indicadores zootécnicos e sanitários compatíveis com a ocorrência da PRRS.
Critério para tomada de decisão sobre interdição dos estabelecimentos investigados:
• Na presença de sinais clínicos compatíveis com PRRS acompanhada de teste laboratorial POSITIVO: Interdição do estabelecimento e colheita de material para o diagnóstico conforme “caso provável” da Ficha Técnica da PRRS (com registro no e-Sisbravet);
• Na ausência de sinais clínicos compatíveis com PRRS acompanhada de teste laboratorial POSITIVO: Acompanhamento e investigação, com preenchimento do Formulário de Inspeção de Monitoramento (Formulário 3), sem interdição do estabelecimento, e com a colheita de sangue total (com EDTA) ou fluido oral, conforme descrito abaixo. A escolha do tipo de material a ser colhido ficará a critério do OESA, baseando-se na avaliação clínico-epidemiológica, condições sanitárias, biosseguridade e instalações do estabelecimento de suinocultura tecnificada. Para os estabelecimentos de suinocultura não tecnificada, as amostras a serem colhidas são obrigatoriamente as de sangue total.
A. Sangue total com EDTA:
A colheita de sangue total (com EDTA) deve ser realizada considerando o número total de suínos existentes no estabelecimento (conforme Tabela 02) e tomando-se em conta que, caso um estabelecimento esteja infectado com o vírus da PRRS, a prevalência intra-rebanho seria de pelo menos 5% de suínos infectados. A sensibilidade do sistema de diagnóstico (PCR) foi considerada de 95%. Assim, as amostras a serem colhidas em cada estabelecimento deve seguir a Tabela 02. A amostragem por estabelecimento definida na tabela seria suficiente para detectar pelo menos um suíno positivo, em caso de existência de infecção no estabelecimento na prevalência considerada e com nível de confiança de 95%.
A escolha pela colheita de sangue total dispensa a colheita de amostras de fluido oral. Deve ser preenchido o Formulário de Colheita de Amostras Complementares (Formulário 5).
Para a escolha dos suínos a serem amostrados, priorizar as porcas gestantes ou lactantes que possuírem histórico de falhas reprodutivas.
Tabela 02. Número de suínos a serem amostrados por estabelecimento
| Número de suínos adultos | Nº de amostras a serem colhidas * |
|---|---|
| 5 - 10 | Todos |
| 11 - 20 | 11 |
| 21 - 30 | 15 |
| 31 - 40 | 19 |
| 41 - 50 | 21 |
| 51 - 60 | 25 |
| 61 - 70 | 27 |
| 71 - 100 | 33 |
| 101 - 200 | 44 |
| 201 - 400 | 50 |
| 401 - 600 | 55 |
| >600 | 56 |
*Prevalência de animais com anticorpos específicos para a doença é igual a 5% com sensibilidade de rebanho ≥ 95%.
Os cálculos propostos foram realizados com a ferramenta do aplicativo Epi Tools - Epidemiology Toobox App., versão 6.0, utilizando-se a opção do fator de correção para populações finitas.
Referência: Dohho I, Martin W, Stryhn H (2003). Veterinary Epidemiologic Research. AVC Inc, Charlottetown, Prince Edward Island, Cana, pp. 47 and pp 102-103.
B. Fluido Oral:
A colheita de amostras de fluido oral dispensa a colheita de amostras de sangue total. Deve ser preenchido o Formulário de Colheita de Amostras Complementares (Formulário 5). A colheita de fluido oral deve ser realizada somente em estabelecimentos de suinocultura tecnificada, na fase de leitões ao desmame ou em baias de gestação coletiva.
A colheita de fluido oral deverá ser feita em três baias de suínos de, no mínimo, 10 suínos por baia.
Se o número de suínos por baia for inferior a 10, a colheita deverá ser feita em 4 baias de forma que se obtenha exposição de, no mínimo, 30 suínos por granja para fluido oral com as cordas.
Abaixo seguem instruções para colheita do fluido oral:
a) Cordas de algodão (1,3 m) serão suspensas nas baias dos suínos ou amarradas nas laterais firmemente para que não se soltem com o contato e força dos suínos;
b) Cuidar para que a corda não tenha contato com piso, comedouros e bebedouros;
c) Utilizar 1 corda/10 suínos ou uma corda/baia, expostas por 20 – 30 minutos;
d) Cortar a ponta da corda que os suínos mastigaram dentro de um saco plástico com fechamento tipo Ziploc, devidamente identificado, cuidando para que a parte contendo o fluido oral não tenha contato com nada para evitar contaminação;
e) Por compressão manual, fluidos orais serão colhidos em sacos plásticos (tipo Ziploc), decantados em frascos plásticos de 5 ml e estocados a -20°C até o envio ao LFDA-MG;
f) O material deve ser enviado ao laboratório congelado;
g) Identificação do material: identificar no Formulário de Colheita de Amostras Complementares (Formulário 5) os indivíduos das baias amostradas e quando não houver identificação individual dos suínos (mossa, brinco ou tatuagem), esta informação deverá ser registrada nas observações do Formulário 5.
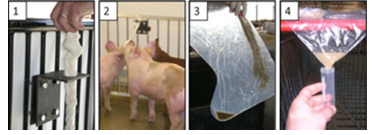
C. Documentação e registros de dados em sistema informatizado do MAPA.
Todas as ações executadas na investigação complementar para PRRS deverão ser registradas em formulários do SIGEP. Os registros, bem como a organização destes, devem ser realizados de forma criteriosa garantindo a comprovação das ações executadas em futuras auditorias e missões internacionais. Também é importante o registro fotográfico das inspeções clínicas.
A investigação complementar oriunda de vigilância ativa não requer registro no e-SISBRAVET.
¶ 3. INVESTIGAÇÃO COMPLEMENTAR PARA PSC EM SUÍNOS ASSELVAJADOS
A. Resultado laboratorial positivo e inconclusivo no teste ELISA.
As amostras com resultados laboratoriais positivos ou inconclusivos para PSC no teste ELISA devem ser encaminhadas para rede de referência do LFDA, pelos laboratórios públicos credenciados, e serão testadas no teste de neutralização viral (VN) para PSC e BVD.
Quando do resultado positivo ou inconclusivo no ELISA, o OESA deverá conduzir uma detalhada investigação no estabelecimento de origem da amostra, onde o suíno asselvajado foi abatido, assim como naquelas com algum vínculo epidemiológico, objetivando obter um diagnóstico final conclusivo sobre a presença, ou não, do vírus da PSC na população de suínos asselvajados.
A investigação será encerrada quando o resultado da VN para PSC for negativo.
Ações no estabelecimento de origem da amostra e estabelecimentos limítrofes com criação de suínos domésticos:
i. inspeção clínica nos suínos domésticos do estabelecimento de origem da amostra e estabelecimentos limítrofes, com preenchimento do Formulário de Inspeção de Monitoramento (Formulário 3);
ii. levantamento do histórico sanitário da pecuária com foco em investigação de doenças que possam apresentar reatividade cruzada nos testes sorológicos para detecção de anticorpos contra o vírus da PSC;
iii. orientação aos criadores de suínos domésticos para providenciarem medidas que evitem contato entre suínos domésticos e asselvajados;
iv. sensibilização e orientação dos criadores de suínos para notificação ao SVO sobre quaisquer alterações ou sinais clínicos compatíveis com a PSC nos suínos domésticos e asselvajados.
Em suínos asselvajados:
i. sensibilização de Agentes de Manejo Populacional de suínos asselvajados para detecção e notificação ao SVO de qualquer animal com clínica e/ou lesões compatíveis com síndrome hemorrágica dos suínos.
ii. investigar junto aos Agentes de manejo populacional o destino das carcaças dos suínos asselvajados reagentes abatidos da mesma procedência.
iii. proceder intensificação da colheita de amostras na área de procedência dos reagentes com acompanhamento do SVO.
B. Resultado laboratorial positivo no teste de neutralização viral (VN)
Ações nos estabelecimentos de criação de suínos domésticos da região
i. o DSA irá delimitar uma área de risco onde deverá ser feito um levantamento das condições de biosseguridade das criações de suínos domésticos;
ii. realizar investigação epidemiológica de possíveis contatos entre suínos domésticos e suínos asselvajados nos estabelecimentos localizadas nas áreas de risco;
iii. realizar investigação clínico-epidemiológica dos suínos dos estabelecimentos, observando sinais da doença e alterações de índices zootécnicos e sanitários do estabelecimento, com preenchimento do Formulário de Inspeção de Monitoramento (Formulário 3);
iv. o DSA irá propor uma vigilância sorológica direcionada aos estabelecimentos da área de risco;
v. orientar o reforço da biosseguridade nos estabelecimentos de suinocultura tecnificada e não tecnificada.
Em suínos asselvajados:
i. reunião para buscar a cooperação de Agentes de Manejo Populacional para intensificar a vigilância, com captura e abate de suínos asselvajados, com colheita de material para pesquisa viral, de acordo com a ficha técnica da PSC, com orientação do PNSS e anuência dos órgãos ambientais.
ii. reforçar a orientação a todos os Agentes de manejo populacional sobre procedimentos de biosseguridade e doenças de notificação obrigatória.
iii. suspender temporariamente o trânsito de carcaças de suínos asselvajados na área de abrangência da investigação.
Em casos suspeitos ou prováveis das doenças em suínos asselvajados, outras amostras (tonsilas, baço, linfonodos, porção distal do íleo e sangue total com EDTA) deverão ser colhidas pelo SVO ou, a critério do SVO, por Agentes de manejo populacional devidamente capacitados e sob supervisão do SVO.
¶ 4. INVESTIGAÇÃO COMPLEMENTAR PARA PRRS EM SUÍNOS ASSELVAJADOS
A. Resultado laboratorial positivo e inconclusivo no teste ELISA.
As amostras com resultados laboratoriais positivos ou inconclusivos para PRRS no teste ELISA devem ser encaminhadas para rede de referência do LFDA, pelos laboratórios públicos credenciados, e serão testadas no teste de PCR.
Quando do resultado positivo ou inconclusivo no ELISA, o OESA deverá conduzir uma detalhada investigação no estabelecimento de origem da amostra, onde o suíno asselvajado foi abatido, assim como naquelas com algum vínculo epidemiológico, objetivando obter um diagnóstico final conclusivo sobre a presença, ou não, do vírus da PRRS na população de suínos asselvajados.
A investigação será encerrada quando o resultado da PCR para PRRS for negativo.
Ações no estabelecimento de origem da amostra e estabelecimentos limítrofes com criação de suínos domésticos:
i. inspeção clínica nos suínos domésticos do estabelecimento de origem da amostra e estabelecimentos limítrofes, com preenchimento do Formulário de Inspeção de Monitoramento (Formulário 3);
ii. orientação aos criadores de suínos domésticos para providenciarem medidas que evitem contato entre suínos domésticos e asselvajados;
iii. sensibilização e orientação dos criadores de suínos para notificação ao SVO sobre quaisquer alterações ou sinais clínicos compatíveis com a PRRS nos suínos domésticos e asselvajados.
Em suínos asselvajados:
i. sensibilização de Agentes de Manejo Populacional de suínos asselvajados para detecção e notificação ao SVO de qualquer animal com clínica e/ou lesões compatíveis com a PRRS.
B. Resultado laboratorial positivo no teste de PCR
Ações nos estabelecimentos de criação de suínos domésticos da região
i. o DSA irá delimitar uma área de risco onde deverá ser feito um levantamento das condições de biosseguridade das criações de suínos domésticos;
ii. realizar investigação epidemiológica de possíveis contatos entre suínos domésticos e suínos asselvajados nos estabelecimentos localizadas nas áreas de risco;
iii. realizar investigação clínica epidemiológica dos suínos dos estabelecimentos, observando sinais da doença e alterações de índices produtivos do estabelecimento, com preenchimento do Formulário de Inspeção de Monitoramento (Formulário 3);
iv. o DSA irá propor uma vigilância sorológica ou virológica direcionada aos estabelecimentos da área de risco.
Em suínos asselvajados:
i. reunião para buscar a cooperação de Agentes de Manejo Populacional para intensificar a vigilância, com captura e abate de suínos asselvajados, com colheita de material para pesquisa viral, de acordo com a ficha técnica da PRRS, com orientação do PNSS e anuência dos órgãos ambientais.
¶ ANEXO V - Formulários
Faça download dos formulários aqui.